
科目: 来源:赣州一中2008~2009学年上学期期中考试高三化学试卷 题型:058
根据如图描述回答下列问题:

(1)关闭图A装置中的止水夹a后,从长颈漏斗向试管中注入一定量的水,静置后如图所示.试判断:A装置是否漏气?(填“漏气”、“不漏气”或“不能确定”)________
(2)关闭图B装置中的止水夹a后,开启活塞b,水不断往下滴,直至全部流入烧瓶.试判断:B装置是否漏气?(填“漏气”、“不漏气”或“不能确定”)________,判断理由________________________________
查看答案和解析>>
科目: 来源:北京市海淀区2009届高三年级第一学期期中练习化学试题 题型:058
测定中和热的实验装置如图所示.

(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3 kJ/mol):________.
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表.
①请填写下表中的空白:

②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃).则中和热ΔH=________(取小数点后一位).
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)________.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目: 来源:北京市海淀区2009届高三年级第一学期期中练习化学试题 题型:058
某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定.
配制0.50 mol/L NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体________g.
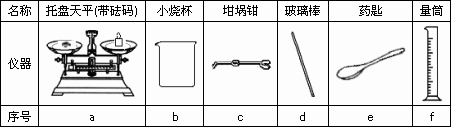
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):________.
查看答案和解析>>
科目: 来源:北京市海淀区2009届高三年级第一学期期中练习化学试题 题型:058
某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去.
(1)写出实验①中发生反应的离子方程式________.
(2)实验②中化学反应转移电子的物质的量是________.
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是________.
查看答案和解析>>
科目: 来源:深圳外国语学校2008届高三年级第二次质量检测化学试卷 题型:058
实验室里有如下仪器和药品,请设计如下实验的操作步骤要点“○”可不填满),并指出可能发生的实验现象.
仪器或用品:①试管 ②烧杯 ③玻璃片 ④石棉网 ⑤滤纸 ⑥火柴 ⑦镊子 ⑧酒精灯 ⑨药匙 ⑩集气瓶
药品:①金属钠(在煤油中) ②AlCl3溶液 ③蒸馏水 ④细沙

查看答案和解析>>
科目: 来源:重庆一中2008届高三年级第一次月考化学试卷 题型:058
某含有少量FeCl2杂质的FeCl3样品,现要测定其中铁元素的含量,实验步骤如下:
①准确称量m g样品;
②向样品中加入10 mL 5 mol·L-1的盐酸,再加入蒸馏水,配制成250 mL溶液;
③量取25 mL操作②中配得的溶液,加入3 mL溴水,加热使之完全反应;
④趁热迅速加入质量分数为10%的氨水至过量,充分搅拌,使之完全沉淀;
⑤过滤,将沉淀洗涤后反复灼烧、冷却、称量至恒重.
请根据上面的叙述回答:
(1)溶解样品时要加入盐酸,其目的是________
(2)配制250 mL溶液时,除需玻璃棒、烧杯外,还须用到的玻璃仪器是________
(3)加入溴水时发生反应的离子方程式是:________
(4)若坩埚质量为W1g,坩锅与灼烧后固体的总质量是W2g,则样品中铁元素的质量分数是________
查看答案和解析>>
科目: 来源:浙江杭州学军中学2007-2008高三第一次月考化学试卷 题型:058
某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO2-、MnO4-、CO32-、SO42-中的若干种组成.取该溶液进行如下实验:
(A)取试液适量,加入过量稀盐酸,有气体生成,得到溶液甲;
(B)向溶液甲中再加入过量碳酸氢铵溶液,有气体生成,析出白色沉淀乙,得到溶液丙
(C)向溶液丙中加入过量Ba(OH)2溶液,有气体生成,析出白色沉淀丁.
根据上述实验回答下列问题:
(1)溶液中一定不存在的离子是________.(全对才给分)
(2)一定存在的离子是________.(全对才给分)
(3)生成沉淀乙的离子反应方程式是________.
(4)写出步骤(C)中一定会发生反应的离子方程式________.
查看答案和解析>>
科目: 来源:汕头市六都中学高三级2007-2008化学模拟试卷 题型:058
实验室有一份混有少量碳酸钙杂质的碳酸钡样品.分离并提纯碳酸钡的实验步骤如下,请根据要求填空(下图为Ba(OH)2和Ca(OH)2的溶解度曲线):

(1)高温灼烧碳酸钡和碳酸钙的混合物,直至分解分解.所需仪器除坩埚、泥三角、玻璃棒、三脚架外还有________;
(2)将灼烧后的固体混合物置于80℃的热水中,制成氢氧化钡的热饱和溶液.为减少Ba(OH)2的损失并除去不溶物应进行的操作是________;
(3)将“(2)”中滤液________并过滤,得到的Ba(OH)2固体溶于水制成溶液.
(4)向制得的Ba(OH)2溶液中滴加________(填一种试剂名称),再通入二氧化 碳.当观察到________时,即可停止通二氧化碳.
(5)滤出碳酸钡沉淀,经洗涤、干燥后即得到纯净的碳酸钡.
查看答案和解析>>
科目: 来源:深圳外国语学校2008届高三年级第二次质量检测化学试题 题型:058
实验室有甲、乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是碳酸钠溶液.为确定甲、乙两瓶溶液的成分及其物质的量浓度,现操作如下:
①量取25.00 mL甲溶液,向其中缓慢滴加乙溶液15.00 mL,共收集到二氧化碳气体224 mL.
②另取15.00 mL乙溶液,向其中缓慢滴加甲溶液25.00 mL,共收集到二氧化碳气体112 mL.
上述气体体积均已换算为标准状况,则根据上述操述及实验数据填空:
(1)写出上述过程所涉及反应的离子方程式________;
(2)甲是________,甲溶液的物质的量浓度为________,乙溶液的物质的量浓度为________;(二氧化碳在溶液中的少量溶解忽略不计)
(3)将n mL的甲溶液与等体积的乙溶液按各种可能的方式混合,产生的气体体积为V mL(标准状况),则V的取值范围为________.
查看答案和解析>>
科目: 来源:深圳外国语学校2008届高三年级第二次质量检测化学试题 题型:058
实验原理,回答下列问题:
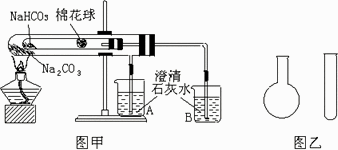
实验一:如图甲,小试管内塞有沾有无水硫酸铜粉末的棉花球.
(1)从点燃酒精灯开始,试管及烧杯A、B中能观察到的现象有________.
(2)整个实验结束时,在操作上需要特别注意的问题是________.
(3)通过该实验可以得出的结论是________.
实验二:在氨气的喷泉实验中,将圆底烧瓶集满氨气的操作很麻烦.请设计一个简单的操作方法,只用一支试管(如图乙),选用下列药品:A.氯化铵固体,B.氢氧化钠固体,C.浓氨水,D.浓硫酸,E.湿润的红色石蕊试纸,采用“套管法”在圆底烧瓶中集满喷泉实验的氨气.
(4)所用的试剂为________.
(5)请简述所设计的操作及判定集满氨气的现象:________.
(6)将上述两个实验与普通实验相比较,“套管实验”明显具备的优点是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com