
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-铁铜及其化合物(1) 题型:058
已知铜氨溶液中存在如下平衡:[Cu(NH3)]42+![]() Cu2++4NH3.
Cu2++4NH3.
某一混合液含有Ag+、Fe3+和Al3+,可以下列流程图加以分离和鉴定.
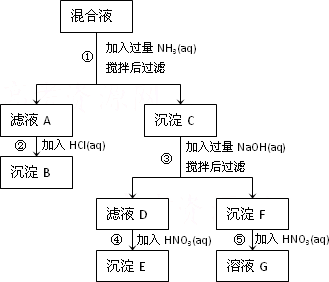
(1)写出滤液A中主要的阳离子的化学式________.
(2)解释步骤②中生成沉淀B的原因________.
(3)写出步骤③中发生反应的离子方程式________.
(4)溶液G中的金属离子的鉴定方法________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-铁铜及其化合物(1) 题型:058
已知当溶液的pH在10左右时,铝元素主要以Al(OH)3形式存在.如果饮用水中含有一定浓度的NO3-将对人类健康产生危害,NO3-能氧化人体血红蛋白中的Fe(Ⅱ),使其失去携氧功能;NO3-还能被水中还原性物质还原成具有强烈致癌作用的NO2-.为此世界卫生组织规定饮用水中NO3-含量(以N计)必须小于10 mg/L.为了降低饮用水中NO3-的浓度,某研究人员提出以下3种方案:
a、微碱性条件下用Fe2+还原,还原产物为NH3.
b、pH=10.25时,用铝粉还原,NO3-的还原产物主要为N2.
c、在催化剂作用下用氢气还原,还原产物主要为N2.
(1)请写出a方案的相关反应的离子方程式:________.
(2)b方案中最好用________调节pH.
A.NaOH B.CaO C.NH3·H2O
理由是_______________.
(3)与a、b方案相比,c方案的优点是:________
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-碳硅及其化合物 题型:058
已知SiO2、SO2、CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性(提示:2Mg+CO2![]() 2MgO+C)
2MgO+C)
Ⅰ、用如图所示的装置进行Mg和SO2的实验:
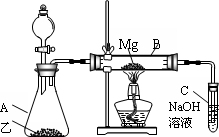
(1)选择制取SO2的合适试剂________.
①10%的H2SO4溶液;
②80%的H2SO4溶液;
③Na2SO3固体;
④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式:________________
(3)你认为该装置是否有不足之处?________,如果有,请列出两点:__________.
Ⅱ、某研究性学习小组进行了“实验室制Si”的研究,它们以课本为基础,查阅资料后得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si;
②Mg在高温的条件下即可与SiO2反应;
③金属硅化物与稀H2SO4反应生成硫酸盐和SiH4;
④Si和SiO2均不与稀H2SO4反应;
⑤SiH4在空气中自燃.
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀H2SO4溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀H2SO4溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”.
(4)该小组“实验室制“Si”的化学方程式是________
(5)你估计“用稀H2SO4溶解固体产物时,发现有爆鸣声和火花”的原因是________
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验探究(1) 题型:058
铜及其化合物一般都具有特征的颜色,例如Cu、Cu2O呈红色,CuO呈黑色,CuSO4·5H2O呈蓝色等.研究性学习小组甲为检测实验室的Cu2O试样中是否含有Cu进行了认真的探究.
Ⅰ.查阅资料:①Cu2O属于碱性氧化物;②在空气中灼烧Cu2O生成CuO;③Cu2O在酸性条件下能发生自身氧化还原反应(Cu2O+2H+=Cu+Cu2++H2O).
Ⅱ.设计实验方案:
方案1:取该红色试样溶于足量的稀硝酸中,观察溶液颜色变化
方案2:取该红色试样溶于足量的稀硫酸中,观察是否有残渣
方案3:称得干燥坩埚的质量为a g,取红色试样置于坩埚中称得总质量为b g,在空气中充分灼烧至完全变黑,并在干燥器中冷却,再称量.如此反复多次直到质量不变,称得最后质量为c g.分析数据,作出合理判断.
(1)请你评价方案1和方案2.如果你认为该方案合理,请简述其工作原理;如果你认为该方案不合理,请简述原因._______
(2)方案3中,如果a、b、c的关系符合c=________可确认红色粉末是Cu2O.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验探究(1) 题型:058
已知SiO2、SO2、CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定的相似性(提示:2Mg+CO2![]() 2MgO+C)
2MgO+C)
Ⅰ、用如图所示的装置进行Mg和SO2的实验:
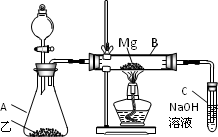
(1)选择制取SO2的合适试剂________.
①10%的H2SO4溶液;
②80%的H2SO4溶液;
③Na2SO3固体;
④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式:________
(3)你认为该装置是否有不足之处?________,如果有,请列出两点:__________.
Ⅱ、某研究性学习小组进行了“实验室制Si”的研究,它们以课本为基础,查阅资料后得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si;
②Mg在高温的条件下即可与SiO2反应;
③金属硅化物与稀H2SO4反应生成硫酸盐和SiH4;
④Si和SiO2均不与稀H2SO4反应;
⑤SiH4在空气中自燃.
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀H2SO4溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀H2SO4溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”.
(4)该小组“实验室制“Si”的化学方程式是________
(5)你估计“用稀H2SO4溶解固体产物时,发现有爆鸣声和火花”的原因是________
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验探究(1) 题型:058
某同学利用铁与水蒸气反应后的固体物质进行了如下实验:

(1)固体溶于稀盐酸的化学方程式为________.
(2)试剂1的化学式是________.
(3)加入新制氯水后溶液红色加深的原因是(用离子方程式表示):________
(4)某同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究.
①提出假设:
假设1:溶液中的+3价铁被氧化为更高的价态;
假设2:________;
②设计方案:
为了对你所提出的假设2进行验证,你设计的实验方案是________________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验探究(1) 题型:058
N2在化工生产、农业、医疗、航天航空等诸多领域用途广泛.某化学兴趣小组同学为探究在实验室制备较为纯净N2的方法,进行了认真的准备.请你参与交流与讨论.
[查阅资料]N2的制法有下列三种方案:
方案1:加热条件下,以NH3还原CuO可制得N2,同时获得活性铜粉.
方案2:加热NaNO2和NH4Cl的浓溶液制得N2.
方案3:将空气缓缓通过灼热的铜粉获得较纯的N2.
[实验准备]以实验室常见仪器(药品)等设计的部分装置如下图(有的夹持和加热仪器未画出).
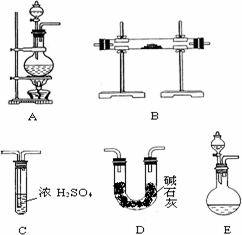
[分析交流]
(1)若按方案1制得干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料,整套制气装置按气流从左到右的顺序连接的顺序是(填写序号,下同)________.
获得N2的反应原理是(写反应方程式)________.
(2)若以排水法收集N2,其中会混入水蒸气.但也不宜用排空气法,其原因是
________.你提出的收集方法是________.
(3)若以方案2制得N2,应选择的发生装置是________.为保证实验安全顺利进行,操作时应________(填写两点).
(4)上述三个方案中,制得的N2纯度最差的是________.在N2纯度要求不甚严格的情况下,有人建议将方案1和方案3结合使用,你认为其优点是________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验探究(1) 题型:058
现有含NaCl、Na2SO4、NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、NO3-的相互分离.相应的实验过程可用下列流程图表示:

(1)写出上述实验过程中所用试剂的名称:
试剂1________ 试剂2________ 试剂4________
(2)恰当地控制试剂4的加入量的方法是________
(3)加入过量试剂3的目的是________
(4)在加入试剂4后,获得固体D的实验操作④是________(填操作名称)
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验探究(1) 题型:058
某校化学兴趣小组的同学欲测定某种品牌味精中食盐的含量.下面是该小组所做的有关实验步骤:
①称取某牌袋装味精样品10.0 g放入烧杯中,并加适量蒸馏水溶解;
②
③
④用蒸馏水洗涤沉淀2-3次;
⑤将沉淀干燥、称量,测得固体质量4.9 g
根据上述实验步骤回答下列问题:
(1)补齐所缺少的实验步骤:②________,③________;
(2)实验步骤③所用的玻璃仪器有________;
(3)检验沉淀是否完全的方法是:________;
(4)干燥沉淀应采取的方法是________.
(5)若味精标签上标注:“谷氨酸钠含量≥80.0%,NaCl含量≤20.0%,则此样品是否合格?”________(填“合格”,“不合格”)
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-实验探究(1) 题型:058
某化学兴趣小组利用实验室提供的下列试剂:铁粉、0.1 mol·L-1 FeCl3溶液、0.1 mol·L-1 FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+、Fe3+的氧化性、还原性,并对实验结果加于应用.
(1)根据氧化还原的有关原理,兴趣小组对Fe2+、Fe3+的氧化性、还原性提出了如下2种假设:
假设一:Fe2+既有还原性又有氧化性;
假设二:Fe3+具有氧化性;
(2)设计实验方案,进行实验并描述实验现象,完成下列表格.

(3)该兴趣小组为说明“Fe2+具有氧化性”,提出了一个反应事实:FeCl2+Zn=ZnCl2+Fe该反应的离子方程式为:________
(4)根据Fe3+的性质,该兴趣小组利用FeCl3溶液腐蚀铜箔制造印刷线路板,反应的离子方程式是:________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com