
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-氧化还原反应 题型:058
北京市场销售的某种食用精制盐包装袋上有如下说明:

(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处):
________KIO3+________KI+________H2SO4=________K2SO4+________I2+________H2O
(2)上述反应生成的I2可用四氯化碳检验.向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是________.
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体.
以上设计中遗漏的操作及上述步骤中的位置是________.
(3)已知:I2+2S2O![]() =2I-+S4O
=2I-+S4O![]() .某学生测定食用精制盐的碘含量,其步骤为:
.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol/L的Na2S2O3溶液10.0 mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是________.
②b中反应所产生的I2的物质的量是________mol.
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)________mg/kg.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-氧化还原反应 题型:058
| |||||||||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-物质的量 题型:058
在现代生活中,人们越来越注意微量元素的摄入.碘元素对人体健康有着至关重要的作用.为预防碘缺乏病,我国卫生部规定每千克食盐中应含有40~50 mg KIO3.下表是某超市出售的加碘精制盐的有关说明:

某同学设计实验验证此食盐中是否含碘和检查该食盐是否为合格产品.
(1)完成下列实验报告:

(2)加碘食盐的包装袋上标有食用方法:待食品熟后加入.其原因是:________
(3)该同学取该食盐样品100.0 g完全溶解于水中,然后加入用盐酸酸化的淀粉-KI溶液,结果溶液呈蓝色,则反应的离子方程式为________.为进一步确证样品是否为合格产品,该同学又用0.010 mol·L-1的Na2S2O3溶液滴定,当用去12.00 mL时蓝色刚好褪去(反应方程式为I2+2S2O![]() =2I-+S4O
=2I-+S4O![]() ),通过计算该加碘食盐中KIO3的含量为________mg/kg.由此可判定该食盐为________(填“合格”或“不合格”)产品.
),通过计算该加碘食盐中KIO3的含量为________mg/kg.由此可判定该食盐为________(填“合格”或“不合格”)产品.
(4)KIO3可用电解的方法制得,原理是:以石墨为阳极,以不锈钢为阴极,在一定温度和电流下电解KI溶液.总反应方程式为KI+3H2O![]() KIO3+3H2↑,则阳极的电极反应式为________;阴极附近pH值________(填“增大”、“减小”、“不变”).
KIO3+3H2↑,则阳极的电极反应式为________;阴极附近pH值________(填“增大”、“减小”、“不变”).
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-无机推断 题型:058
某固体混合物可能含Al、(NH4)2SO4、MgCl2、A1Cl3、FeCl3中的一种或几种,现对该混合物作如下实验,所得现象和有关数据如图(气体体积已换算成标况下的体积):

请回答:
(1)混合物中是否存在FeCl2________(填“是”或“否”);
(2)混合物中是否存在(NH4)2SO4________(填“是”或“否”),你的判断依据是________.
(3)写出反应⑤的离子反应方程式;________.
(4)请根据图中数据分析,原固体混合物中一定含有的物质为________(写化学式),不写计算过程.
(5)把AlCl3溶液加热浓缩蒸干,不能得到较纯的A1Cl3晶体,请你设计一个可行的简易实验从溶液中得到较纯的AlCl3结晶:________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-无机推断 题型:058
A、B、C、D、E五种可溶性化合物,分别由阳离子Fe3+、Ba2+、Al3+、Na+、Ag+和阴离子NO3-、OH-、SO42-、Cl-、CO32-中的各一种组成(离子不重复).现做如下实验:
①A和E的溶液显碱性,0.1 mol/L A溶液的pH小于13;
②在B的溶液中逐滴加入氨水有白色沉淀生成,继续加氨水至过量,沉淀消失;
③在C的溶液中加入铁粉,溶液的质量增加;
④在D的溶液中加入过量的Ba(OH)2溶液,没有沉淀.
(1)根据以上事实推断A~E的化学式:
A________、B________、C________、D________、E________
(2)写出②、③、④的离子方程式:
②________________________________
③________________________________
④________________________________
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-无机推断 题型:058
已知某工业废水中含有大量CuSO4,少量的Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质.
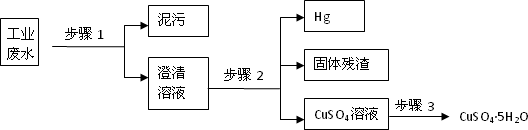
(1)步骤1的主要操作是________,需用到的玻璃仪器除烧杯外有________.
(2)步骤2中需加入某种试剂后再将混合物分离,该试剂是(填化学式)________,固体残渣的成分是(填化学式)________.
(3)步骤3中涉及的操作是:蒸发浓缩、________、过滤、烘干.
(4)步骤2应该在通风橱中进行,原因是________________
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-无机化学综合 题型:058
短周期元素的单质X、Y、Z在通常状况下均为气态,并有下列转化关系(反应条件略去):
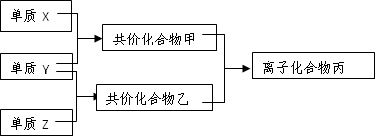
已知:a.常见双原子单质分子中,X分子含共价键最多,键能很大.b.甲分子中含10个电子,乙分子含有18个电子.
(1)X的电子式是________.
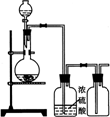
(2)实验室可用下图所示装置(缺少收集装置,夹持固定装置略去)制备并收集甲.

①在图中方框内绘出用烧瓶收集甲的仪器装置简图.
②试管中的试剂是(填写化学式)________.
③烧杯中溶液由无色变为红色,其原因是(用电离方程式表示)________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-无机化学综合 题型:058
A、B、C、D均为中学化学常见的物质,其组成元素均为主族元素.它们间的反应关系如图所示.
(1)若A为金属钠,B为饱和Ca(OH)2溶液,则白色沉淀D为________(写化学式)
(2)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则A与B反应(可加热)的离子方程式为:____________________________.
(3)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液,A的相对分子质量与D相同.向一定量的B溶液中逐渐加入固体粉末A,当A与B以物质的量之比3∶1反应时,生成的D的量最多.推知A的化学式为________,B的化学式为________,D与NaOH溶液反应的离子方程式是________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-无机化学综合 题型:058
A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去).
试回答:
(1)若X的强氧化性单质,则A不可能是________.(填选项)
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为________;C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示)________,检验此C溶液中金属元素价态的操作方法是________.
(3)若A、B、C为含有金属元素的化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式可能为________,X的化学式可能为(写出不同类物质)________或________,反应①的离子方程式为________或________.
查看答案和解析>>
科目: 来源:广东省2009届高三化学各地名校月考试题汇编-铁铜及其化合物(2) 题型:058
某同学利用铁与水蒸气反应后的固体物质进行了如下实验:

(1)固体溶于稀盐酸的化学方程式为________.
(2)试剂1的化学式是________.
(3)加入新制氯水后溶液红色加深的原因是(用离子方程式表示)____________;
(4)某同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究.
①提出假设:
假设1:溶液中的+3价铁被氧化为更高的价态;
假设2:________;
②设计方案:
为了对你所提出的假设2进行验证,实验方案是________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com