
科目: 来源:2009年高考化学(广东A卷) 题型:058
甲酸甲酯水解反应方程式为:
![]()
某小组通过试验研究该反应
(反应过程中体积变化忽略不计).反应体系中各组分的起始量如下表:甲酸甲酯转化率在温度
T1下随反应时间(t)的变化如下图: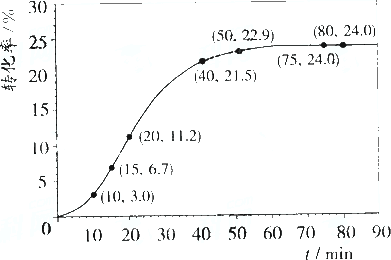
(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:
![]()
请计算
15-20 min范围内甲酸甲酯的减少量为________mol,甲酸甲酯的平均反应速率为________mol·min-1(不要求写出计算过程).(2)依据以上数据,写出该反应的反应速率在不同阶段的变化规律及其原因:________.
(3)上述反应的平衡常数表达式为:![]() ,则该反应在温度T1下的K值为________.
,则该反应在温度T1下的K值为________.
(4)其他条件不变,仅改变温度为T2(T2大于T1),在答题卡框图中画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图.
查看答案和解析>>
科目: 来源:2009年高考化学(广东A卷) 题型:058
某试验小组利用如下装置
(部分固定装置略)制备氧化钙(Ca3N2),并探究其实验式.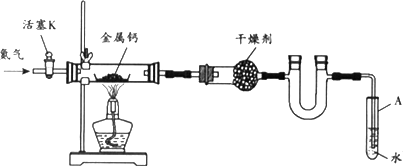
(1)按图连接好实验装置.检查装置的气密性,方法是________.
(2)反映过程中末端导管必须插入试管A的水中,目的是________.
(3)制备氮化钙的操作步骤是:①打开活塞K并通入N2;②点燃酒精灯,进行反应;③反应结束后,________;④拆除装置,取出产物.
(4)数据记录如下:
①计算得到实验式
Ca2N2,其中x=________.②若通入的
N2中混有少量O2,请比较x与3的大小,并给出判断依据:________.查看答案和解析>>
科目: 来源:2009届山东诸城一中高三年级阶段性评估练习、化学试题 题型:058
饱和氯水与石灰石的反应是制取较浓的HClO溶液方法之一.某同学运用这一方法,尝试制取HC1O溶液并进行了如下定性实验:
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水,充分反应,有少量气泡产生,溶液的黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验;
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量气泡;
第三份加热,看到溶液变浑浊且有大量无色气体产生;
经检测,上述实验中产生的无色气体均为CO2气体.
(1)试解释可以在饱和氯水中加入石灰石制备HClO的原因________.
(2)写出步骤③中第一份及第二份滤液发生反应的离子方程式:
第一份___________________.
第二份____________________.
(3)试根据所学知识推测,在②的滤液中含有的溶质,除了溶解的极少量氯气外,还含有的其它溶质为(写化学式)________.
查看答案和解析>>
科目: 来源:2009届9月北京明光中学高三教学检测、化学试卷 题型:058
某学生用实验室常见的酸、碱、盐和金属为反应物,并利用一个底部有小孔的试管和一个广口瓶组装成如图所示的替代简易气体发生器的即开即停装置,该装置中装有铜丝网隔板,利用该装置可制取哪些气体________.若将铜丝网隔板改为铁丝网隔板,则该装置可用于制取何种气体________.写出反应的离子方程式________.
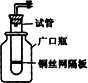
查看答案和解析>>
科目: 来源:2008届宁夏银川一中高三年级第六次月考测试、理科综合试卷化学部分 题型:058
指出在使用下列仪器(已经洗涤干净)或用品时的第一步操作:
①石蕊试纸(检验气体):________.
②容量瓶:___________________.
③托盘天平___________________.
查看答案和解析>>
科目: 来源:2008-2009学年度泰安市宁阳一中第一学期高三期中考试、化学试卷 题型:058
实验室常用的几种气体发生装置如下图A、B、C所示:
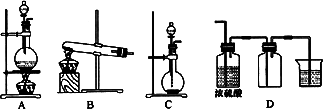
(1)实验室可以用B或C装置制取氨气,如果用C装置,通常使用的药品是________.检查C装置气密性是否良好的操作方法是________.
(2)气体的性质是气体收集方法选择的主要依据.下列性质与收集方法无关的是________(填序号,下同).
①密度
②颜色
③溶解性
④热稳定性
⑤与氧气反应
(3)若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的________.
①CO2
②NO
③Cl2
④H2
查看答案和解析>>
科目: 来源:2008-2009学年度上海交通大学附中第一学期高三摸底考试、化学试卷 题型:058
实验室检验下列物质,在以下可选用的实验方法中选出合适的按实验顺序填在下表中:(实验方法或试剂如需重复使用应多次填入)

可选用的实验方法:
①加入硝酸银溶液 ②通过饱和NaHCO3溶液 ③加入稀硝酸 ④加入浓硫酸 ⑤通过品红溶液 ⑥通过石灰水 ⑦通过酸性KMnO4溶液 ⑧加入足量NaOH溶液 ⑨滴加盐酸 ⑩过滤 ![]() 加热
加热
查看答案和解析>>
科目: 来源:2008-2009学年度山东省聊城一中第一学期高三期中考试、化学试卷 题型:058
某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体(七水合硫酸亚铁)和胆矾晶体,以探索工业废料的再利用.其实验方案如下:
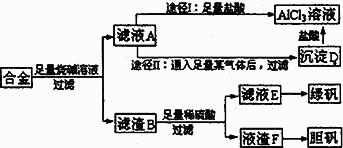
试回答下列问题:
(1)写出合金溶于足量烧碱溶液时相关反应的离子方程式________;写出途径I中相关反应的离子方程式________.
(2)由滤液A制AlCl3溶液有途径I和途径II两种,你认为哪种途径比较合理,说明理由________.
(3)按环保要求,写出用滤渣F制备硫酸铜溶液的各步反应的化学方程式
_________________
查看答案和解析>>
科目: 来源:2008-2009学年度济宁市育才中学高三阶段性测试、化学试卷 题型:058
已知当溶液的pH在10左右时,铝元素主要以Al(OH)3形式存在.如果饮用水中含有一定浓度的NO3-将对人类健康产生危害,NO3-能氧化人体血红蛋白中的Fe(Ⅱ),使其失去携氧功能;NO3-还能被水中还原性物质还原成具有强烈致癌作用的NO2-.为此世界卫生组织规定饮用水中NO3-含量(以N计)必须小于10 mg/L.为了降低饮用水中NO3-的浓度,某研究人员提出以下3种方案:
a.微碱性条件下用Fe2+还原,还原产物为NH3.
b.pH=10.25时,用铝粉还原,NO3-的还原产物主要为N2.
c.在催化剂作用下用氢气还原,还原产物主要为N2.
(1)请写出a方案的相关反应的离子方程式:________.
(2)b方案中最好用________调节pH.理由是________.
A.NaOH
B.CaO
C.NH3·H2O
(3)与b方案相比,c方案的优点是:________
查看答案和解析>>
科目: 来源:2007-2008学年上海市嘉定一中第一学期高三年级测试(二)、化学试题 题型:058
①指出在使用下列仪器(已净)或用品的第一步操作:
②下面是中学化学实验常见的几种定量仪器:
A.量筒
B.容量瓶
C.滴定管
D.托盘天平,其中
(填代号)
③利用图所示装置收集以下8种气体.(图中烧瓶的位置不得变化)

①H2 ②Cl2 ③CH4 ④HCl ⑤NH3 ⑥NO ⑦H2S ⑧SO2
(答案均填序号)
(1)若烧瓶是干燥的,则由B口进气可收集的气体有________
(2)若烧瓶是干燥的,则由A口进气可收集的气体有________
(3)若烧瓶充满水,可收集的气体有________;此时气体由________口进入.
(4)若烧瓶内装入浓H2SO4进行气体干燥,则可用此装置干燥的气体有________,这时气体由________口进入.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com