
科目: 来源:上海市崇明县2011届高三上学期期末考试化学试题 题型:058
用沉淀法测定NaHCO3和K2CO3混合物的组成,实验过程是每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的Ba(OH)2溶液,充分反应,实验记录见下表:

回答下列问题:
(1)第2次实验中产生的沉淀质量是________.
(2)样品中NaHCO3和K2CO3的物质的量之比是________.
(3)室温下取第3组实验所得溶液体积的1/10,加水配成500 mL溶液,稀释以后溶液的pH值为________(写出计算过程)
查看答案和解析>>
科目: 来源:上海市崇明县2011届高三上学期期末考试化学试题 题型:058
化学实验的微型化可有效减少污染,实现化学实验的绿色要求.如图所示,某学生在一块衬白纸的玻璃片的不同位置分别加一滴含酚酞的NaOH溶液(a)、浓度为0.1 mol/L KI淀粉溶液(b)、FeCl2(含KSCN)溶液(c),并在e处放置少量KMnO4晶体,向KMnO4晶体上滴加几滴浓盐酸后立即用表面皿盖好,形成一个气室.

已知反应中有关物质的转化过程为:
KMnO4→MnCl2;
HCl→Cl2
(1)e处的化学反应方程式为________该反应中氧化剂与还原剂的物质的量之比为________,电子转移的数目为________.
(2)b处的实验现象为________________,c处的实验现象为________________.
(3)a处的反应方程式为________.
(4)通过该实验可比较Cl2、FeCl3、KMnO4三种物质氧化性由强到弱的顺序是________.
查看答案和解析>>
科目: 来源:上海市嘉定区2011届高三上学期第一次质量调研化学试题 题型:058
现用如图所示的装置制取较多量的饱和氯水并测定饱和氯水的pH.
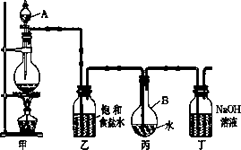
回答有关问题:
(1)写出有关化学方程式.
装置甲:________;
装置丁:________.
(2)证明氯水已饱和的现象是________________.
(3)制取结束时,装置丙的液体中含有的微粒是______________(用微粒符号表示);
(4)若撤去装置乙,直接将装置甲和丙相连.这样做对实验测定结果的影响是:________________.
测定饱和氯水的pH方法是________________.
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:058
研究性学习小组的同学为了了解Cu及其化合物的性质,提出以下问题;
①Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②Fe的+2价化合物的稳定性比+3价化合物的稳定性小,Cu的+1价化合物的稳定性也比+2价化合物的稳定性小吗?
③CuO能被H2、CO等还原,也能被NH3还原吗?
(1)解决问题①需要用到的药品有CuSO4溶液、________、________(填字母).
A.A1Cl3溶液
B.NaOH溶液
C.稀H2SO4
D.H2O2溶液
假若Cu(OH)2具有两性,应该看到的实验现象是________.
(2)为了比较Cu的+1价化合物和+2价化合物的稳定性,他们取98 g Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变成红色粉末X.冷却后称量,X的质量为72 g.向X中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在.据此可推得,X的化学式为________,可以得出的结论是________.
(3)为解决问题③,设计了如下的实验装置(夹持及尾气处理装置未画出):
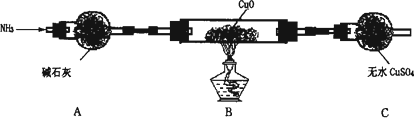
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体.装置A的作用是________,B中发生反应的化学方程式为________.
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:058
pC类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值.如某溶液溶质的浓度为:1×10-3 mol/L,则该溶液中该溶质的pC=-lg1×10-3=3.已知H2CO3溶液中存在的化学平衡为:CO2+H2O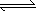 H2CO3
H2CO3 H++HCO3-
H++HCO3- 2H++CO32-.下图为H2CO3溶液的pC-pH图.请回答下列问题:
2H++CO32-.下图为H2CO3溶液的pC-pH图.请回答下列问题:
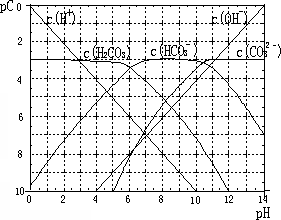
(1)在pH=0~4时,H2CO3溶液中主要存在的离子为:________;在pH=12时,H2CO3溶液中主要存在的含碳阴离子为:________;
(2)pH<5时,溶液中H2CO3的pC值总是约等于3的原因是________;
(3)一定浓度的NaHCO3和Na2CO3混合溶液是一种“缓冲溶液”,在这种溶液中加入少量的强酸或强碱,溶液的pH变化不大,其原因是________.
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:058
已知A为常见金属,X、Y为常见非金属,X、E、F、G常温下为气体,C为液体,B是一种盐,受热极易分解,在工农业生产中用途较广(如被用作某些电池的电解质).现用A与石墨作电极,B的浓溶液作电解质,构成原电池.有关物质之间的转化关系如下图:(注意:其中有些反应的条件及部分生成物被略去)

请填写下列空白:
(1)反应④为A在某种气体中燃烧,生成单质Y和A的氧化物,其反应方程式为________.
(2)从D溶液制备D的无水晶体的“操作a”为________.
(3)反应⑤的化学方程式为________.
(4)原电池反应①中正极的电极反应式为________.
查看答案和解析>>
科目: 来源:江西省南昌三中2011届高三第六次月考化学试题 题型:058
有一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl-、I-、NO3-、CO32-、SO42-中的几种.取该溶液进行以下实验:
(1)用pH试纸检验,表明溶液呈强酸性.
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡CCl4层呈紫红色.
(3)另取部分溶液,逐渐向其中加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,均无沉淀产生.取部分碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝.
(4)另取部分上述碱性溶液,向其中加入Na2CO3溶液,有白色沉淀生成.
(5)根据上述实验事实确定:①该溶液中肯定存在的离子是________;
②肯定不存在的离子是________.
③还不能确定是否存在的离子是________.
查看答案和解析>>
科目: 来源:江苏省苏北四市2011届高三第二次调研考试化学试题 题型:058
硫酸锌是一种重要的工业原料.在实验室从粗锌(含有少量的铅)与稀硫酸反应后的废液中提取硫酸锌的主要操作步骤如下:
步骤1:将废液过滤,调节滤液的pH约为2,过滤,将滤液加热浓缩,制得较高温度下的饱和溶液,冷却结晶得到粗制晶体.
步骤2:①在烧杯中用蒸馏水溶解步骤1得到的晶体,滴加少量稀硫酸,水浴加热至晶体全部溶解.②停止加热,让其自然冷却、结晶.③抽滤,用少量无水乙醇洗涤晶体l~2次,得精制晶体.
(1)废液中含有的不溶性杂质是________.
(2)步骤1中调节滤液pH约为2,可加入的物质是________.
(填字母)a.NH3·H2O
b.ZnO
c.ZnCO3
d.NaOH
(3)步骤1中对滤液加热浓缩时,当________时,停止加热.
(4)步骤2中滴加少量稀硫酸的目的是________.
(5)抽滤装置如图所示,仪器B的名称是________.仪器C的作用是________.
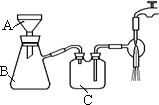
(6)用少量无水乙醇洗涤晶体的目的是________.
查看答案和解析>>
科目: 来源:江苏省苏北四市2011届高三第二次调研考试化学试题 题型:058
氧元素与多种元素具有亲和力,所形成化合物的种类很多.
(1)氮、氧、氟元素的第一电离能从大到小的顺序为________.氧元素与氟元素能形成OF2分子,该分子的空间构型为________.
(2)根据等电子原理,在NO2+离子中氮原子轨道杂化类型是________;1 mol O22+中含有的π键数目为________.
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成
Cr2O3、CrO3、CrO5等.Cr3+基态核外电子排布式为________.(4)钙在氧气中燃烧时得到一种钙的氧化物晶体,其晶体结构如图所示,则该钙的氧化物的化学式为________.
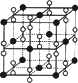
查看答案和解析>>
科目: 来源:江苏省苏北四市2011届高三第二次调研考试化学试题 题型:058
用广谱高效的二氧化氯(ClO2)替代液氯进行消毒,可避免产生对人体健康有害的有机氯代物.
(1)工业上,ClO2常用NaClO3和Na2SO3溶液混合并加硫酸酸化后反应制得,在该反应中NaClO3和Na2SO3的物质的量之比为________.
(2)有效氯含量是含氯消毒剂的一个重要指标,有效氯含量的定义为:从HI中氧化出相同量的I2所需Cl2的质量与指定含氯消毒剂的质量之比,常用百分数表示.则ClO2的有效氯含量是________.
(3)化学小组的同学欲对用ClO2消毒过的自来水进行氯元素含量的测定(假定ClO2全部转化为Cl-),他们进行了如下实验:向30.00 mL水样中加几滴K2CrO4溶液作指示剂,用0.001000 mol·L-1 AgNO3溶液滴定,当有砖红色Ag2CrO4沉淀出现时,达滴定终点,此时用去AgNO3溶液12.12 mL.
①水样中Cl-的物质的量浓度是________.
②已知Ksp(AgCl)=1.78×10-10,Ksp(Ag2CrO4)=2.00×10-12.如在滴定终点时,测得溶液中CrO42-的浓度是5.000×10-3 mol·L-1.试计算此时溶液中Cl-的浓度是多少.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com