
科目: 来源:湖北省武汉市部分学校2011-2012学年高三新起点调研测试化学试题 题型:058
某研究性学习小组利用如图所示装置完成有关实验.
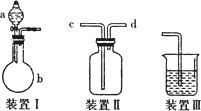
[实验一]快速制氨气
(1)用装置I快速制氨气,则装置I的a仪器中可加入浓氨水,b仪器中加入________.装置Ⅱ从________管口进气可作为氨气的收集装置.
[实验二]收集NO
(2)利用装置Ⅱ可收集NO,试简述操作方法:________.
[实验三]比较硫、碳、硅三种元素的非金属性强弱
(3)设计实验,完成下列表格(可以不填满,也可以再加行)

查看答案和解析>>
科目: 来源:新人教版2012届高三上学期单元测试(1)化学试题 新人教版 题型:058
电解法制碱的主要原料是饱和食盐水,由于粗盐水中含有泥沙、Ca2+、Mg2+、Fe3+、SO![]() 等杂质,不符合电解要求,因此必须经过精制.某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
等杂质,不符合电解要求,因此必须经过精制.某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
步骤1:取一定量的粗盐,置于烧杯中,加入足量的水,配成粗盐水;
步骤2:向粗盐水中加入除杂试剂,然后进行过滤,滤去不溶物,再向滤液中加入盐酸调节盐水的pH;
步骤3:将得到的溶液蒸发浓缩、冷却、结晶、过滤、烘干即得精盐;
请回答以下问题:
(1)上述实验中的过滤操作需要烧杯、________、________等玻璃仪器.
(2)步骤2中常用Na2CO3、NaOH、BaCl2作为除杂试剂,则加入除杂试剂的顺序为:
________.
(3)步骤2中,判断加入BaCl2已过量的方法是:________.
(4)步骤2中,若先用盐酸调节pH再过滤,将会对实验结果产生影响,其原因是________.
(5)为检验精盐纯度,需配制150 mL 0.2 mol/L NaCl(精盐)溶液,下图是该
同学转移溶液的示意图,图中的两处错误是:
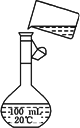
_________________________.
若在定容时仰视,则所配溶液的浓度________0.2 mol/L(填“大于”或“小于”);若定容不慎超过刻度线,应采用的处理方法是:________.
查看答案和解析>>
科目: 来源:新人教版2012届高三上学期单元测试(1)化学试题 新人教版 题型:058
实验室需要制备纯净的氯化钾.现有含少量KBr和K2SO4的氯化钾样品,
按照下图所示的实验方案进行提纯.
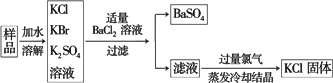
(1)检验加入BaCl2溶液后SO![]() 是否沉淀完全的操作为________;
是否沉淀完全的操作为________;
(2)若用硝酸钡来代替氯化钡,请判断是否可行,并说明理由:________;
(3)某同学认为该实验方案中加适量氯化钡溶液不容易控制,应加入过量氯化钡溶液他的思路如下,请写出方框内或横线①②③④⑤中溶质或沉淀(或物质)的化学式:________.
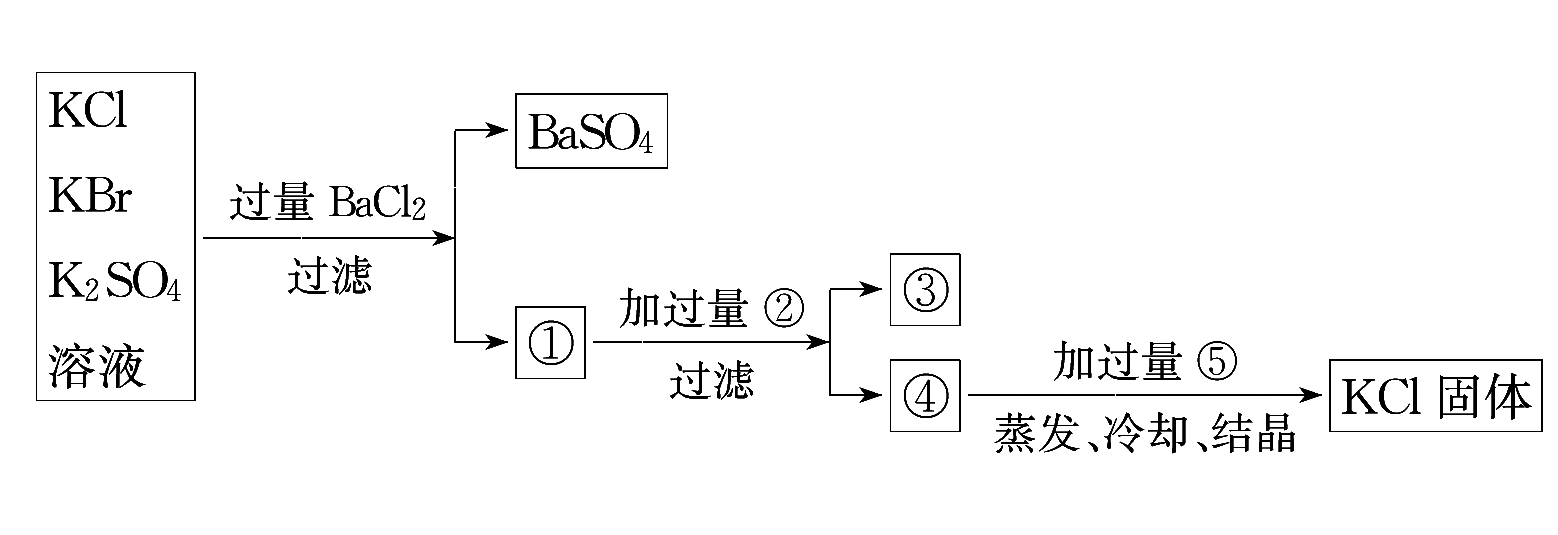
查看答案和解析>>
科目: 来源:大纲版2012届高三上学期单元测试(3)化学试题 题型:058
某种催化剂为铁的氧化物.化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色.一位同学由此得出该催化剂中铁元素价态为+3的结论.
(1)请指出该结论是否合理并说明理由
________.(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3 mol·L-1 H2SO4/3% H2O2、6 mol·L-1 HNO3/0.01 mol·L-1 KmnO4、NaOH稀溶液、0.1 mol·L-1 Kl、20% KSCN、蒸馏水.
①提出合理假设
假设1:________;假设2:________;假设3:________.
②设计实验方案证明你的假设
③实验过程
根据②的实验方案,进行实验.请在答题卡上按下表格式写出实验操作步骤、预期现象与结论.

查看答案和解析>>
科目: 来源:山东省兖州市2012届高三入学摸底考试化学试题 题型:058
某校学生利用以下装置验证氯气与氨气之间的反应(部分装置已略去).其中A、B分别为氯气和氨气的发生装置,C为纯净干燥的氯气与氨气反应的装置.
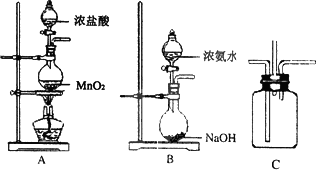
请回答下列问题:
(1)装置A中发生反应的离子方程式为________.
(2)装置B中浓氨水与NaOH固体混合可制取氨气,其原因是________.
(3)装置C中氯气和氨气相遇,有浓厚的白烟并在容器内壁凝结,同时生成一种可参与生态循环的无毒气体,该反应的化学方程式为________.
(4)将装置C中反应生成的固体溶于水,所得溶液中离子浓度由大到小的顺序为________.
查看答案和解析>>
科目: 来源:四川省成都外国语学校2012届高三8月月考化学试题 题型:058
如下图
,通电5 min后,电极5质量增加2.16 g,回答:
(1)电源:a是________极 ;A池中电极________上产生气体能使湿润KI淀粉试纸变蓝;B池中电极________上发生氧化反应,电解过程中pH________(填增大、减小或不变).
电池电极反应,电极1:________;电极4:________.
A池电池总反应________.
C池电池总反应________.
(2)如果B池中共收集到224 mL气体(标准状况),且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为________.
查看答案和解析>>
科目: 来源:四川省成都外国语学校2012届高三8月月考化学试题 题型:058
小明为验证NO2的氧化性和NO的还原性,设计了如下装置制取NO2和NO,并验证其性质,装置图如下:
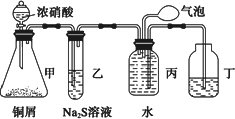
(1)写出甲中反应的离子方程式________,乙中的现象是________,可证明NO2的氧化性;在丙中鼓入空气后现象是________,可证明NO的还原性.
(2)实验前丙中充满水的作用是________.
(3)小华对小明的实验设计提出了质疑,他认为乙中的现象不足以证明NO2的氧化性,他的理由是________.
你认为怎样才能准确证明NO2的氧化性?(简要回答出原理和现象即可)________.
查看答案和解析>>
科目: 来源:四川省成都外国语学校2012届高三8月月考化学试题 题型:058
物质的转化关系如下图所示(有的反应可能在水溶液中进行).其中A为化合物,甲可由两种单质直接化合得到,乙为金属单质,G为酸,乙在G的浓溶液中发生钝化.
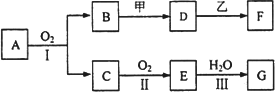
(1)若A为硫酸工业的重要原料,C能使品红试液褪色,D的水溶液中加入HNO3酸化的AgNO3 溶液有白色沉淀生成.则:
①工业上反应Ⅱ在________中进行(填设备名称),工业上反应Ⅲ用于吸收E的试剂是________.
②D的水溶液呈________性(填“酸”、“碱”或“中”).
③反应I的化学方程式是________.
(2)若甲为淡黄色固体,D、F的溶液均呈碱性,用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成.则
①甲的电子式是________.
②写出B和甲反应的化学方程式是________.
③若17 g A与O2反应生成气态的B和C时放出226.7 kJ热量,写出该反应的热化学方程式:________.
查看答案和解析>>
科目: 来源:四川省成都外国语学校2012届高三8月月考化学试题 题型:058
某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO![]() 、MnO
、MnO![]() 、CO
、CO![]() 、SO
、SO![]() 中的若干种组成,取该溶液进行如下实验:
中的若干种组成,取该溶液进行如下实验:
①取适量试液,加入过量盐酸,有气体生成,并得到溶液;
②在①所得溶液中再加入过量碳酸氢铵溶液,有气体生成;同时析出白色沉淀甲;
③在②所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出.
根据上述实验回答下列问题:
(1)溶液中一定不存在的离子是________;
(2)一定存在的离子是________;
(3)判断沉淀乙成分的方法是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com