
科目: 来源:山东省泰安市2011届高三上学期期末考试化学试题 题型:058
已知Fe(OH)2是白色难溶于水的物质,很容易被空气中的氧气氧化为Fe(OH)3.如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑和6 mol/L的硫酸,其它试剂自选.

请填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是________;
(2)实验开始时应先将活塞E________(填“打开”或“关闭”),C中收集到的气体的主要成份是________;
(3)简述生成Fe(OH)2的操作过程________;
(4)(3)操作后拔出装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式________.
查看答案和解析>>
科目: 来源:山东省泰安市2011届高三上学期期末考试化学试题 题型:058
某化学小组的同学到实验室学习.在实验桌上摆有下列仪器:
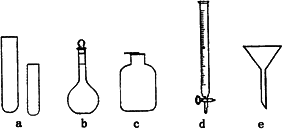
(1)指导教师要求同学们写出仪器的名称,甲同学书写的答案如下表,请你找出其中的错误,将改正后的名称填写在下表中(若正确,则该空不需要填写).

(2)关于e的用途,乙同学说:组成防倒吸装置.你还能说出其他两种用途吗?
①________;
②________.
(3)丙同学想用下图装置以大理石和稀盐酸反应制取CO2.教师指出,这需要太多的稀盐酸,造成浪费.该同学选用了上面的一种仪器,加在装置上,解决了这个问题.请你把该仪器画在图中合适的位置.

查看答案和解析>>
科目: 来源:山东省莱芜一中2011届高三上学期期末复习诊断性测试(二)化学试题 题型:058
二次合金中含有金、银、铂、钯等贵重金属,实验室以二次合金为原料提取金、银、铂、钯等贵重金属的步骤如下,试回答下列问题:
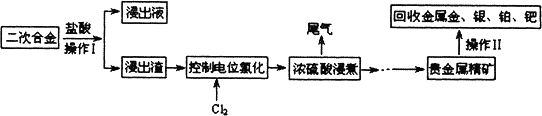
(1)浓硫酸浸煮过程中产生尾气的主要成分是________(填写代号,下同),欲对该气体进行检验,最好的试剂是________;
A.H2
B.SO2
C.灼热的氧化铜粉末
D.品红试剂
(2)操作Ⅰ的实验名称是________,完成该实验需要的玻璃仪器有________(填写仪器名称);
(3)实验室制备的Cl2中混有水蒸气和HCl杂质,甲同学设计了如下图所示的实验装置来证明水蒸气和HCl杂质的存在,请根据甲同学的设计意图完成下列有关问题.
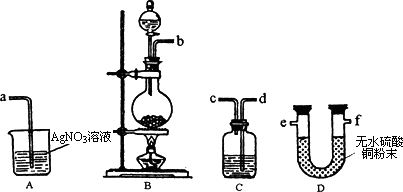
①各实验装置的接口顺序为:b接________,________接________,________接a;
②装置C的作用是________;
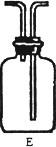
③乙同学认为甲同学的实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种.为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加装置E.你认为装置E应加在________之间(填装置序号),并且在广口瓶中放入________(填写所用试剂或用品名称).
查看答案和解析>>
科目: 来源:江西省南昌市南昌一中、南昌十中2011届高三第三次联考化学试题 题型:058
某化学研究性学习小组探讨
Fe3+和SO32-之间发生怎样的反应,请你一起参与并协助他们完成实验.(1)提出猜想:
甲同学认为发生氧化还原反应,其反应的离子方程式为________;
乙同学认为发生双水解反应,其反应方程式为
2Fe3++3SO32-+6H2O=2Fe(OH)3(胶体)+3H2SO3;(2)实验验证:
丙同学设计了下列实验来探究反应的可能性.
①为了检验所用Na2SO3是否变质,应选用的试剂是________.
②取5 mL FeCl3溶液于试管中,逐滴加入Na2SO3溶液至过量,观察到溶液颜色由黄色变为红棕色(无气泡产生,也无沉淀生成).
③将②溶液分成两等份,其中一份加入稀盐酸至过量,再加入BaCl2稀溶液,有白色沉淀生成;另一份滴入几滴KSCN溶液,溶液变成血红色.
(3)得出结论:
①根据丙同学的实验得出的结论是:________;
②实验③中溶液变成血红色的离子方程式为________.
(4)拓展探究:
①丁同学在FeCl3溶液中加入Na2CO3溶液,观察到红褐色沉淀并且产生无色气体,该反应的离子方程式是________.
②从形式上看,Na2CO3和Na2SO3相似,但是从上述实验中可以看到,二者的水溶液与氯化铁溶液反应的现象差别很大,其可能的原因除SO32-水解能力较CO32-小外,还有________.
查看答案和解析>>
科目: 来源:辽宁省沈阳四校协作体2012届高三12月月考化学试题 题型:058
空气吹出法工艺,是目前“海水提溴”的最主要方法之一.其工艺流程如下:
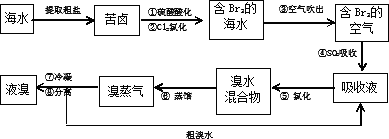
(1)溴在周期表中位于________周期,________族.
(2)步骤④的离子方程式:________.
(3)已知溴的沸点是58.5℃,步骤⑥的蒸馏过程中,溴出口温度为何要控制在80-90℃.温度过高或过低都不利于生产,请解释原因:________.
(4)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离.若在实验室分离上述混合物的分离仪器的名称是________,分离时液溴从分离器的________(填“上口”或“下口”)排出.
(5)为什么不直接用含溴的海水进行蒸馏得到液溴,而要经过“空气吹出、SO2吸收、氯化”:________.
查看答案和解析>>
科目: 来源:辽宁省沈阳四校协作体2012届高三12月月考化学试题 题型:058
为检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用酸性高锰酸钾溶液浸湿的脱脂棉.
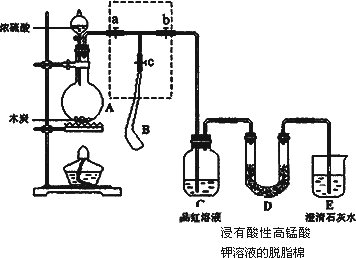
请回答下列问题:
(1)装置A、D中发生反应的化学方程式为________;________.
(2)实验前欲检查装置A的气密性,可以采取的操作是________;
(3)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,则正确的操作顺序是________(用操作编号填写)
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(4)实验时,装置C中的现象为________;
(5)当D中产生________现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;
(6)装置D的作用为________.
查看答案和解析>>
科目: 来源:陕西省宝鸡中学2012届高三第三次月考化学试题 题型:058
实验室里临时需要用NaOH溶液和CO2来制取纯Na2CO3溶液.已知CO2气体通入NaOH溶液过程中极易过量生成NaHCO3,且无明显现象.
实验室有下列试剂:
①未知浓度的NaOH溶液;
②37﹪的盐酸;
③37﹪的硫酸;
④14﹪的盐酸;
⑤大理石;
⑥K2CO3固体;
⑦碱式碳酸铜.
实验室有以下仪器:铁架台,启普发生器,量筒,烧杯,橡皮管,玻璃导管,分液漏斗.已知下表中各物质在常温时的溶解度(g/100 g H2O)
(1)实验应选用的仪器:除启普发生器,橡皮管,玻璃导管外,还需要:________;
(2)为了保证制得的Na2CO3溶液尽量纯,应选用的药品(填编号):除①外,还需要:________;
(3)简要叙述实验步骤,直到制得纯Na2CO3溶液(仪器安装可省略).
________.
(4)据实验给出的溶解度表,求出当NaOH溶液中溶质的质量分数大于________时,在通入CO2过程中会有晶体析出.
查看答案和解析>>
科目: 来源:陕西省宝鸡中学2012届高三第三次月考化学试题 题型:058
某化学小组用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,其实验流程如下所示:
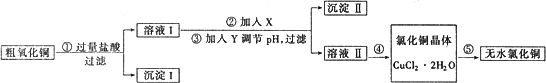
(1)步骤①、③的过滤操作中,除用到铁架台(带铁圈)外,还需要使用的玻璃仪器是________.
(2)已知:
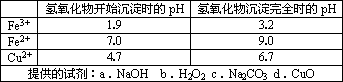
参照表中给出的数据和试剂,请回答:步骤②的目的是________,反应的离子方程式是________.
步骤③中调节溶液pH的范围是________,试剂Y是________(填字母).
(3)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl2·2H2O,其原因是________.
查看答案和解析>>
科目: 来源:陕西省宝鸡中学2012届高三第三次月考化学试题 题型:058
(1)下列物质属于非电解质的是________,属于弱电解质的是________.(填序号)
①氨水
②SO2
③Cl2
④HF
⑤BaSO4
⑥CH3CH2OH
⑦H2O
⑧NaHCO3
⑨Al2O3
(2)向氯水中滴加几滴紫色石蕊试液后的现象是________;
用离子方程式说明原因________.
(3)设计实验证明某种白色晶体是硫酸铵________.
(4)实验室制取氨气的反应的化学方程式为________,下图各种尾气吸收装置中,适合于吸收氨气,而且能防止倒吸的有________.(填序号)
A.![]()
B.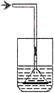
C.
D.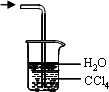
(5)如下图所示,氨气因极易溶于水而形成喷泉实验,请写出引发喷泉的操作是________;在下表中所列各组试剂也能形成喷泉的有(填序号)________.
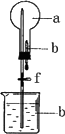

查看答案和解析>>
科目: 来源:江西省白鹭洲中学2012届高三上学期期中考试化学试题 题型:058
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混物.探究过程如下:
查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO
提出假设:
假设1:红色粉末是Fe2O3,
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3,和Cu2O的混合物
设计探究实验:
取少量粉末放人足量稀硫酸中,在所得溶液中再滴加KSCN试剂.
(1)若假设l成立,则实验现象是________.
(2)若滴加KSCN试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁.你认为这种说法合理吗?________,简述你的理由(不需写出反应的方程式)________.
(3)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则证明原固体粉末是________.
探究延伸:
经实验分析,确定红色粉末为Fe2O3,和Cu2O的混合物.
(4)实验小组欲用加热法测定Cu2O的质量分数.取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com