
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第2章 第4讲 氧化还原反应的基本概念(鲁科版) 鲁科版 题型:058
某学生往一支试管中按一定的顺序分别加入下列几种物质(一种物质只加一次):
A.KI溶液
B.淀粉溶液
C.NaOH溶液
D.稀H2SO4
E.氯水
发现溶液颜色按如下顺序变化:
①无色→②棕黄色→③蓝色→④无色→⑤蓝色.依据溶液颜色的变化,回答下列问题:
(1)加入以上药品的顺序是(写序号)________.
(2)①→②反应的化学方程式为________.
(3)溶液由棕黄色变为蓝色的原因是________.
(4)③→④反应的化学方程式为________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第2章 第3讲 离子的检验、鉴别及推断(鲁科版) 鲁科版 题型:058
有一白色固体混合物,可能含有的阴、阳离子分别是
为了鉴定其中的离子,现进行如下实验,根据实验现象,填写下列表格:
(1)取该粉末,加水后得到无色溶液,且未嗅到气味;用pH试纸测得溶液的pH为12.

(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出.
![]()
![]()
(3)尚待检验的离子及其检验方法
![]()
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第2章 第3讲 离子的检验、鉴别及推断(鲁科版) 鲁科版 题型:058
有一无色透明溶液,可能含Cu2+、NH![]() 、Al3+、Fe3+、Mg2+、Na+、K+、CO
、Al3+、Fe3+、Mg2+、Na+、K+、CO![]() 、SO
、SO![]() 、NO
、NO![]() 等离子中的若干种.现做如下实验:
等离子中的若干种.现做如下实验:
①取少量该溶液,滴入用盐酸酸化的BaCl2溶液,有白色沉淀生成.
②另取部分溶液,加入过氧化钠,有无色气体放出,且有白色沉淀产生,加入过氧化钠的量与生成白色沉淀的量可用下图表示.
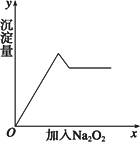
试推断:
(1)该溶液中一定存在________,一定不存在________,可能存在________.
(2)上述溶液中至少有________等物质混合而成.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第2章 第3讲 离子的检验、鉴别及推断(鲁科版) 鲁科版 题型:058
某强碱性溶液中含有的离子是K+、NH![]() 、Al3+、[Al(OH)4]-、CO
、Al3+、[Al(OH)4]-、CO![]() 、SiO
、SiO![]() 、Cl-中的某几种,进行如下实验:
、Cl-中的某几种,进行如下实验:
①取少量的溶液用硝酸酸化后,该溶液无沉淀生成;②另取少量溶液,加入盐酸其发生的现象是:一段时间保持原样后,开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
试回答下列问题:
(1)原溶液中肯定存在的是________,肯定不存在的是________.
(2)已知一定量的原溶液中加入5 mL 0.2 mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.187 g,则原溶液中是否含有Cl-?
________.
(3)请写出此题中肯定发生的离子方程式:________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第2章 第3讲 离子的检验、鉴别及推断(鲁科版) 鲁科版 题型:058
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH![]() 、Cl-、CO
、Cl-、CO![]() 、SO
、SO![]() ,现取两份100 mL溶液进行如下实验:
,现取两份100 mL溶液进行如下实验:
①第一份加过量NaOH溶液加热后,只收集到气体0.02 mol,无沉淀生成,同时得到溶液甲.
②在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g.
③第二份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65 g.
根据上述实验回答:
(1)一定不存在的离子是________,不能确定是否存在的离子是________.
(2)试确定溶液中肯定存在的离子及其浓度(可不填满):
离子符号________,浓度________;
离子符号________,浓度________;
离子符号________,浓度________.
(3)试确定K+是否存在________(填“是”或“否”),判断的理由是________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第2章 第2讲 电解质(鲁科版) 鲁科版 题型:058
某无色溶液,由Na+、Ag+、Ba2+、Al3+、[Al(OH)4]-、MnO![]() 、CO
、CO![]() 、SO
、SO![]() 中的若干种组成,取该溶液进行如下实验:
中的若干种组成,取该溶液进行如下实验:
①取适量试液,加入过量盐酸,有气体生成,并得到溶液;
②在①所得溶液中再加入过量碳酸氢铵溶液,有气体生成;同时析出白色沉淀甲;
③在②所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出.
根据上述实验回答下列问题:
(1)溶液中一定不存在的离子是________;
(2)一定存在的离子是________;
(3)判断沉淀乙成分的方法是________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第2章 第2讲 电解质(鲁科版) 鲁科版 题型:058
在烧杯里加入20 mL 0.1 mol/L的Ba(OH)2溶液,再滴几滴酚酞试液,然后用滴定管向烧杯中滴加等物质的量浓度的NaHSO4溶液.实验装置如下图(夹持仪器已去掉):
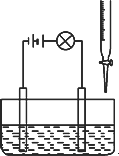
实验现象如下:
①灯泡逐渐变暗;
②烧杯中有白色沉淀生成,溶液红色变浅甚至消失.
请依据实验现象回答下列问题:
(1)灯泡变暗的原因是________.
(2)有白色沉淀生成,说明________,红色变浅说明________.
(3)当Ba2+恰好完全沉淀时,消耗NaHSO4溶液的体积为________ mL,溶液呈________色,离子反应方程式为________.
(4)若向(3)得到的溶液中,继续滴加NaHSO4溶液到恰好变为无色,此阶段的离子反应方程式为________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第1章 第2讲 物质的量浓度(鲁科版) 鲁科版 题型:058
(1)向Fe(OH)3胶体中加入饱和(NH4)2SO4溶液,发生的现象是________,原因是________.
(2)在Fe(OH)3胶体中逐渐滴入HI稀溶液,会出现一系列变化.
①先出现红褐色沉淀,原因是________.
②随后沉淀溶解,溶液呈黄色,此反应的离子方程式是________.
③最后溶液颜色加深,原因是________,此反应的离子方程式是________.
(3)若用稀盐酸代替HI稀溶液,能出现(3)所述变化现象中的________(填写上面各题序号).
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第1章 第2讲 物质的量浓度(鲁科版) 鲁科版 题型:058
某学生欲配制6.0 mol/L的H2SO4 1 000 mL,实验室有三种不同浓度的硫酸:
①480 mL 0.5 mol/L的硫酸;
②150 mL 25%的硫酸(ρ=1.18 g/mL);
③足量的18 mol/L的硫酸.
有三种规格的容量瓶:250 mL、500 mL、1 000 mL.老师要求把①②两种硫酸全部用完,不足的部分由③来补充.
请回答下列问题:
(1)实验所用25%的硫酸的物质的量浓度为________mol/L(保留1位小数).
(2)配制该硫酸溶液应选用容量瓶的规格为________mL.
(3)配制时,该同学的操作顺序如下,请将操作步骤B、D补充完整.
A.将①②两溶液全部在烧杯中混合均匀;
B.用量筒准确量取所需的18 mol/L的浓硫酸________mL,沿玻璃棒倒入上述混合液中.并用玻璃棒搅拌,使其混合均匀;
C.将混合均匀的硫酸沿玻璃棒注入所选的容量瓶中;
D.________________;
E.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2 cm处;
F.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
G.将容量瓶盖紧,振荡,摇匀.
(4)如果省略操作D,对所配溶液浓度有何影响?________(填“偏大”、“偏小”或“无影响”).
(5)进行操作C前还需注意________.
查看答案和解析>>
科目: 来源:山东省青州一中2012届高三化学一轮跟踪训练:第1章 第2讲 物质的量浓度(鲁科版) 鲁科版 题型:058
实验室需要0.1 mol/L NaOH溶液450 mL和0.5 mol/L硫酸溶液500 mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称).
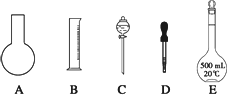
(2)下列操作中,容量瓶所不具备的功能有________(填序号).
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.量取一定体积的液体
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为________g.在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol/L(填“大于”、“等于”或“小于”,下同).若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________0.1 mol/L.
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为________mL(计算结果保留一位小数).如果实验室有15 mL、20 mL、50 mL量筒,应选用________mL量筒最好.配制过程中需先在烧杯中将浓
硫酸进行稀释,稀释时操作方法是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com