
科目: 来源:山西省大同一中2008-2009学年上学期高三期中试卷(化学) 题型:058
有A、B、C、D、E、F、G7瓶不同物质的溶液,它们各是KCl、MgCl2、Na2SO4、Na2CO3、AgNO3、Ca(NO3)2、Ba(OH)2溶液中的一种.为了鉴别,各取少量溶液进行两两混合,实验结果如表所示.表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显变化.试回答下面问题:

(1)A的化学式是________,G的化学式是________.判断理由是______________.
(2)写出其余几种物质的化学式:
B___________ C___________ D___________ E___________ F___________.
查看答案和解析>>
科目: 来源:辽宁省沈阳二中2008-2009学年高三上学期期中考试(化学) 题型:058
无水氯化铝是白色晶体,易吸收水分,在178℃升华.装有无水氯化铝的试剂瓶久置潮湿空气中,会自动爆炸并产生大量白雾.氯化铝常作为有机合成和石油工业的催化剂,并用于处理润滑油等.工业上由金属铝和氯气作用或由无水氯化氢气体与熔融金属铝作用而制得.
某课外兴趣小组在实验室里,通过下图所示装置制取少量纯净的无水氯化铝.
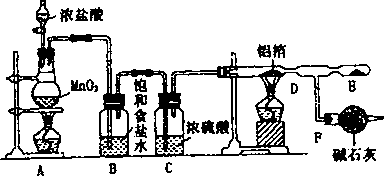
(1)A装置中发生反应的化学方程式为:_______________.
(2)在E处可收集到纯净的氯化铝,其原因是___________.
(3)从A装置导出的气体若不经过B、C装置而直接进入D管,将对实验产生不良的后果是:______________.
(4)F装置所起的作用有:______________.
(5)无水氯化铝在潮湿空气中,会产生大量白雾,有关反应的化学方程式为:
__________________________.
查看答案和解析>>
科目: 来源:辽宁省沈阳二中2008-2009学年高三上学期期中考试(化学) 题型:058
用下图装置进行实验,将A逐滴加入B中:
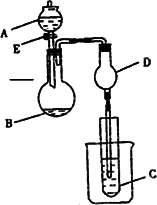
(1)若A为浓H2SO4,B为第三周期金属元素的片状单质,其在常温下难与水反应,C为品红溶液,实验中观察到溶液褪色,则B是________(填化学式),B与浓H2SO4反应的化学方学方程式为________.反应后往烧杯中加入沸水,又可观察到试管C中的现象为________.
(2)若B为Na2Co3,C为C6H5ONa溶液,实验中观察到小试管内溶液变浑浊,则酸A应具有的性质是________.然后往烧杯中加入沸水,可观察到试管C中的现象是____________.
查看答案和解析>>
科目: 来源:江西师大附中2009届高三上学期期中考试(化学) 题型:058
某化学课外活动小组学生用下图所示的装置研究P2O5能否干燥HCl气体.实验步骤为:①检验装置的气密性;②称量B、C、D、E、F(含连接的橡胶塞和玻璃管)仪器的质量(数据见下表),取58.5 g NaCl和足量浓硫酸;③迅速加入药品,连接好装置,反应开始,使干燥剂与气体充分作用;④当F内碱石灰由红色变为黄色时停止加热,冷却后称量B、C、D、E、F(含连接的橡胶塞和玻璃管)仪器的质量并记录数据.
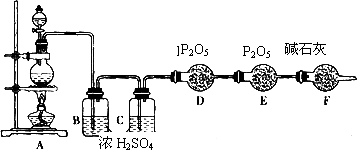
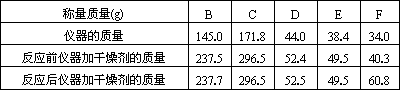
问:(1)B少量增重的原因是______________
(2)F增重的原因是_____________,F最大增重应是___________.
(3)通过上述实验,你能得出的结论是_______________________.
查看答案和解析>>
科目: 来源:江西师大附中2009届高三上学期期中考试(化学) 题型:058
在实验室里可用如图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质.

图中:①是氯气发生装置;②中试管里盛有15 mL 30%KOH溶液,并在热水浴中加热;③中试管里盛有15 mL 8%NaOH溶液,并置冰水浴中;④中试管里盛有紫色石蕊试液;⑤是尾气吸收装置.
(1)制取氯气时,通过________(填仪器名称)向烧瓶中加入适量的浓盐酸.为了除去氯气中的氯化氢气体,应在①和②之间安装盛有________(填试剂名称)的净化装置.
(2)图②中反应的离子方程式是:________;
图③中反应的离子方程式是:________.
(3)④中的现象是:________.
(4)如从图⑥中的A、B两端分别通入等体积的氯气和硫化氢气体,关闭A、B两端活塞,打开活塞C,一定可观察到的现象是________.
(5)若从图⑥中的A端通入氯气,待烧瓶内收集满氯气后,从B端逐渐通入足量的氨气,可观察到在烧瓶内出现红光和产生白烟等现象,表明氯气完全反应的现象是:________,发生反应的化学方程式是________,除了红光和白烟外,打开活塞C,还可观察到的现象是________.
查看答案和解析>>
科目: 来源:江苏省盐城中学2008-2009学年度高三上学期期中考试(化学) 题型:058
(化学实验)饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一.2005年的《化学教育》报道了如下实验研究:
实验一、定性研究:
①在试管中加入过量的块状碳酸钙,再加入约20 mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生.经检测,上述实验中产生的无色气体均为CO2.请回答:
(1)反应后所得的溶液漂白性增强的原因是____________.
(2)依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有__________.
实验二、定量研究:
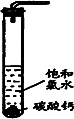
在圆底烧瓶底部,有一用塑料网包住的过量块状碳酸钙和150 mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解).请回答:
(3)为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是____________.
(4)用改进后的装置进行上述实验,测得塑料网内的碳酸钙质量减少Ag,总共收集到标准状况下的CO2气体BL,发现B/22.4 moL明显小于A/100 moL.若不考虑实验操作和CO2的溶解等因素造成的误差,从化学反应原理来看,导致这一大小关系的原因是____________.
(5)实验后发现,装置Ⅱ中的液体增多了,其原因是________.
查看答案和解析>>
科目: 来源:江苏省盐城中学2008-2009学年度高三上学期期中考试(化学) 题型:058
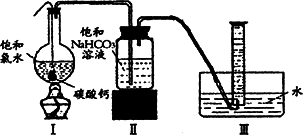
化学课外活动小组设计了如图所示的一套气体发生、收集和尾气吸收装置,以探究该装置的多功能性能.
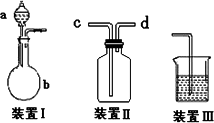
(1)甲同学认为装置Ⅰ可作为实验室制氧气的快速发生器,则装置Ⅰ的a仪器中可加入________或________,b仪器中加入________或________(与a中分别对应).装置Ⅱ从________管口进气即可作为O2的收集装置.
(2)丙同学认为利用装置Ⅱ,可收集NO,试简述操作方法:________
(3)戊同学认为利用装置Ⅰ和装置Ⅲ可进行验证Cl2的氧化性比Br2强的实验,进行此项实验时在装置Ⅰ中的a仪器中加入________试剂,b仪器中加入_________试剂,装置Ⅲ中应加入适量的________试剂,根据装置Ⅲ中观察到的________实验现象即可得出Cl2的氧化性比Br2强的结论.
查看答案和解析>>
科目: 来源:江苏省南京六中2008-2009学年度高三第一学期期中考试 化学试卷 题型:058
将磷肥生产中形成的副产物石膏(CaSO4·2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都具有重要意义.以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图.
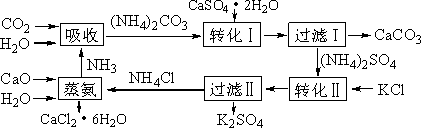
(1)本工艺中所用的原料除CaSO4·2H2O、KCl外,还需要________等原料.
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式:________.
(3)过滤Ⅰ操作所得固体中,除CaCO3外还含有________(填化学式)等物质,该固体可用作生产水泥的原料.
(4)过滤Ⅰ操作所得滤液是(NH4)2SO4溶液.检验滤液中含有CO![]() 的方法是:________.
的方法是:________.
(5氯化钙结晶水合物(CaCl2·6H2O)是目前常用的无机储热材料,选择的依据是________
a.熔点较低(29℃熔化) b.能导电 c.能制冷 d.无毒
(6)上述工艺流程中体现绿色化学理念的是:___________________________.
查看答案和解析>>
科目: 来源:江苏省南京六中2008-2009学年度高三第一学期期中考试 化学试卷 题型:058
工业上用铝土矿(主要成分是Al2O3,还有少量的Fe2O3、SiO2)提取冶炼铝的原料氧化铝.工艺流程如下图
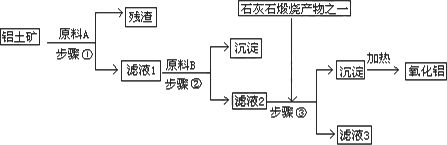
(1)原料A的名称是________,步骤①反应的离子方程式是________.
(2)滤液1中要加入稍过量原料B,原料B的化学式是________,步骤②反应的离子方程式是:________.
(3)步骤③的化学方程式是:___________________.
(4)如果省去步骤①,即溶解铝土矿是从加入原料B开始,则会对氧化铝的提取有什么影响________.
查看答案和解析>>
科目: 来源:江苏省南京六中2008-2009学年度高三第一学期期中考试 化学试卷 题型:058
某品牌消毒液包装说明的部分内容摘录如下:主要有效成份为次氯酸钠,有效氯含量8000-10000 mg/L.可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用.切勿用于丝绸、毛、尼龙、皮革、油漆表面,勿用于铝、铜、碳钢制品.本品须密封,置阴凉暗处保存.请完成以下实验探究过程:
(一)阅读材料,获取信息
(1)推测该消毒液的酸碱性:________,原因是(用离子方程式表示)________.
(2)该消毒液还具有的化学性质是________性和________性.
(3)从该消毒液的保存要求分析,导致其失效的外界因素主要是________.
(二)确定要研究的问题
该消毒液对碳钢制品是否有腐蚀作用?
(三)设计方案,实施探究
用烧杯取少量样品,将一颗光亮的铁钉放入烧杯,浸泡一段时间.对可能产生的现象有如下假设:
假设①:有明显现象;
假设②:无明显现象.
(4)基于假设①,结论是铁钉被腐蚀,预期的实验现象是____________.
(5)基于假设②,结论是________,请设计实验进一步验证该结论,叙述实验操作:________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com