
科目: 来源:四川省乐山市2009届高三上学期第一次模拟考试、理科综合能力测试化学试题 题型:058
重铬酸铵[(NH4)2Cr2O7]是一种橘黄色的晶体,常用于石油精炼、制革、印染、烟火、陶瓷等行业,是一种重要的化工原料.
(1)已知在酸性条件下,重铬酸盐有强氧化性.向冷的酸性重铬酸铵溶液中通入H2S,可得到Cr3+和S,写出反应的离子方程式:________.
(2)在150℃时,重铬酸铵迅速呈膨胀式分解,发生如下主要反应:(NH4)2Cr2O7=Cr2O3+4H2O+N2↑,
但同时要发生副反应.某同学设计了如下装置,探究副反应的生成物:

①装置中棉花的作用是________;加热前,该同学先通过导管K向试管中通一会N2,其目的是________;
②连接a、b,关闭导管K,加热使反应发生.若装置A中所盛溶液为酚酞溶液,且溶液变红,说明有________产生,仪器X的作用是________;若装置A中所盛溶液为新制的硫酸亚铁溶液,且出现棕红色的沉淀,说明副反应中有________产生,写出产生该沉淀的离子方程式________.
查看答案和解析>>
科目: 来源:四川省乐山市2009届高三上学期第一次模拟考试、理科综合能力测试化学试题 题型:058
有一瓶澄清溶液,可能含有K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、Cl-、I-.根据如下各步实验,完成相应填空.
(1)用pH试纸检验,溶液呈强酸性,说明一定不存在的是(填离子符号,下同)________;
(2)取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡、静置后,CCl4层呈紫红色,反应的离子方程式为________,该实验说明原溶液一定存在的离子是________,一定不存在的离子是________;
(3)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀产生,说明原溶液中一定不存在的离子是________;
(4)取(3)所得溶液加热,加入Na2CO3溶液,有白色沉淀产生,说明原溶液中一定还存在的离子是________,一定不存在的离子是________.
通过上述实验,还不能确定是否存在的是________.
查看答案和解析>>
科目: 来源:上海交通大学附中2009学年度第一学期高三摸底(化学) 题型:058
某学生为探究CO2与NaOH溶液的反应过程,进行了以下实验:
(1)在100 mL 2 mol/L的NaOH溶液中通入一定量的CO2
(2)在以上溶液中取出20 mL,滴加一定浓度的盐酸溶液至过量.在滴加过程中产生气体的物质的量与加入盐酸体积的关系如图,试讨论:
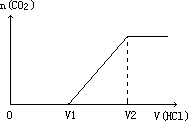
①如V1/(V2-V1)=1,实验(1)中通入CO2的体积为________mL(S·T·P)
②如V1/(V2-V1)>1,实验(1)中通入CO2的体积为________mL(S·T·P)
③如V1/(V2-V1)<1,实验(1)中通入CO2的体积为________mL(S·T·P)
④如V2=40 mL,加入盐酸溶液的浓度为________.
查看答案和解析>>
科目: 来源:上海交通大学附中2009学年度第一学期高三摸底(化学) 题型:058
已知甲酸经浓硫酸加热脱水可制得CO,以下试剂和仪器(酒精灯未画出,仪器可重复使用)用于测定当CO气流通过Fe2O3粉末后,发生反应的CO在CO总量中所占的百分比.
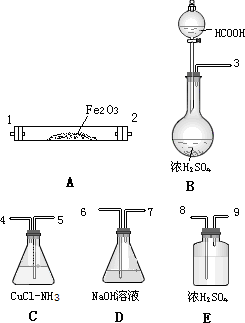
(1)氯化亚铜和氨水溶液吸收CO,实验装置合理的连接顺序自左至右为(填装置接口编号,空格不一定填满)
( )( )( )( )( )( )( )( )( )( )( )( )
(2)装置C和D的顺序不能颠倒,原因是________.
(3)装置B的反应中,浓硫酸是________.
a.吸水剂 b.脱水剂 c.氧化剂
(4)设装置C、D的增重为Δm(C)、Δm(D),发生反应的CO在CO总量中所占的质量分数(CO%)可表示为:CO%=________
如装置D、E的顺序颠倒,将使实验结果CO%________.(填增大、减小或不变)
(5)已知草酸(H2C2O4)有下列反应:H2C2O4(固)![]() CO+CO2+H2O
CO+CO2+H2O
用草酸热分解代替装置B进行上述实验,下列判断正确的是________.
a.不可行
b.增加CO2吸收装置也可行
c.不必增加任何装置也可行
查看答案和解析>>
科目: 来源:陕西省西安中学2009届摸底考试、化学试题 题型:058
现有含NaCl、Na2SO4和NaNO3的混合溶液,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-和NO3-的相互分离.相应的实验过程如下:
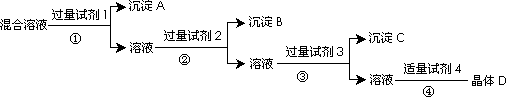
(1)写出上述实验过程中所用试剂的名称:
试剂1________;试剂2________;试剂4________.
(2)加入过量试剂3的目的是________.
(3)在加入试剂4后,获得晶体D的实验操作④步骤是________.(填操作名称)
查看答案和解析>>
科目: 来源:江苏省武进高级中学2009届高三模拟试题(化学) 题型:058
由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样进行下列实验(部分产物略去):
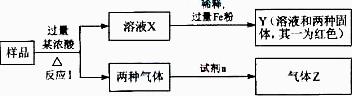
![]() (1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填化学式)________.
(1)取少量溶液X,加入过量的NaOH溶液,有沉淀生成.取上层清液,通入CO2,无明显变化,说明样品中不含有的物质是(填化学式)________.![]()
(2)Z为一种或两种气体:
①若Z只为一种气体,试剂a为饱和NaHCO3溶液,则反应Ⅰ中能同时生成两种气体的化学方程式是________.
②若Z为两种气体的混合物,试剂a为适量的水,则Z中两种气体的化学式是________.
(3)向Y中通入过量的Cl2,并不断搅拌,充分反应后,溶液中的阳离子是(填写离子符号)________.
(4)取Y中的溶液,调节pH约为7,加入淀粉KI和H2O2,溶液呈蓝色并有红褐色沉淀生成.当消耗2 mol I-时,共转移3 mol电子,该反应的离子方程式是________.
(5)另取原样品,加入足量稀硫酸充分反应,若溶液中一定不会产生Y中的红色固体,则原样品中所有可能存在的物质组合是(各组合中物质用化学式表示)________.
查看答案和解析>>
科目: 来源:江苏省武进高级中学2009届高三模拟试题(化学) 题型:058
现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2).已知实验中可能会发生下列反应:
①2Mg+O2![]() 2MgO;②3Mg+N2
2MgO;②3Mg+N2![]() Mg3N2;③2Mg+CO2
Mg3N2;③2Mg+CO2![]() 2MgO+C;④Mg+H2O
2MgO+C;④Mg+H2O![]() MgO+H2↑;⑤Mg3N2+6H2O
MgO+H2↑;⑤Mg3N2+6H2O![]() 3Mg(OH)2+2NH3↑
3Mg(OH)2+2NH3↑
可供选择的装置和药品如下图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连).
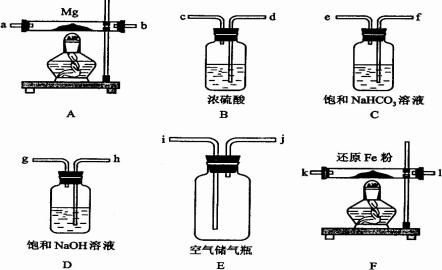
回答下列问题;
(1)在设计实验方案时,除装置A、E外,还应选择的装置________(填字母代号)及其目的分别________________;
(2)连接并检查实验装置的气密性.实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)________;
(3)通气后,如果同时点燃A、F装置的酒精灯,对实验结果有何影响?________,原因是________________;
(4)请设计一个实验,验证产物是氮化镁:_____________________________
查看答案和解析>>
科目: 来源:江苏省无锡市2009届高三上学期模拟考试、化学 题型:058
乙醛在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)________________;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置.在实验开始时温度计水银球的位置应在________,目的是________;当试管A内的主要反应完成后,应进行蒸馏操作,温度计水银球的位置应在___________________.
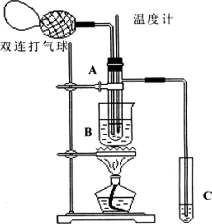
(3)烧杯B内盛装的液体可以是________(写出一种即可).
(4)若想检验试管C中是否含有产物乙酸,在下列所提供的药品或用品中,可以使用的是________.(填字母)
a.pH试纸
b.碳酸氢钠粉末
c.红色石蕊试纸
d.银氨溶液
查看答案和解析>>
科目: 来源:江苏省无锡市2009届高三上学期模拟考试、化学 题型:058
硫是煤中的有害成分.艾士卡法是世界公认的测定煤中硫含量的标准方法.
原理:将煤样与艾氏卡试剂(简称艾氏剂)混合灼烧,煤中的硫全部转化为硫酸盐,然后以BaCl2为沉淀剂使硫酸根离子转化为硫酸钡沉淀.根据硫酸钡的质量计算煤样中硫的含量.艾氏剂是质量比为2∶1的轻质MgO与无水Na2CO3的混合物.
实验步骤:
①称取粉碎的干燥煤样1.00 g和艾氏剂2 g置于30 mL的瓷坩埚中,充分混匀,再用1 g艾氏剂覆盖.高温加热1~2 h.
②取出坩埚,冷却到室温,将灼烧物放入烧杯中,用热蒸馏水冲洗坩埚内壁,将冲洗液加入烧杯中,再加入100~150 mL煮沸的蒸馏水,充分搅拌.
③过滤,用热蒸馏水冲洗烧杯3次,冲洗液加入过滤器.再用热蒸馏水清洗残渣至少10次.
④在上述滤液中滴加盐酸溶液,使溶液呈微酸性.将溶液加热至沸腾,在不断搅拌下滴入BaCl2溶液l0 mL,在近沸腾状况下保持2 h.
⑤将溶液与其中沉淀放置过夜后,经过滤、洗涤、干燥后称量,得沉淀m1g.
⑥艾氏剂应进行空白实验(实验除不加煤样外,全部按步骤①~⑤进行,目的是排除其他含硫物质的干扰),得到沉淀质量为m2g.
根据以上知识回答下列问题:
(1)写出煤中燃烧产生的二氧化硫被艾氏剂中的Na2CO3吸收生成硫酸盐的化学方程式________.
(2)如果步骤③中残渣清洗不充分,实验结果将________.如果步骤④中用硫酸代替盐酸,实验结果将________(均填“偏大”、“偏小”或“无影响”)
(3)步骤④在滤液中滴加盐酸使溶液呈微酸性的目的是________________.
(4)如何用实验证明步骤⑤中的沉淀已洗净?____________________.
(5)用上述实验数据(包括字母)表示出该煤样中硫元素质量分数____________.
查看答案和解析>>
科目: 来源:江苏省溧阳市南渡高级中学2009届高三模拟考试(化学) 题型:058
某化学研究性学习小组为测定果汁中
Vc含量,设计并进行了以下实验.Ⅰ实验原理
将特定频率的紫外光通过装有溶液的比色皿,一部分被吸收,通过对比入射光强度和透射光强度之间的关系可得到溶液的吸光度(用A表示,可由仪器自动获得).吸光度A的大小与溶液中特定成分的浓度有关,杂质不产生干扰.溶液的pH对吸光度大小有一定影响.
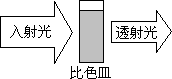
Ⅱ实验过程
(1)配制系列标准溶液.分别准确称量质量为1.0 mg、1.5 mg、2.0 mg、2.5 mg的标准Vc试剂,放在烧杯中溶解,加入适量的硫酸,再将溶液完全转移到100 mL容量瓶中定容.
上述步骤中所用到的玻璃仪器除烧杯、容量瓶外还有________.
(2)较正分光光度计并按顺序测定标准溶液的吸光度.为了减小实验的误差,实验中使用同一个比色皿进行实验,测定下一溶液时应对比色皿进行的操作是________.测定标准溶液按浓度________(填“由大到小”或“由小到大”)的顺序进行.
(3)准确移取10.00 mL待测果汁样品到100 mL容量瓶中,加入适量的硫酸,再加水定容制得待测液,测定待测液的吸光度.
Ⅲ数据记录与处理
(4)实验中记录到的标准溶液的吸光度与浓度的关系如下表所示,根据所给数据作出标准溶液的吸光度随浓度变化的曲线.
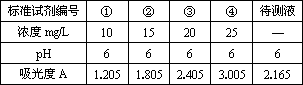
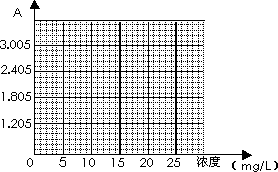
(5)原果汁样品中Vc的浓度为________mg/L
(6)实验结果与数据讨论除使用同一个比色皿外,请再提出两个能使实验测定结果更加准确的条件控制方法________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com