
科目: 来源:2008年普通高等学校招生全国统一考试(上海卷)、化学 题型:058
如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体在同温同压下测定).试回答下列问题:

(1)实验1中,沉淀最终变为________色,写出沉淀变色的化学方程式________.
(2)实验2甲针筒内的现象是:有________生成,活塞________移动(填向外、向内、不).
反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入________溶液中.
(3)实验3中,甲中的30 mL气体是NO2和N2O4的混合气体,那么甲中最后剩余的无色气体是________,写出NO2与H2O反应的化学方程式________.
(4)实验4中,已知:3Cl2+2NH3→N2+6HCl.甲针筒除活塞有移动,针筒内有白烟产生外,气体的颜色变化为________,最后针筒中剩余气体的体积约为________mL.
查看答案和解析>>
科目: 来源:2008年普通高等学校招生全国统一考试(海南卷)、化学 题型:058
如何防止铁的锈蚀是工业上研究的重点内容.为研究铁锈蚀的影响因素,某同学做了如下探究实验:
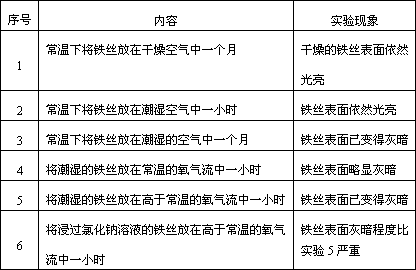
回答以下问题:
(1)上述实验中发生了电化学腐蚀的是(填实验序号)________;在电化学腐蚀中,负极反应是________;正极反应是________;
(2)由该实验可知,可以影响铁锈蚀速率的因素是________;
(3)为防止铁的锈蚀,工业上普遍采用的方法是________(答两种方法)
查看答案和解析>>
科目: 来源:2008年普通高等学校招生全国统一考试(海南卷)、化学 题型:058
现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2).已知实验中可能会发生下列反应:
①2Mg+O2![]() 2MgO;②3Mg+N2
2MgO;②3Mg+N2![]() Mg3N2;③2Mg+CO2
Mg3N2;③2Mg+CO2![]() 2MgO+C;④Mg+H2O
2MgO+C;④Mg+H2O![]() MgO+H2↑;⑤Mg3N2+6H2O
MgO+H2↑;⑤Mg3N2+6H2O![]() 3Mg(OH)2+2NH3↑
3Mg(OH)2+2NH3↑
可供选择的装置和药品如下图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连).
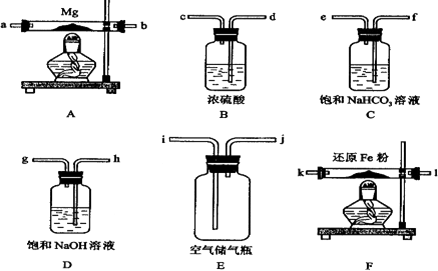
回答下列问题;
(1)在设计实验方案时,除装置A、E外,还应选择的装置(填字母代号)及其目的分别________;
(2)连接并检查实验装置的气密性.实验开始时,打开自来水的开关,将空气从5升的储气瓶压入反应装置,则气流流经导管的顺序是(填字母代号)________;
(3)通气后,如果同时点燃A、F装置的酒精灯,对实验结果有何影响?________,原因是________;
(4)请设计一个实验,验证产物是氮化镁:________
查看答案和解析>>
科目: 来源:2008年普通高等学校招生全国统一考试(广东卷)、化学 题型:058
镁、铜等金属离子是人体内多种酶的辅因子.工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁.
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有________.
(2)已知MgO的晶体结构属于NaCl型.某同学画出的MgO晶胞结构示意图如图所示,请改正图中错误:________.

(3)用镁粉、碱金属盐及碱土金属盐等可以做成焰火.燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:________.
(4)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:

解释表中氟化物熔点差异的原因:________.
(5)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b:

①a中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有________键的特性.
②微粒间的相互作用包括化学键和分子间相互作用,比较a和b中微粒间相互作用力的差异________.
查看答案和解析>>
科目: 来源:2008年普通高等学校招生全国统一考试(广东卷)、化学 题型:058
铜在自然界存在于多种矿石中,如:

请回答下列问题:
(1)上表所列铜化合物中,铜的质量百分含量最高的是________.
(2)工业上以黄铜矿为原料.采用火法溶炼工艺生产铜.该工艺的中间过程会发生反应:2Cu2O+Cu2S![]() 6Cu+SO2↑,反应的氧化剂是________.
6Cu+SO2↑,反应的氧化剂是________.
(3)SO2尾气直接排放到大气中造成环境污染的后果是________;处理该尾气可得到有价值的化学品,写出其中1种酸和1种盐的名称________.
(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制.请简述粗铜电解得到精铜的大批量:________.
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是________(填字母).
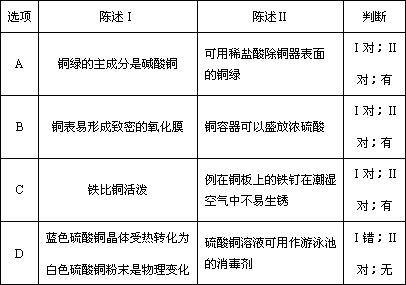
查看答案和解析>>
科目: 来源:2008年普通高等学校招生全国统一考试(广东卷)、化学 题型:058
某种催化剂为铁的氧化物.化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色.一位同学由此得出该催化剂中铁元素价态为+3的结论.
(1)请指出该结论是否合理并说明理由________.
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3 mol·L-1 H2SO4/3% H2O 2.6 mol·L-1 HNO3/0.01 mol·L-1 KmnO4、NaOH稀溶液、0.1 mol·L-1 Kl、20% KSCN、蒸馏水.
①提出合理假设
假设1:________;
假设2:________;
假设3:________.
②设计实验方案证明你的假设
③实验过程
根据②的实验方案,进行实验.请在答题卡上按下表格式写出实验操作步骤、预期现象与结论.

查看答案和解析>>
科目: 来源:2008年普通高等学校招生全国统一考试(广东卷)、化学 题型:058
某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0 mL、大理石用量为10.00 g.
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
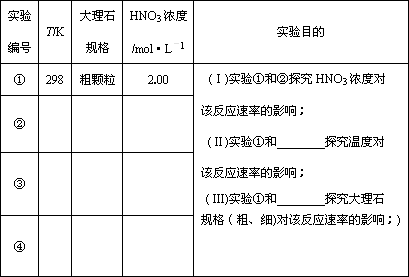
(2)实验①中CO2质量随时间变化的关系见下图:
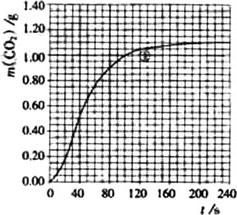
依据反应方程式![]() CaCO3+HNO3=
CaCO3+HNO3=![]() Ca(NO3)2+
Ca(NO3)2+![]() CO2↑+
CO2↑+![]() H2O,计算实验①在70-90 s范围内HNO3的平均反应速率(忽略溶液体积变化,写出计算过程).
H2O,计算实验①在70-90 s范围内HNO3的平均反应速率(忽略溶液体积变化,写出计算过程).
(3)画出实验②、③和④中CO2质量随时间变化关系的预期结果示意图.
查看答案和解析>>
科目: 来源:2008年普通高等学校招生全国统一考试(广东卷)、化学 题型:058
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料.工业碳酸钠(钝度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO![]() 等杂质,提纯工艺路线如下:
等杂质,提纯工艺路线如下:
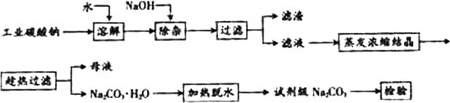
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
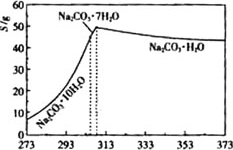
回答下列问题:
(1)滤渣的主要成分为________.
(2)“趁热过滤”的原因是________.
(3)若在实验室进行“趁热过滤”,可采取的措施是________(写出1种).
(4)若“母液”循环使用,可能出现的问题及其原因是________.
(5)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH1=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式________.
查看答案和解析>>
科目: 来源:贵州省凯里一中2009届第二轮限时训练理综化学(4) 题型:058
乳酸是人体生理活动中的一种代谢产物,近年来已成为人们研究的热点之一,其结构简式为:![]()
下图是采用化学方法对乳酸进行加工处理的过程:
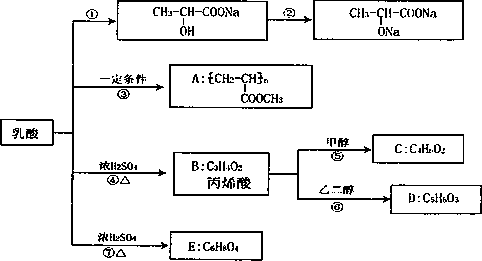
请回答有关问题:
(1)实验变化过程①和②时依次加入的试剂是________、________.
(2)完成转化③时所涉及的主要反应有三步,写出反应的化学方程式及其反应类型:
________,反应类型:________;
________,反应类型:________;
________,反应类型:________;
(3)化合物C的名称为________(填序号).
a.丙酸甲酯 b.甲酸丙烯酯 c.丙烯酸甲酯
(4)写出化合物D和E的结构简式:D________、E________.
查看答案和解析>>
科目: 来源:贵州省凯里一中2009届第二轮限时训练理综化学(4) 题型:058
如图是某化学兴趣小组的同学设计的制取NH3并进行NH3性质实验的改进装置.他们先称取mg固体氯化铵放入试管底部,再快速称取ng氢氧化钠固体盖在氯化铵表面,立即用带滴管的胶塞塞紧试管(滴管内事先吸入一定体积的浓氨水),慢慢挤压胶头滴管,立即看到试管内产生大量气泡.请回答有关问题:
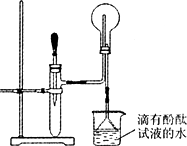
(1)该化学兴趣小组的同学对用此装置制取NH3的原理进行了分析,你认为合理的是(填序号):________;
①浓氨水中存在平衡:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH+4+OH-,NaOH使平衡向左移动;
NH+4+OH-,NaOH使平衡向左移动;
②浓氨水中存在平衡:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH+4+OH-,NH4Cl使平衡向左移动;
NH+4+OH-,NH4Cl使平衡向左移动;
③NaOH溶于水时放热,温度升高,NH3的溶解度减小,有部分NH3逸出;
④NH4Cl和NaOH在此条件下反应,生成NH3.
(2)简述判断图中烧瓶内收满NH3的现象:________;
(3)该实验还能证明NH3的什么性质?________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com