
科目: 来源:2009届9月北京明光中学高三教学检测、化学试卷 题型:058
①写出CO2和Na2O2反应的化学方程式__________________.
②某学生判断SO2和Na2O2反应能生成硫酸钠,你认为他的判断合理吗?________.简要说明理由:________.
③该同学无法断定SO2和Na2O2反应中是否有氧气生成,拟使用下列装置进行实验.

装置中B的作用是________,D的作用是________.
④为确认SO2和Na2O2反应产物,该同学设计了以下实验步骤,你认为应进行的操作按顺序排列是(填序号)________.
A.用带火星的细木条靠近干燥管口a,观察细木条是否着火燃烧.
B.将C装置中反应后的固体物质溶于适量水配成溶液.
C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液,观察是否有沉淀生成.
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成
查看答案和解析>>
科目: 来源:2009届9月北京明光中学高三教学检测、化学试卷 题型:058
有一纯净的亚硫酸钠晶体因部分被氧化而变质,为了测定样品中杂质的质量分数,现设计下列实验过程,按要求填写空格:

(1)向混合溶液中加入的无色溶液A是________,A必须过量的原因是________.
(2)白色沉淀C中含有________.
(3)无色溶液B通常是________溶液,加入后与C反应的离子方程式为________;若无色溶液B是硝酸溶液或硫酸溶液,是否能测定样品中杂质的质量分数?________(填是或否);请简要说明理由:
①__________________
②__________________
③__________________(可不填满也可补充)
(4)通过以上测定可得到样品中杂质的质量分数的计算式为________.
查看答案和解析>>
科目: 来源:2008年宁夏中卫一中高三第三次模拟考试、理科综合能力测试化学部分 题型:058
某兴趣小组设计出下图所示装置来改进教科书中“铜与硝酸反应”实验,以探究化学实验的“绿色化学”.
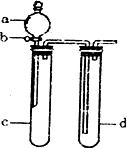
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,用热毛巾捂住C对其加热,其目的是________.
(2)在d中加适量NaOH溶液,c中放足量铜片,由分液漏斗a向c中加人2 mL浓硝酸,c中反应的化学方程式是________;再由a向c中加2 mL蒸馏水,c中的实验现象是________.
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是________,理由是________.

(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2.操作步骤为________,实验现象为________.但此实验的不足之处是________.
查看答案和解析>>
科目: 来源:2008年宁夏银川一中高三年级第三次模拟考试、理科综合试卷化学部分 题型:058
工业“从海水中提取镁”的流程图如下:
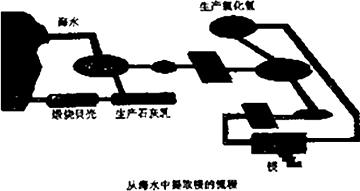
其步骤为:
①将海边大量存在的贝壳煅烧成石灰,并将石灰制成石灰乳;
②将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;
③在Mg(OH)2沉淀中加入盐酸得到MgC12溶液,再经蒸发结晶得到MgC12·5H2O;
④将MgC12·6H2O在一定条件下加热得到无水MgC12;
⑤电解熔融的氯化镁可得到Mg.
请回答下列问题:
(1)步骤③中的蒸发量是利用风吹日晒来完成的,而在实验室中进行蒸发操作需要的主要仪器有________、________、酒精灯、铁架台等.
(2)步骤④中的“一定条件”指的是________,目的是________.
(3)上述提取镁的流程中,在降低成本、减少污染方面做了一些工作,请写了出其中一点:________.
(4)有同学认为:步骤②后可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则.你同意该同学的想法吗?为什么?
你的观点是_______________.
理由中___________________.
查看答案和解析>>
科目: 来源:2008年宁夏银川一中高三年级第三次模拟考试、理科综合试卷化学部分 题型:058
某校化学实验兴趣小组进行实验室制取纯净的氯气、并验证氯气的某些化学性质实验,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题.
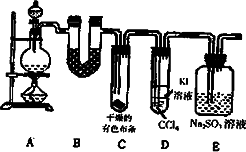
(1)下列方法中,不能用于制氯气的是________
①MnO2和浓盐酸混合共热;
②NaCl固体和浓硫酸混合共热;
③次氯酸钠和稀硫酸混合;
④KMnO4和浓盐酸混合.
⑤KClO3和浓盐酸混合;
(2)写出A装置中玻璃仪器的名称________
(3)若用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得Cl2的体积(标准状况下)总是小于1.12 L的原因是____________
(4)装置C中的现象是________________________
装置D振荡后静置,下层溶液的现象是________
装置E中发生反应的离子方程式为____________
(5)乙同学认为甲同学的实验有缺陷,该缺陷可能是________.
查看答案和解析>>
科目: 来源:2008届宁夏银川一中高三年级第一次模拟考试、理科综合能力测试化学部分 题型:058
某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的合成氨厂联合设计了以下制备硫酸铵的工艺流程:

请回答下列问题:
(1)合成氨反应的化学方程式是_____________________.
(2)沉淀池中发生的主要反应方程式是_______________.在上述流程的沉淀池中通入足量氨气的目的是________,可以循环使用的X是________.
查看答案和解析>>
科目: 来源:2008届宁夏银川一中高三年级第一次模拟考试、理科综合能力测试化学部分 题型:058
1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g/cm3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2-二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水).
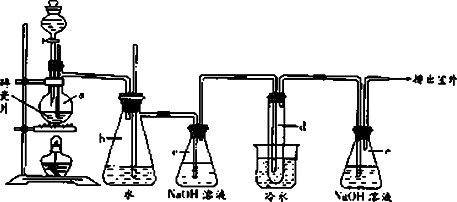
填写下列空白:
(1)写出a、d装置中的两个化学反应方程式.
_________________
_________________
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象____________.
(3)容器c中NaOH溶液的作用是________.
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因是_______________.
查看答案和解析>>
科目: 来源:2008届宁夏银川一中高三年级第六次月考测试、理科综合试卷化学部分 题型:058
以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
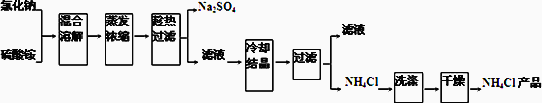
氯化铵和硫酸钠的溶解度随温度变化如图所示.回答下列问题:
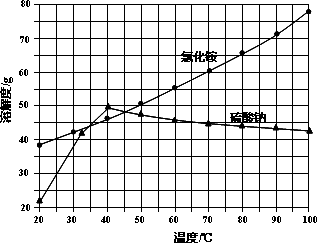
(1)欲制备10.7 g NH4Cl,理论上需NaCl________g.
(2)实验室进行蒸发浓缩用到的主要仪器有________、烧杯、玻璃棒、酒精灯等.
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为________.
(4)不用其它试剂,检查NH4Cl产品是否纯净的方法及操作是________.
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是________.
查看答案和解析>>
科目: 来源:2008届宁夏银川一中高三年级第六次月考测试、理科综合试卷化学部分 题型:058
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:先配制100 mL 0.10 mol·L-1 NaOH标准溶液,然后取20.00 mL待测稀盐酸溶液放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定.重复上述滴定操作3次,记录数据如下.
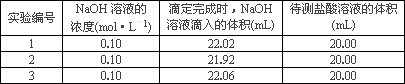
①滴定达到终点的标志是_____________________
②根据上述数据,可计算出该盐酸的浓度________
③排去碱式滴定管中气泡的方法应采用操作________,然后轻轻挤压玻璃球使尖嘴部分充满碱液.
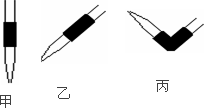
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________(多选扣分)
A.滴定终点读数时俯视读数
B.碱式滴定管尖嘴部分有气泡,滴定后消失
C.锥形瓶水洗后未干燥
D.锥形瓶水洗后用待测稀盐酸溶液润洗
E.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
查看答案和解析>>
科目: 来源:2008届宁夏省中卫一中高三化学第二学期第二次模拟理综化学部分 题型:058
某课外小组,用含有较多杂质的铜粉,通过不同的化学反应制取胆矾,其设计的实验过程为:

(1)铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于________上(用以下仪器的编号填空,下同),取用坩埚应使用________,灼烧后的坩埚应放在________上,不能直接放在桌面上.
a.泥三角
b.蒸发皿
c.石棉网
d.表面皿
e.坩埚钳
f.试管夹
(2)杂铜经灼烧后得到的产物是氧化铜及少量的铜的混合物,用以制取胆矾.灼烧后含有少量铜的可能原因是________
a、灼烧过程中部分氧化铜被还原
b、灼烧不充分铜未被完全氧化
c、氧化铜在加热过程中分解生成铜
d、该条件下铜无法被氧气氧化
(3)通过途径Ⅱ实现用粗铜制取胆矾,必须进行的实验操作步骤:酸溶、加热通氧气、过滤、________冷却结晶、自然干燥.
(4)由粗铜制氧化铜通过两种途径制胆矾,与途径Ⅰ相比,途径Ⅱ有两个明显优点是________
(5)在测定所得胆矾(CuSO4·XH2O)晶体中结晶水的实验过程中,称量操作至少进行________次
(6)若测定结果X值偏高,可能原因是________
a.加热温度过高
b.胆矾晶体的颗粒较大
c.加热后放在空气中冷却
d.胆矾晶体部分风化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com