
科目: 来源:广东省潮州市2011届高三二模理综化学试题 题型:058
纯碱、烧碱等是重要的化工原料.
(1)利用下图所示装置可间接证明二氧化碳与烧碱溶液发生了反应:将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是____
_______,反应的离子方程式是________.
(2)向100 mL 2 mol/L的NaOH溶液中通入一定量CO2,充分反应后将溶液在一定条件下蒸发结晶,得到少量的白色固体.试设计实验确认该白色固体的成分.
①提出合理假设.
假设1:该白色固体为NaOH
和Na2CO3;假设2:该白色固体为只有Na2CO3;
假设3:该白色固体为只有NaHCO3;
假设4:该白色固体为________.
②基于假设1,设计实验方案进行实验证明固体的成分是NaOH
和Na2CO3.请在答题卡上写出实验步骤及预期现象和结论.(步骤可不填满也可增加)限选实验试剂及仪器:1 moL·L
-1 HCl溶液、1 mol·L-1 MgCl2溶液、0.5 moL·L-1 BaCl2溶液、1 mol·L-1 Ba(OH)2溶液、甲基橙试液、酚酞试液、试管、胶头滴管、过滤装置.
查看答案和解析>>
科目: 来源:安徽省江南十校2011届高三二模冲刺卷理综化学试题 题型:058
三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O可用于摄影和蓝色印刷.某小组将无水三草酸合铁酸钾在一定条件下加热分解,对所得气体产物和固体产物进行实验和探究.实验装置图如下:

限选试剂:
浓H2SO4、、1.0 mo1·L-1 H2SO4、1.0 mo1·L-1 HNO3、1.0 mo1·L-1 NaOH、3%H2O2、1.0 mol·L-1 CuSO4、20% KSCN、饱和澄清石灰水、蒸馏水、0.1%酸性高锰酸钾溶液.
(1)实验时观察到:C试管中饱和澄清石灰水变浑浊,E试管中盛浓H2SO4,从E试管流出的气体被点燃,则气体产物是________.D试管中应盛有________溶液,其作用是:________________.
(2)固体产物中有钾盐和含铁元素的物质.该小组同学查阅资料后推知固体产物中铁元素无正三价形式,并对固体产物中铁元素存在形式进行了探究.实验过程如下:①取适量固体产物于试管中,加入足量蒸馏水,充分振荡.过滤取出不溶性固体,用蒸馏水充分洗涤.②向试管中加入少量上述不溶固体,加入过量CuSO4溶液,充分振荡.溶液的蓝色明显变浅,且有暗红色固体物质生成.③过滤取出暗红色不溶性固体,用蒸馏水洗涤至洗涤液无色.取少量该固体于试管中,加过量1.0 mol·L-1·H2SO4后,静置,取上层清液少许于试管中,滴加适量3% H2O2溶液,充分振荡后滴加20% KSCN溶液,发现溶液呈红色.
以上实验证明固体产物中铁元素的存在形式为:________.
(3)请你对固体产物中钾盐的成分进行探究.
①提出合理假设
假设1:全部为________(写化学式)
假设2:全部为K2C2O4
假设3:为以上二者的混合物.
②设计实验方案证明你的假设(不用作答)
③实验过程
根据②中方案进行实验.完成下表实验步骤、现象与结论.

查看答案和解析>>
科目: 来源:北京市昌平区2011届高三二模理综化学试题 题型:058
某有机化合物A因其具有麻醉作用,常用作局部麻醉剂和镇痛剂.它的结构简式如图所示,请回答:

(1)A的分子式是________.
(2)有机物A不能发生的化学反应有(填序号)________.
a.加成反应
b.消去反应
c.加聚反应
d.氧化反应
(3)满足下列条件的A的同分异构体有________种,写出其中一种的结构简式________.
①能与碳酸氢钠溶液反应;
②核磁共振氢谱显示有四种类型氢原子的吸收峰
(4)已知:

①试剂Ⅰ可以选用的是(填字母)________;
a.CH3COONa溶液
b.NaOH溶液
c.NaHCO3溶液
d.Na2CO3溶液
②上述转化过程中,设置步骤M→N的目的是________;
③写出P生成Q的化学方程式________;
④P与乙二酸在一定条件下可发生反应生成高分子化合物W,写出W的结构简式________.
查看答案和解析>>
科目: 来源:北京市昌平区2011届高三二模理综化学试题 题型:058
氧化铜有多种用途,如用作玻璃着色剂、油类脱硫剂等.为获得纯净的氧化铜,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如下实验:
![]()
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:

(1)步骤Ⅰ的目的是除不溶性杂质.所需操作的名称是________.
(2)步骤Ⅱ的目的是除硫酸亚铁.操作步骤是先滴加H2O2溶液,稍加热,当Fe2+转化完全后,慢慢加入Cu2(OH)2CO3粉末,搅拌,以调整溶液pH在一定范围之内,加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH=1.
①写出用H2O2溶液除去硫酸亚铁的离子方程式________.
②调整pH的范围应该在________之间.
(3)步骤Ⅲ的目的是得到CuSO4·5H2O晶体.操作是将溶液加热蒸发至有晶膜出现时,停止加热,________,水浴加热烘干.采用水浴加热的原因是________.
(4)该同学用CuSO4溶液进行如下探究实验:
取A、B两支试管,分别加入2 mL 5% H2O2溶液,再向H2O2溶液中分别滴入0.1 mol·L-1 FeCl3和CuSO4溶液各1 mL,摇匀,观察到滴入FeCl3溶液的试管产生气泡更快,由此得到结论:Fe3+对H2O2溶液分解的催化效率比Cu2+高,该同学的结论是否正确________(填正确或错误),请说明原因________.
查看答案和解析>>
科目: 来源:北京市大兴区2011届高三二模理综化学试题 题型:058
烃
A是石油裂解气中的一种成分,与A相关的反应如下:
请回答
:(1)A
的结构简式是________,B→C的反应类型:________.(2)
H的结构简式是________.(3)写出反应方程式:(要求注明反应的条件)
①E→I________.
②C与足量的![]() COOH________.
COOH________.
(4)E的同分异构体有多种,和E同类别的同分异构体共有________种:
写出其中一种不含甲基的同分异构体的结构简式________.
(5)某氨基酸(C4H9NO2)是组成人体蛋白质的氨基酸之一,可由G通过以下反应制取:
![]()
该氨基酸的结构简式是________.
查看答案和解析>>
科目: 来源:北京市大兴区2011届高三二模理综化学试题 题型:058
某兴趣小组在实验室用铜和硫酸为原料多种方法制取硫酸铜.制备方法如下:
方法一:铜与浓硫酸反应
(1)浓硫酸试剂瓶上适合贴上的标签是________(可多选).

(2)甲同学取6.4 g铜片和10 mL 18 mol·L-1浓硫酸,放在试管中共热时发现,铜与热的浓硫酸反应后并没有得到预期的蓝色溶液,而是在试管底部看到灰白色固体.甲同学为了验证其中白色固体的主要成分.设计下列实验:
实验步骤:倾倒掉上层液体后,向所得灰白色的固体中加入适量蒸馏水,边加边搅拌.
实验现象:________;实验结论:所得白色固体的化学式为________.
(3)甲还观察到加热时,在试管内壁上部析出少量淡黄色固体物质,持续加热,淡黄色固体物质又慢慢地溶于浓硫酸而消失.淡黄色固体消失的原因是(用化学反应方程式回答)________.
方法二:
(4)乙同学认为甲设计的实验方案不好,他自己设计的思路是:
2Cu+O2 2CuO,CuO+H2SO4
2CuO,CuO+H2SO4 CuSO4+H2O.对比甲的方案,你认为乙同学设计的实验方案的优点是________.
CuSO4+H2O.对比甲的方案,你认为乙同学设计的实验方案的优点是________.
方法三:
(5)丙同学取一铜片和稀硫酸放在试管中,再向其中滴入双氧水,发现溶液逐渐呈蓝色.
写出反应的化学反应方程式________.
方法四:
(6)请你再帮助该实验小组的同学设计一种只用铜和稀硫酸为原料制取硫酸铜的方法,写出该方方法中的化学反应方程式:________.
查看答案和解析>>
科目: 来源:北京市大兴区2011届高三二模理综化学试题 题型:058
短周期元素A、B、C、D、E、F、G其核外电子总数依次增多,A原子是元素中电子总数最少的,B的最外层电子数是次外层电子数的二倍,C最外层电子数是其电子层数的三倍,G与C同族且两元素核外电子总数之和与D、E两元素核外电子总数之和相等,F的最外电子数是次外层电子数的二分之一.
(1)、写出元素F在周期表中的位置________.
(2)、由元素ABC组成的18电子物质,是假酒中常见的有毒物质之一,其电子式为________.
(3)、已知这样两反应G(s)+C2(g) GC2(g) ΔH1=-296 KJ·mol-1,2GC3(g)
GC2(g) ΔH1=-296 KJ·mol-1,2GC3(g)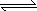 2GC2(g)+C2(g) ΔH2=+198 KJ·mol-1
2GC2(g)+C2(g) ΔH2=+198 KJ·mol-1
则2G(s)+3C2(g)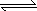 2GC3(g) ΔH3=________.
2GC3(g) ΔH3=________.
(4)、对于可逆反应:2GC2(g)+C2(g)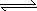 2GC3(g) ΔH=a KJ·mol-1图中两条曲线分别表示温度为T1和T2时体系中GC3的百分含量和时间的关系.
2GC3(g) ΔH=a KJ·mol-1图中两条曲线分别表示温度为T1和T2时体系中GC3的百分含量和时间的关系.
GC3%
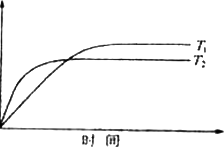
T1时平衡常数K1、T2时平衡常数K2,则K1________K2(>、<、=).
T2时在2 L密闭容器中充入4 moL GC2和3 moL C2,在一定条件下达到平衡时GC2的转化率为90%,则这时的平衡常数数值是________.
(5)、D2FC3溶液与E2(GC4)3溶液混合产生两种匀溶于DCA溶液的难溶物质,写出两溶液混合所发生的离子反应方程式________.
(6)向Ba(AGC3)2溶液中滴加足量A2C2产生23.3克白色沉淀时,反应中电子转移总数物质的量为________.
查看答案和解析>>
科目: 来源:广东省韶关市2011届高三一模理综化学试题 题型:058
氯气和漂白粉是现代工业和生活常用的消毒、杀菌剂.
(1)实验室拟用下列装置制备干燥纯净的氯气,请按照气体从左向右流动的方向将仪器进行连接:H→________、________→________、________→________;并指出其中广口瓶Ⅱ中的试剂为________;
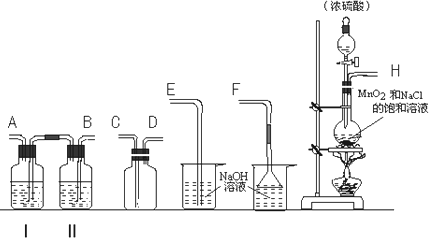
(2)写出工业上用氯气和石灰乳制取漂白粉的化学反应方程式________;
(3)实验室有一瓶密封不严的漂白粉样品,其中肯定存在CaCl2,请设计实验,探究该样品中可能存在的其它固体物质.
①提出合理假设.
假设1:该漂白粉未变质,只含________;
假设2:该漂白粉全部变质,只含________;
假设3:该漂白粉部分变质,既含有Ca(ClO)2又含有CaCO3.
②设计实验方案,进行实验.请写出实验步骤、预期现象与结论
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1 mol/L HCl、品红溶液、新制澄清石灰水.(提示:不必检验Ca2+和Cl-)

查看答案和解析>>
科目: 来源:广东省韶关市2011届高三一模理综化学试题 题型:058
| |||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:广东省肇庆市2011届高三一模理综化学试题 题型:058
某同学为了验证Fe3+是否能氧化H2SO3生成了SO42-,他
用50 mL 0.1 mol /LFeCl3溶液吸收制取SO2气体的尾气后,进行以下实验:(1)检验吸收液中的SO42-:________,证明Fe3+能够把H2SO3氧化成SO42-.
(2)请配平并完成上述反应中的
化学方程式:2FeCl3+SO2+________=________+H2SO4+________,反应中的氧化产物是________(写化学式).
(3)吸收液中除了含有H+、Cl-、SO42-以外,对其它成份(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①
提出假设.假设1:溶液中存在Fe3+、Fe2+;假设2:溶液中存在②设计方案、进行实验,验证假设.请写出实验步骤以及预期现象和结论(可不填满).限选实验试剂和仪器:试管、滴管、0.1 moL·L-1 KMnO4、0.1 moL·L-1 KSCN溶液、品红稀溶液.

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com