
科目: 来源:山东省实验中学2012届高三第一次诊断性考试化学试题 题型:058
化学实验是研究物质性质的基础.
(1)下列有关实验操作或测量数据合理的是________(填序号).
a.用铁坩埚加热CuSO4·5H2O晶体测定结晶水质量分数
b.用干燥的pH试纸测定浓硫酸的pH
c.用规格为20 mL的量筒,量取16.8 mL的Na2CO3溶液
(2)某废水样品中含有一定的Na+、CO32-、SO32-,甲、乙两研究小组欲测定其中SO32-离子的浓度.
![]()
甲组方案:
试剂X从下列试剂中选择:
a.0.1 mol·L-1 KMnO4(H2SO4酸化)溶液
b.0.5 mol·L-1 NaOH溶液
c.新制氯水d.KI溶液
①加入的试剂X为________(填字母序号),生成SO42-主要的离子方程式为________.
②甲组方案中,第ⅲ步的“系列操作”包含的操作名称各为________.
乙组方案:
ⅰ.用烧杯盛取废水适量,加少量活性炭,除去废水的杂色;过滤,取滤液;
ⅱ.精确量取20.00 mL过滤后废水试样,选择使用紫色的0.1 mol·L-1 KMnO4(H2SO4酸化)溶液进行滴定:(有关反应为:2MnO4-+5SO32-+6H+![]() 2Mn2++5SO42-+3H2O)
2Mn2++5SO42-+3H2O)
ⅲ.记录数据,计算.
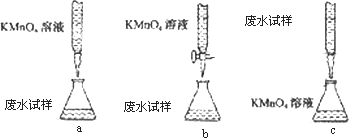
③乙组设计的下列滴定方式中,最合理的是________(夹持部分略去)(填字母序号)
(3)某同学制备Fe(OH)3胶体:用洁净烧杯量取适量蒸馏水加热至沸腾,向烧杯中缓慢滴加饱和的FeCl3溶液,并不断用玻璃棒搅拦,结果溶液变浑浊.该同学制备胶体失败的原因是________,你认为成功制得Fe(OH)3胶体的特征现象是________.
(4)用下图装置进行CO2性质的有关实验.
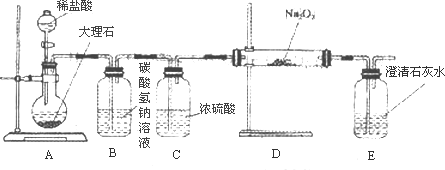
①试剂瓶B中盛有饱和NaHCO3溶液,其目的是________.
②反应过程中,E中澄清石灰水变浑浊,E中的混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系________.
查看答案和解析>>
科目: 来源:大纲版2012届高三上学期单元测试(6)化学试题 题型:058
利用下图所示装置,选用适当试剂可完成实验A、B、C并得出相应实验结论.实验A、B、C所用试剂或所得结论列于表中.

(1)实验A中,试剂①为________,②为________(写化学式);反应的离子方程式为________.
(2)实验B中,结论③为________;反应的离子方程式为________.
(3)实验C中,试剂①为________,②为________,③为________.
(4)利用该装置自行设计有机实验D.写出所用试剂:甲________,乙________,丙________;简述实验现象和结论:________;反应的化学方程式为________.
查看答案和解析>>
科目: 来源:上海市南汇中学2012届高三第一次考试化学试题 题型:058
重晶石矿的主要成分为硫酸钡,纯净的硫酸钡才能供医用作“钡餐”,在对某些内脏器官进行X射线透视时服用.硫化钡是可溶于水的盐.讨论用重晶石矿制硫酸钡,设计流程如下:
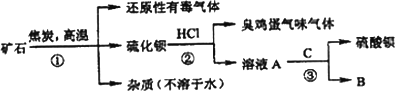
(1)写出步骤①的化学反应方程式________,该反应产生的气体具有________、________等用途.
(2)为进行②反应先要分离出硫化钡溶液,采用的方法是________.在此之前要在溶液中滴入少量Ba(OH)2溶液,其作用是________.
(3)若B物质在该生产过程中可循环使用,则③反应的化学方程式是:________.
(4)有人提出②反应产生了有臭有毒的气体,可采用改变反应物的方法使无该气体产生,则②反应的化学方程式是:________.此时若要B物质还能循环使用,则C为________(写化学式).
(5)BaSO4是因为具有________、________等性质而可用作“钡餐”的.
查看答案和解析>>
科目: 来源:上海市南汇中学2012届高三第一次考试化学试题 题型:058
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂.某课外研究小组测定该补血剂中铁元素的含量,实验步骤如下:
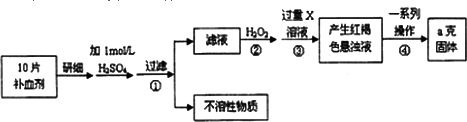
请回答下列问题:
(1)证明步骤①滤液中含有Fe2+的方法是先滴加KSCN溶液,再滴加________,该过程的现象为:________.
(2)步骤②加入过量H2O2的目的:________.
(3)步骤③中反应的离子方程式:________.
(4)步骤④中一系列处理的操作步骤:过滤、________、灼烧、________、称量.
(5)若实验无损耗,则每片补血剂含铁元素的质量________g.
(6)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定.
(5Fe2++MnO-4+8H+→5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻棒、烧杯、胶头滴管外,还需
②上述实验中的KMnO4溶液需要酸化,用于酸化的酸是________.
a.稀硝酸
b.稀硫酸
c.稀盐酸
d.浓硝酸
③滴定到终点时的颜色为________色.
(7)正常人每天应补充14 mg左右的铁.其中绝大部分来自于食物.如果全部通过服用含FeSO4·7H2O的片剂来补充铁,则正常人每天服需用含________mg FeSO4·7H2O的片剂.
查看答案和解析>>
科目: 来源:陕西省西安铁一中2011届高三第二次模拟考试化学试题 题型:058
为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题.
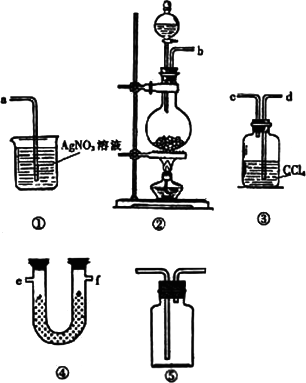
(1)请根据甲同学的意图,连接相应的装置,接口顺序:b接________,________接________,________接a.
(2)U形管中所盛试剂的化学式为________.
(3)装置③中CCl4的作用是________.
(4)乙同学认为甲同学实验中有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种.为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出在某两个装置之间再加装置⑤.你认为装置⑤应加在________之间(填装置序号).瓶中可以放入________.
(5)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液.你认为可将溶液换成________,如果观察到________的现象,则证明制Cl2时有HCl挥发出来.
查看答案和解析>>
科目: 来源:新人教版2012届高三上学期单元测试(1)化学试题 新人教版 题型:058
碳酸钠与工农业生产、日常生活紧密相关.工业碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案.请回答下列有关问题:
方案一:沉淀分析法
(1)把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀________(填操作)、洗涤、烘干、称量.洗涤沉淀的操作是________.
方案二:气体分析法
(2)把一定量的样品与足量盐酸反应后,用如图装置测定产生CO2气体的体积,为了测定结果准确,B中的溶液最好采用________,但选用该溶液后实验结果仍然不够准确,其原因是________.

方案三:质量差分析法
(3)把一定质量的样品和足量的稀硫酸反应,采用如图所示装置,通过称量反应前后盛有碱石灰的干燥管质量,利用其质量差求算样品的纯度.
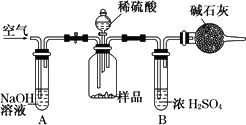
该实验的操作步骤有:
①在干燥管内填满碱石灰,质量为m g
②取n g样品装入广口瓶中
③检验装置的气密性
④缓慢鼓入空气数分钟,再称量干燥管质量为w g
⑤关闭止水夹
⑥打开止水夹
⑦缓慢加入稀硫酸至不再产生气体为止
⑧缓慢鼓入空气数分钟
Ⅰ.正确的操作顺序是(填写序号):
③→________→⑥→________→⑤→________→⑦→________→④
Ⅱ.若去掉装置A,测定结果________;若去掉装置B,测定结果________(填“偏大”、“偏小”或“无影响”).
查看答案和解析>>
科目: 来源:大纲版2012届高三上学期单元测试(3)化学试题 题型:058
回答实验室制取NH3并进行氨气性质实验的若干问题,根据要求填写空白.
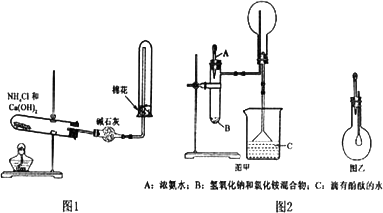
(1)实验室用图1所示装置制备干燥的NH3:
①反应的化学方程式为:________.装置中收集NH3的试管口放置棉花团的作用是:________.
②干燥管中干燥剂能否改用无水CaCl2________,理由是________.
(2)图2是某化学小组制备NH3并进行性质实验时的改进装置.按图甲把仪器安装好,称取2 g固体氯化铵装入试管底部,再快速称取2 g氢氧化钠覆盖在氯化氨上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2 mL浓氨水);烧杯内盛满有酚酞试液的水;把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡产生.
将图甲中收满NH3的圆底烧瓶取下,改装成图乙所示的装置,胶头滴管内事先吸入2 mL H2O,此时小气球系在玻璃棒上呈自然松弛状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3的某项性质.
①下面是某同学关于某化学小组能用图甲制取NH3的原因分析,有道理的是________.
a.在NH3·H2O中有平衡:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH
NH![]() +OH-,NaOH使平衡向左移动
+OH-,NaOH使平衡向左移动
b.在NH3·H2O中有平衡:NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH
NH![]() +OH-,NH4Cl使平衡向左移动
+OH-,NH4Cl使平衡向左移动
c.NaOH溶于水时放热,使体系的温度升高,NH3的溶解度减小,会有部分NH3逸出
d.NH4Cl与NaOH在此情况下可反应生成NH3,即NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
e.NH4Cl会分解释放出NH3
②图甲中的NH4Cl与NaOH固体混合物能否用CaO固体代替?________(填“能”或“不能”).
③如何判断图甲中烧瓶已收满NH3?________.
④图乙中随胶头滴管中的水挤入烧瓶中,观察到的现象是________,说明NH3________.
查看答案和解析>>
科目: 来源:大纲版2012届高三上学期单元测试(3)化学试题 题型:058
某化学课外活动小组用浓盐酸、MnO2共热制Cl2,并用Cl2和Ca(OH)2反应制少量漂白粉,现已知反应2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O,正反应为放热反应,温度稍高即发生副反应6Cl2+6Ca(OH)2=5CaCl2+Ca(ClO3)2+6H2O.甲、乙、丙三人分别设计三个实验装置,如下图所示.
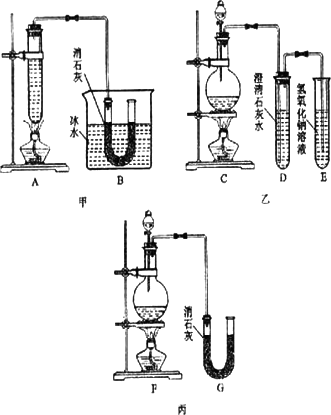
(1)请指出三个装置各处的缺点或错误(如没有可不填)
甲:________;
乙:________;
丙:________.
(2)图甲由A、B两部分组成,乙由C、D、E三部分组成,丙由F、G组成,从上述甲、乙、丙三套装置中选出合理的部分(按气流从左到右的方向)组装一套较完善的实验装置(填所选部分的编号)________.
(3)实验中若用12 mol·L-1的浓盐酸100 mL与足量的MnO2反应,最终生成Ca(ClO)2的物质的量总是小于0.15 mol,其可能的主要原因是(假定各步反应均无反应物损耗且无副反应发生)________.
查看答案和解析>>
科目: 来源:山东省兖州市2012届高三入学摸底考试化学试题 题型:058
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周期;E元素原子的最外层电子数比次外层电子数少2;A、B、D、E这四种元素,每一种与C元素都能形成原子个数比不相同的若干种化合物.请回答:
(1)C和E两种元素相比较,原子得电子能力较强的是(填元素名称)________,以下三种说法中,可以验证该结论的是(填写编号)________;
A.比较这两种元素的常见单质的沸点
B.二者形成的化合物中,C元素的原子显负价
C.比较这两种元素的气态氢化物的稳定性
(2)A、B、C、E可形成两种酸式盐(均含有该四种元素),这两种酸式盐在水溶液中相互反应的离子方程式为________.
(3)C与D形成的某种化合物可作潜水面具中的供氧剂,每生成标准状况下11.2 L O2,消耗该化合物的质量为________.
(4)B2A4是一种可燃性液体,B2A4-空气燃料电池是一种碱性燃料电池,B2A4的氧化产物为B2.用该燃料电池电解足量的饱和食盐水,如下图所示,电解装置内发生反应的离子方程式为________;
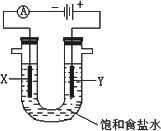
查看答案和解析>>
科目: 来源:湖北省荆州中学2012届高三第一次质量检查化学试题 题型:058
实验室制取少量溴乙烷的装置如下图所示.根据题意完成下列填空:
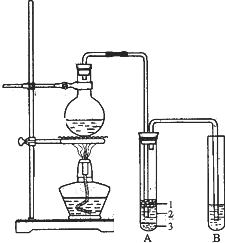
(1)圆底烧瓶中加入的反应物是溴化钠、________和1∶1的硫酸.配制体积比1∶1的硫酸所用的定量仪器为________(选填编号).
a.天平
b.量筒
c.容量瓶
d.滴定管
(2)写出加热时烧瓶中发生的主要反应的化学方程式________.
(3)将生成物导入盛有冰水混合物的试管A中,冷却、液封溴乙烷.
试管A中的物质分为三层(如图所示),产物在第________层.
(4)试管A中除了产物和水之外,还可能存在________、________(写出化学式).
(5)用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的正确方法是________(选填编号).
a.蒸馏
b.氢氧化钠溶液洗涤
c.用四氯化碳萃取
d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质的名称是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com