
科目: 来源:广西桂林十八中2012届高三第一次月考化学试题 题型:058
有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常用的无机试剂.纯E为无色油状液体;B、C、D和F是盐溶液,且他们的阴离子均不同.现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五种溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶.
根据上述实验信息,请回答下列问题:
(1)能确定溶液是(写出溶液标号与相应溶质的化学式):
_________________________.
(2)不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:
_________________________.
查看答案和解析>>
科目: 来源:山东省汶上一中2012届高三10月月考化学试题 题型:058
过碳酸钠(Na2CO4)在洗涤、印染、造纸、医药卫生等领域有大量应用.
已知:过碳酸钠与硫酸溶液反应的化学方程式如下:
Na2CO4+H2SO4→Na2SO4+H2O2+CO2↑ 2H2O2→2H2O+O2↑
为测定已变质的过碳酸钠(含碳酸钠)的纯度,设计如图所示的实验:Q为-具有良好的弹性的气球(不与反应物和生成物反应),称取一定量的样品和少量二氧化锰放于其中,按图安装好实验装置,打开分液漏斗的活塞,将稀H2SO4滴入气球中.

(1)Q内发生反应生成的气体为_________,导管a作用是_________.
(2)为测出反应时生成气体的总体积,滴稀H2SO4前必须关闭K1、K2,打开K3.当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是_________,b中装的碱石灰的作用是_________.
(3)实验结束时,量筒I中有x mL水,量筒Ⅱ中收集到y mL气体(上述体积均已折算到标准状况),则过碳酸钠的纯度是_________
(4)某同学实验测得的过碳酸钠的纯度超过100%,你认为可能的原因是_________
A.气体滞留在Q和导气管中,未全部进入量筒Ⅱ
B.量筒Ⅱ读数时,量筒液面高于水槽液面
C.右侧量筒Ⅰ和储液集气瓶连接导管内的液体没有计入读数x
D.气体体积数值x、y没有扣除滴加的硫酸的体积
查看答案和解析>>
科目: 来源:河南省开封高中2012届高三第一次定位测试化学试题 题型:058
根据要求完成下列各小题实验.(a、b为弹簧夹,加热及固定装置已略去)
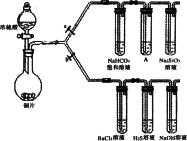
(1)验证碳、硅非金属性的相对强弱.(已知酸性:亚硫酸>碳酸)
①反应原理:铜与浓硫酸反应的化学方程式是________.
②实验步骤:连接仪器、________、加药品后,打开a关闭b,然后滴人浓硫酸,加热.
③试剂选择:装置A中试剂是________.
④结论:能说明碳的非金属性比硅强的实验现象是________.
(2)验证SO2的氧化性、还原性和酸性氧化物的通性.
①在(1)②操作后打开b,关闭a.
②H2S溶液中有浅黄色浑浊出现,化学方程式是________.
③BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置.
写出其中SO2显示还原性生成沉淀的离子方程式________.
查看答案和解析>>
科目: 来源:山东省诸城市2012届高三10月月考化学试题 题型:058
下表是实验室制备气体的有关内容:
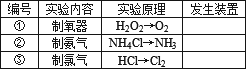
(1)上述气体中,从反应中有无电子转移的角度看,明显不同于其他气体的是________,写出实验室制取该气体的化学方程式________.
(2)根据表中所列实验原理,从下列装置中选择合适的发生装置,将其编号填入下表的空格中.
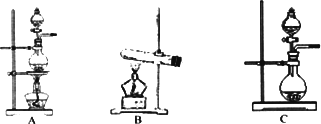
(3)若用上述制备O2的装置制备NH3,应选择的试剂为________.
(4)在浓CaCl2溶液中通人NH3和CO2可以制得纳米级碳酸钙,制取时应先通入的气体是________,制取纳米级碳酸钙的化学方程式为________.试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级________.
(5)制备Cl2需用8 mol·L-1的盐酸100 mL,现用12 mol·L-1的盐酸来配制.
①需要用量筒量取12 mol·L-1的盐酸的体积为________mL;
②实验室提供有如下仪器,为完成配制需要选择的仪器为(填序号)
A.100 mL量筒
B.托盘天平
C.玻璃棒
D.50 mL容量瓶
E.10 mL量筒
F.胶头滴管
G.100 mL烧杯
H.100 mL容量瓶
③下列实验操作中.不正确的是________(填写标号).
A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加人蒸馏水到距离刻度线1~2 cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次
查看答案和解析>>
科目: 来源:内蒙古包头三十三中2012届高三上学期期中考试化学试题 题型:058
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用品、用下图中的实验装置进行实验,证明过氧化钠可作供氧剂.
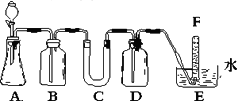
(1)A是制取CO2的装置.写出A中发生反应的化学方程式:________.
(2)填写表中空格:
(3)写出过氧化钠与二氧化碳反应的化学方程式:________.
(4)试管F中收集满气体后,下一步实验操作是:________.
查看答案和解析>>
科目: 来源:辽宁省抚顺二中2012届高三第一次月考化学试题 题型:058
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定某含镁3%-5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究.填写下列空白.
[探究一]
实验方案:铝镁合金![]() 测定剩余固体质量
测定剩余固体质量
实验中发生反应的化学方程式是________
实验步骤:
(1)称取5.4 g铝镁合金粉末样品,投入V mL 2.0mol·L-1 NaOH溶液中,充分反应.NaOH溶液的体积V≥________.
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将________(填“偏高”或“偏低”)
[探究二]
实验方案:铝镁合金![]() 测定生成气体的体积实验装置:
测定生成气体的体积实验装置:
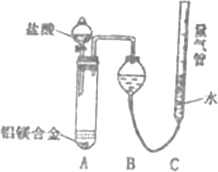
问题讨论:
(1)某同学提出该实验装置不够完善,应在A、B之间添加一个干燥,除酸雾的装置.你的意见是:________(填“需要”或“不需要”)
(2)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):
①________②________
[探究三]
实验方案:称量x g铝镁合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧.
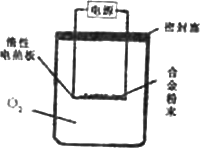
问题讨论:
(1)欲计算Mg的质量分数,该实验中还需测定的数据是________
(2)若用空气代替O2进行实验,对测定结果何影响?________(填“偏高”或“偏低”或“无影响”)
查看答案和解析>>
科目: 来源:江苏省南京市金陵中学2011届高三第四次模拟考试化学试题 题型:058
纳米材料二氧化钛(TiO2)可做优良的催化剂.

Ⅰ.工业上二氧化钛的制备方法:
①将干燥后的金红石(主要成分为TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4.
②将SiCl4分离,得到纯净的TiCl4.
③在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O.
④TiO2·xH2O高温分解得到TiO2.
(1)根据资料卡片中信息判断,TiCl4与SiCl4在常温下的状态是_________,分离二者所采取的操作名称是_________.
(2)③中反应的化学方程式是_________.
(3)若④在实验室完成,应将TiO2·xH2O放在_________(填仪器名称)中加热.
Ⅱ.据报道:能“吃废气”的“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:
a.O2→2O
b.O+H2O→2OH
c.OH+OH→H2O2
(4)b中破坏的是_________(填“极性共价键”或“非极性共价键”).
(5)H2O2能清除路面空气中的CxHy、CO等,主要是利用了H2O2的_________(填“氧化性”或“还原性”).

Ⅲ.某研究性学习小组用下列装置模拟“生态马路”清除CO的原理.(夹持装置已略去)
(6)若缓慢通入22.4 L(已折算成标准状况)CO气体,结果NaOH溶液增重16.5 g,则CO的转化率为_________.
(7)当CO气体全部通入后,还要通一会儿空气,其目的是_________.
查看答案和解析>>
科目: 来源:福建省师大附中2012届高三上学期期中考试化学试题(人教版) 人教版 题型:058
某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体[FeSO4·7H2O]和胆矾晶体,以探索工业废料的再利用.其实验方案如下:
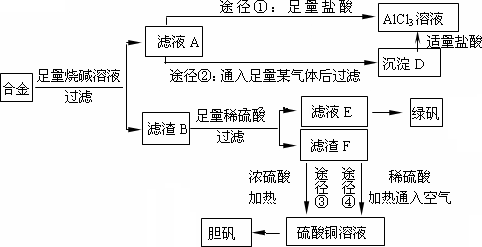
回答下列问题:
(1)写出合金与烧碱溶液反应的离子方程式________.
(2)由滤液A制AlCl3溶液的途径有①和②两种,你认为合理的是________.上述实验方案多处采用了过滤操作,过滤所用到的玻璃仪器有________和玻璃棒;其中玻璃棒的作用是________.
(3)用滤渣F通过两种途径制取胆矾,与途径③相比,途径④明显具有的两个优点是________、________.
(4)通过途径④制取胆矾,必须进行的实验操作步骤:加硫酸、加热通氧气、过滤、________、冷却结晶、________、自然干燥.其中“加热通氧气”所起的作用为________(用离子方程式表示).
(5)测定所得胆矾(CuSO4·xH2O)中x值的实验方案是蒸发硫酸铜晶体中的水得到白色的无水硫酸铜,冷却后称量.此变化的化学方程式为:CuSO4·xH2O![]() CuSO4+xH2O,但温度过高,CuSO4会继续分解为CuO和SO3.在此实验过程中,称量操作至少进行________次.若测定结果x值偏高,可能的原因是________.
CuSO4+xH2O,但温度过高,CuSO4会继续分解为CuO和SO3.在此实验过程中,称量操作至少进行________次.若测定结果x值偏高,可能的原因是________.
a.加热温度过高
b.加热时胆矾晶体飞溅出来
c.加热后放在空气中冷却
d.所用坩埚事先未干燥(潮湿)
查看答案和解析>>
科目: 来源:河北省衡水中学2012届高三第三次调研考试化学试题(人教版) 人教版 题型:058
黄铁矿是我国大多数硫酸厂制取硫酸的主要原料.某化学兴趣小组对某黄铁矿石(主要成分为FeS2)进行如下实验探究.
[实验一]:测定硫元素的含量
Ⅰ.将m1g该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通人空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体.
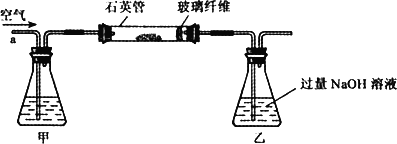
写出石英管中发生反应的化学方程式为:________.
Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:
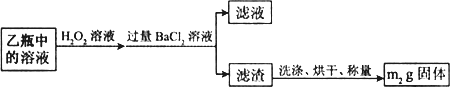
问题讨论:
(1)Ⅰ中,甲瓶内所盛试剂是________溶液.乙瓶内发生反应的离子方程式有________、________.
(2)Ⅱ中,所加H2O2溶液需足量的理由是________.
(3)该黄铁矿石中硫元素的质量分数为________.
[实验二]:设计以下实验方案测定铁元素的含量

问题讨论:
(4)②中,若选用铁粉作还原剂.你认为合理吗?________.
若不合理,会如何影响测量结果:________(若合理,此空不答).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有________.
(6)④中发生反应的离子方程式为________.
查看答案和解析>>
科目: 来源:江苏省南通市通州区2012届高三重点热点专项检测化学试题 题型:058
某化学兴趣小组设计以下实验步骤与操作来定性检验茶叶中含有的少量钙、铁、铝三种元素.
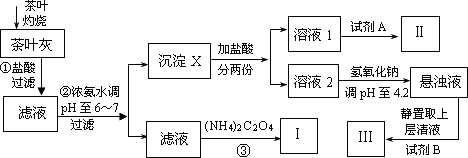
已知Ca2+、Al3+、Fe3+完全形成相应氢氧化物沉淀的pH如下表:
(1)步骤①中加入盐酸的作用是________.
(2)步骤②中调节pH至6~7的目的是________.
(3)沉淀X所含主要物质的化学式为________.
(4)写出步骤③中发生反应的离子方程式:________.
(5)试剂A为________;试剂B为铝试剂,加入该试剂后的实验现象是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com