
科目: 来源: 题型:填空题
O2和O3是氧元素的两种单质,根据其分子组成或性质完成下列各题:
(1)臭氧发生器将氧气转化为臭氧的反应属于 变化;
(2)等物质的量的O2和O3所含分子个数比为 ,它们的质量之比为 ;
(3)等温等压下,等体积的O2和O3所含分子个数比为 ;
(4)O3与KI溶液反应生成的两种单质分别是 和 (填分子式);
(5)设NA为阿伏加德罗常数的数值,如果Ag氧气中含有的分子数为b,则c g臭氧在标准状况下的体积约是 (用含NA、a、b、c的式子表示)。
查看答案和解析>>
科目: 来源: 题型:填空题
把一只表面被氧化成10.2 g氧化铝的铝条A,放入1 L 1.5 mol/L的热氢氧化钠溶液中,过一段时间后取出铝条,溶液质量增加12.6克,此溶液称为甲溶液,体积仍为1 L,再把另一只表面也氧化成一定量的氧化铝的铝条B,放入1 L 0.9 mol/L的硫酸溶液中,,过一段时间取出,其质量减少25.8克,溶液质量增加25.2克,此溶液称为乙溶液,体积仍为1 L,回答下列问题:
(1)甲溶液溶质是 (写化学式),其物质的量是 ;
(2)乙溶液的溶质 (写化学式),其物质的量是 ;
(3)将甲乙两溶液反应,若使滴加的量最小,产生沉淀最多,应将 溶液 (填甲、乙)L 滴加到 溶液中(填甲、乙)。
查看答案和解析>>
科目: 来源: 题型:填空题
(1)实验室用氯化铵固体制取氨气的化学方程式是 。
(2)将4.48L(标准状况)氨气通入水中得到0.05L溶液,所得溶液的物质的量浓度是 。
(3)现有100mL AlCl3与MgSO4的混合溶液,分成两等份。
①向其中一份中加入10mL 4mol/L的氨水,恰好完全反应,其中AlCl3与氨水反应的离子方程式是 。继续加入l mol/L NaOH溶液至10mL时,沉淀不再减少,沉淀减少的离子方程式是 ,减少的沉淀的物质的量是 。
②向另一份中加入a mL 1mol/LBaCl2溶液能使SO42-沉淀完全,a= 。
查看答案和解析>>
科目: 来源: 题型:填空题
(1)下列物质中水溶液能导电但属于非电解质的有 (填序号)①乙醇 ②氨气 ③氯气 ④氯化钠 ⑤硫酸 ⑥干冰 ⑦BaSO4 ⑧醋酸 ⑨氢氧化钠 ⑩CaO
(2)某实验需要使用240ml 0.4mol/L CuSO4溶液,用胆矾配制该浓度溶液需要使用的仪器有托盘天平、烧杯、玻璃棒、 、 ;需要称量 克胆矾;若所称胆矾失去部分结晶水,则配制出的溶液浓度 。(填偏高、偏低或无影响)
(3)汉紫是中国古代兵马俑和古代壁画中的一种颜料,其化学式是BaCuSi2O6,请用氧化物的形式表示其组成: 。
查看答案和解析>>
科目: 来源: 题型:填空题
铜及其合金是人类最早使用的金属材料。
(1)金属铜采取下列哪种方式堆积( )

(2)在1个Cu2O晶胞中(结构如上图所示),Cu原子配位数为__________。
(3)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下:
①胆矾的化学式用配合物的形式表示为____________。
②胆矾中SO42—的空间构型为________,H2O中O原子的杂化类型为________。
③某兴趣小组称取2.500 g胆矾晶体,逐渐升温使其失水,并准确测定不同温度下剩余固体的质量,得到如图所示的实验结果示意图。下列说法正确的是( )
| A.晶体从常温升到105 ℃的过程中只有氢键断裂 |
| B.胆矾晶体中形成配位键的4个水分子同时失去 |
| C.120 ℃时,剩余固体的化学式是CuSO4·H2O |
| D.按胆矾晶体失水时所克服的作用力大小不同,晶体中的水分子可以分为3种 |
查看答案和解析>>
科目: 来源: 题型:填空题
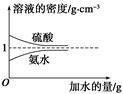
已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| | 溶质的物质的量 浓度/mol·L-1 | 溶液的密度/g·cm-3 |
| 硫酸 | c1 | ρ1 |
| 氨水 | c2 | ρ2 |
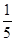 c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________
c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________ 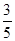 c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
c2 mol·L-1(设混合后溶液的体积变化忽略不计)。查看答案和解析>>
科目: 来源: 题型:填空题
盐泥是氯碱工业中的废渣,主要成分是镁的硅酸盐和碳酸盐(含少量铁、铝、钙的盐)。实验室以盐泥为原料制取MgSO4·7H2O的实验过程如下:
①水,调成泥浆②稀硫酸调pH为1~2③煮沸④过滤―→―→产品
已知:①室温下Ksp[Mg(OH)2]=6.0×10-12。②在溶液中,Fe2+、Fe3+、Al3+从开始沉淀到沉淀完全的pH范围依次为7.1~9.6、2.0~3.7、3.1~4.7。③三种化合物的溶解度(S)随温度变化的曲线如图所示。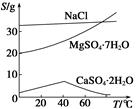
(1)在盐泥中加入稀硫酸调pH为1~2以及煮沸的目的是_____________________。
(2)若室温下的溶液中Mg2+的浓度为6.0 mol·L-1,则溶液pH≥________才可能产生Mg(OH)2沉淀。
(3)由滤液Ⅰ到滤液Ⅱ需先加入NaClO调溶液pH约为5,再趁热过滤,则趁热过滤的目的是__________________,滤渣的主要成分是______________________。
(4)从滤液Ⅱ中获得MgSO4·7H2O晶体的实验步骤依次为①向滤液Ⅱ中加入______________;②过滤,得沉淀;③________________;④蒸发浓缩,降温结晶;⑤过滤、洗涤得产品。
(5)若获得的MgSO4·7H2O的质量为24.6 g,则该盐泥中镁[以Mg(OH)2计]的百分含量约为________(MgSO4·7H2O的相对分子质量为246)。
查看答案和解析>>
科目: 来源: 题型:填空题
标准状况下336 L的NH3溶于1 L水中,所得溶液的质量分数为________,若该溶液的密度为a g/cm3,则物质的量浓度为________。将上述氨水全部转化为NH4Cl,所需4 mol·L-1的盐酸的体积为________。
查看答案和解析>>
科目: 来源: 题型:填空题
2014年全运会在辽宁举办,其开幕式就是一场焰火盛宴。
(1)焰火利用了部分金属元素特征的 反应,该反应属于 (填“物理”或“化学”)变化。
(2)如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素组成,每种化合物仅含两种元素。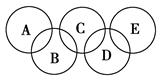
图中A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E分子结构的球棍模型为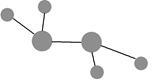 ,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3∶4,电子总数之比为3∶2。根据以上信息回答下列问题:
,C与纯碱在高温下的反应是工业制玻璃的主要反应之一,D中所含两种元素的原子个数比为3∶4,电子总数之比为3∶2。根据以上信息回答下列问题:
①B的水溶液呈弱酸性,其主要的电离方程式可表示为 ,D的化学式是 。
②A、B、E中均含有的一种元素符号为 。
③C与纯碱反应的化学方程式为 。
④液态B与液态E反应可生成一种单质和一种常见液体,1 mol B参加反应放出热量Q kJ,其反应的热化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:填空题
工业上用含锌物料(含FeO、CuO等杂质)可制得活性ZnO,流程如下: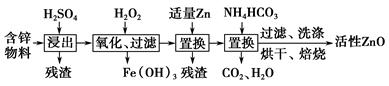
(1)上述流程中,浸出用的是60%H2SO4(1.5 g·cm-3),配制这种H2SO4 100 mL需要18.4 mol·L-1的浓H2SO4________ mL(保留一位小数)。
(2)加入氧化剂H2O2后,有Fe(OH)3沉淀出现,没有Cu(OH)2沉淀出现,若溶液中c(Fe3+)=2.6×10-18 mol·L-1,则溶液中c(Cu2+)的取值范围是________mol·L-1。(已知Ksp[Fe(OH)3]=2.6×10-39,
Ksp[Cu(OH)2]=2.2×10-20)
(3)加入NH4HCO3后生成的沉淀是形态均为Zna(OH)b(CO3)c(a、b、c为正整数)的两种碱式碳酸锌A和B的混合物,A中a=5、b=6,则生成碱式碳酸锌A的化学方程式为__________________________________________________。
(4)取洗涤、烘干后的碱式碳酸锌A和B的混合物49.70 g,其物质的量为0.10 mol,高温焙烧完全分解得到37.26 g ZnO、3.584 L CO2(标准状况下)和水,通过计算求出碱式碳酸锌B的化学式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com