
科目: 来源: 题型:填空题
某种物质溶于水后得到的溶液中,含有Fe2+、Fe3+、SO42-、NH4+、Ba2+、CO32-离子中的某几种。
(1)甲同学欲探究溶液的组成,进行了如下实验:①取少量溶液于试管中,逐滴加入浓氢氧化钠溶液,发现开始生成白色沉淀,白色沉淀迅速变为灰绿色,最后变为红褐色,同时伴有刺激性气体放出;②另取少量溶液于试管中,加入足量盐酸酸化后再滴加氯化钡溶液,有白色沉淀生成。
该溶液中一定含有的离子是 ;
写出①中白色沉淀转化为红褐色沉淀的化学方程式 。
(2)乙同学进行如下实验:取少量溶液于试管中,滴加几滴硫氰酸钾溶液,无明显现象;再滴加H2O2,发现溶液变红色;继续滴加H2O2,红色逐渐褪去且有气泡产生。为弄清其中缘由,乙同学查阅资料知:
H2O2+SCN-→SO42-+CO2↑+N2↑+H2O+H+
①该反应中,被氧化的元素为 ,每生成lmol CO2转移的电子数为 NA;
②根据乙同学的实验现象,请判断还原性强弱为:Fe2+ SCN-(填<、=或>);
③根据资料,乙同学提出的猜想是:H2O2将SCN-氧化使红色逐渐褪去。请你设计一个实验,验证乙同学的猜想是否正确 。
查看答案和解析>>
科目: 来源: 题型:填空题
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Ca2+、Ba2+、CO32-、SO42-. 现取三份各100mL溶液进行如下实验:
第一份加入AgNO3溶液有沉淀产生;
第二份加入足量NaOH溶液加热后,收集到0.08mol气体;
第三份加入足量BaCl2 溶液后,得到干燥沉淀12.54g,经足量的盐酸洗涤、干燥后,沉淀质量为4.66g。
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl- : ,原因是 .
(2)由第二份进行的实验可知混合物中应含有 离子,其物质的量浓度为 .
(3)由第三份进行的实验可知12.54g 沉淀的成份为 。请计算形成该沉淀的原混合物中各离子的物质的量。(要求计算过程)
(4)综合上述实验,你认为以下结论正确的是
| A.该混合物中一定含有K+、NH4+、CO32-、SO42-,可能含有Cl-,且n(K+)≥0.04mol |
| B.该混合物中一定含有NH4+、CO32-、SO42-,可能含有Ca2+、 K+、Cl- |
| C.该混合物中一定含有NH4+、CO32-、SO42-,可能含有K+、Cl- |
| D.该混合物中一定含有NH4+、SO42-,可能含有Ca2+、K+、Cl- |
查看答案和解析>>
科目: 来源: 题型:填空题
有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种物质中的一种或几种。现进行如下实验:
(1)取少量固体粉末加到足量水中,得到白色沉淀,上层为无色清液。
(2)继续往其中加入足量稀硝酸,白色沉淀完全消失,并有气泡产生。
(3)取少量⑵中的溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶。
根据上述实验现象判断:该白色固体中一定含有__________________,一定不含有________,可能含有_____________。
如何验证可能存在的物质
查看答案和解析>>
科目: 来源: 题型:填空题
按要求准确表达下列变化过程中的化学用语,其中(1)~(3)写化学方程式,(4)~(5)写离子方程式。
(1)铁丝在氯气中燃烧 。 (2)能体现SO2氧化性 。
(3)镁在二氧化碳中燃烧 。(4)NaOH溶液与NaHCO3溶液反应 。
(5)用氯化铁溶液刻画电路板 。
查看答案和解析>>
科目: 来源: 题型:填空题
含铬化合物有毒,对人畜危害很大。因此含铬废水必须进行处理才能排放。
已知: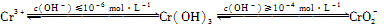
(1)在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去。
①写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式:________________。
②用离子方程式表示溶液pH不能超过10的原因:____。
(2)将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。
①写出阴极的电极反应式:________________。
②电解法中加入氯化钠的作用是________________。
(3)铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。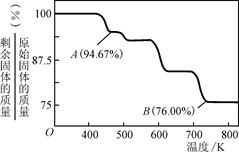
①CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为____。
②CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如右图所示,则B点时剩余固体的成分是________________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:填空题
某研究小组用黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2气体,再用水吸收该气体可得ClO2溶液。在此过程中需要控制适宜的温度,若温度不当,副反应增加,影响生成ClO2气体的纯度,且会影响ClO2的吸收率,具体情况如图所示。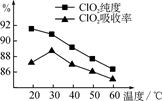
(1) 据图可知,反应时需要控制的适宜温度是________℃,要达到此要求需要采取的措施是______________。
(2) 已知:黄铁矿中的硫元素在酸性条件下可被ClO3-氧化成SO42-,请写出FeS2、氯酸钠和硫酸溶液混合反应生成二氧化氯(ClO2)的离子方程式:______________________。
(3) 该小组拟以“m(ClO2)/m(NaClO3)”作为衡量ClO2产率的指标。若取NaClO3样品6.0 g,通过反应和吸收获得400 mL ClO2溶液,取此溶液20 mL与37.00 mL 0.500 mol·L-1 (NH4)2Fe(SO4)2溶液充分反应后,过量的Fe2+再用0.050 0 mol·L-1 K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7标准溶液20.00 mL。反应原理为:
4H++ClO2+5Fe2+=Cl-+5Fe3++2H2O
14H++Cr2O72-+6Fe2+=2Cr3++6Fe3++7H2O
试计算ClO2的“产率”(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:填空题
有一瓶无色澄清的溶液,其中可能含NH4+、K+、Na+、Mg2+、H+、Cu2+、CO32-、I-中的一种或几种,取该溶液进行如下实验:
①用PH试纸检验,表明溶液呈强酸性
②取部分溶液,加入少量的CCl4及数滴新制的氯水,振荡后CCl4层显紫红色
③另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成
④将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定并回答:
(1)在溶液中,肯定存在的有___________,肯定不存在的离子有__________________。
(2)写出实验④中的离子反应方程式 ,
(3)不能确定是否存在的离子有__________________________。请设计简单实验方案证明它(们)是否存在(写出实验方法、现象、结论)__________ _________。
查看答案和解析>>
科目: 来源: 题型:填空题
⑴按要求写出下列反应的离子方程式
①氢氧化铜溶于盐酸
②碳酸钠溶液中和足量的盐酸溶液混合
(2)现有以下物质:①NaCl晶体 ②液态HCl ③CaCO3固体 ④熔融KCl ⑤蔗糖⑥铜⑦CO2⑧H2SO4⑨KOH固体 ⑩水⑾盐酸⑿CH3COOH ⒀酒精(填序号)
①以上物质中能导电的是_________________________________。
②以上物质中属于电解质的是_____________________________。
③以上物质中属于非电解质的是___________________________。
查看答案和解析>>
科目: 来源: 题型:填空题
某混合溶液中可能大量含有的离子如下表所示:
| 阳离子 | H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 | Cl-、Br-、OH-、CO32-、AlO2- |
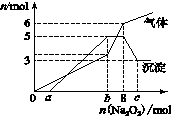
查看答案和解析>>
科目: 来源: 题型:填空题
某溶液中的溶质由下列中的几种离子构成:Na+、Fe3+、Cu2+、Ba2+、AlO2—、CO32—、SO32—、SO42—。取该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH) 2溶液,得到白色沉淀丙、气体丙和溶液丙。
④检验气体甲、气体乙、气体丙,都只含有一种成份,而且各不相同。
请回答下列问题:
(1)只根据实验①能得出的结论是 (3分)
(2)沉淀丙中一定含有 (1分),可能含有 (1分)
(3)该溶液中肯定存在的离子有
(4)气体乙分子的结构式为
(5)向溶液甲中加入NH4HCO3溶液至过量,该过程中可能发生反应的离子方程式为 ; ; (根据需要,可不填完,也可补充)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com