
科目: 来源: 题型:填空题
下图是氮元素的各种价态与物质类别的对应关系: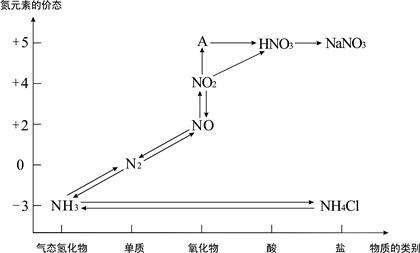
(1)根据A对应的化合价和物质类别,A的摩尔质量是 ,从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的化合物有 。
(2)实验室依据复分解反应原理制取NH3的化学方程式是 。
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应使 。
(4)汽车尾气中含有CO和NOx等多种有害气体,若在汽车的排气管上安装一种催化转化装置,可使CO与NOx反应,生成两种无毒气体,则该反应的化学方程式为 。
(5)合成法制硝酸是以NH3为原料,经催化氧化后再用水吸收来实现的,若开始时投入17吨NH3,最后生产出的硝酸为42吨,则硝酸的产率是 。
查看答案和解析>>
科目: 来源: 题型:填空题
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
(1)若A是一种黄色单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 ,试用化学方程式表示该物质与二氧化碳气体的反应 。将C长期露置于空气中,最后将变成物质D,D的化学式为 。现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38 g,D的质量分数为 。
(3)若C是红棕色气体,A可能是一种能使湿润的红色石蕊试纸变蓝的气体。下图是实验室制取A气体的装置,请结合所学知识,回答下列问题:
①收集A的方法是 ,验证A是否已经收集满的方法是 (任写一种)。
②写出实验室制取A的化学方程式 。
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为 L。
④试写出C与水反应的化学方程式 ,反应可得到酸X,X是 电解质(填“强”或“弱”)。如下图:足量X的浓溶液与Cu反应,写出烧瓶中发生反应的离子方程式 。实验完毕后,试管中收集到的气体的主要成分为 (写化学式)。
查看答案和解析>>
科目: 来源: 题型:填空题
(1)将复杂硅酸盐改写成氧化物形式:KAlSi3O8:________________。
(2)有一包白色粉末可能由K2SO4、NaHCO3、BaCl2、FeCl3、KCl五种物质中的某几种组成,现进行如下实验:
①将白色粉末加水溶解,得无色溶液。
②向①中所得的无色溶液中加入NaOH溶液,观察到有白色沉淀A生成,过滤后,向滤液中滴加硝酸酸化的AgNO3溶液,又得到白色沉淀B。
根据上述现象判断:
①A的化学式是 B的化学式是 。
②原白色粉末中一定含有 ,可能含有 ,对可能含有的物质,可通过 (填实验名称)进一步检验。检验操作步骤有:①蘸取待测液②置于酒精灯火焰上灼烧 ③透过蓝色钴玻璃观察 ④用稀盐酸洗净铂丝。其中正确的操作顺序为 。
A.①②③④ B.④①②③ C.④②①②③④ D.①③②④
查看答案和解析>>
科目: 来源: 题型:填空题
已知A、B、C、D、E、F是含有同一种元素的化合物,其中F能使红色湿润石蕊试纸变蓝色,它们之间能发生如下反应:
① A+H2O → B+C ② C+F → D ③ D+NaOH → F+E+H2O
(1)写出它们的化学式:D_______________,F_______________。
(2)写出①反应的化学方程式:_______________________________
(3)写出反应③的离子方程式:___________________________。
(4)工业生产C的过程中有如下一步反应:即F经催化氧化生成B和H2O,写出该步反应的化学方程式:________________________________。
查看答案和解析>>
科目: 来源: 题型:填空题
硝酸铵是一种常用的化肥,其工业生产流程如下图,请回答下列问题。
⑴写出反应容器B中发生反应的化学方程式: 。
⑵吸收塔C中通入空气的目的是 ;C、D两个反应容器中发生的反应,属于氧化还原反应的是 (填反应容器代号)。
⑶浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因: 。
⑷金属铜与稀硝酸反应的离子方程式是 ,该反应中稀硝酸表现的性质是 。
查看答案和解析>>
科目: 来源: 题型:填空题
硝酸铵是含氮量较高的化肥,生产流程如下(产物水均已略去):
(1)反应④的化学方程式为3NO2+H2O = 2HNO3+NO,该反应的氧化剂为__________,还原剂为__________。
(2)补充并配平反应②的化学方程式:____NH3 +___O2 ____NO+ ________
____NO+ ________
(3)化学反应_______(填序号)是非氧化还原反应,离子方程式为_________________
(4)有人设计了一个反应来制备硝酸NO2+NH3 — HNO3+H2O(未配平),你认为该反应 (填“能”或“不能”)发生,理由是______________________。
查看答案和解析>>
科目: 来源: 题型:填空题
三大强酸的性质均与浓度有关。回答下列问题:
(1)某学习小组用15 mol/L浓硝酸配制100 mL3 mol/L稀硝酸。
①他们需要用量筒量取15 mol/L浓硝酸_______mL;
②如下图所示仪器,在配制过程中不需用的是_________(填序号)。
除图中已有的仪器外,配制上述溶液还需用到的玻璃仪器是___________;
③下列实验操作中,不正确的是_________(填写标号)。
| A.使用容量瓶前,检查它是否漏水。 |
| B.定容时液面超过刻度线,多出的液体应用胶头滴管吸出。 |
| C.配制溶液时,用量筒量取浓硝酸直接倒入容量瓶中,然后加蒸馏水定容。 |
| D.定容后盖好瓶塞,把容量瓶反复上下颠倒,摇匀。 |
查看答案和解析>>
科目: 来源: 题型:填空题
在半导体工业中有这样一句话:“从沙滩到用户”,其中由粗硅制纯硅的常用方法为:Si(粗)+2Cl2=SiCl4 SiCl4+2H2=Si(纯)+4HCl。若在25℃101KPa条件下反应生成HCl气体49L(注:25℃101KPa条件下气体摩尔体积为24.5L/mol)则:
(1)反应生成HCl气体的质量为__________,转移电子的个数为_____________。
(2)反应生成的HCl气体溶于127mL水中,得到密度为1.20g/mL的盐酸,此盐酸的物质的量浓度为 。
(3)“从沙滩到用户”涉及到多个反应,其中制取粗硅的反应方程式为 ,纯净的石英砂与烧碱反应可以制得水玻璃,反应的离子方程式为 。
(4)普通玻璃若以氧化物形式表示其组成为(质量分数):Na2O 13%,CaO 11.7%,SiO2 75.3%。现以石灰石、纯碱和石英为原料生产这种玻璃10t,石灰石的利用率为80%,纯碱和石英的利用率为95%,至少需要上述原料的质量是 t(保留两位小数)。
查看答案和解析>>
科目: 来源: 题型:填空题
NOx是汽车尾气中的主要污染物之一。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:_________________________________________________________。
(2)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下: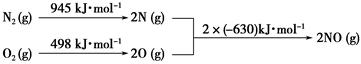
①写出该反应的热化学方程式:_______________________________________。
②随温度升高,该反应化学平衡常数的变化趋势是____。
(3)在汽车尾气系统中装置催化转化器,可有效降低NOx的排放。
①当尾气中空气不足时,NOx在催化转化器中被还原成N2排出。写出NO被CO还原的化学方程式:____________________________________。
②当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐。其吸收能力顺序如下:12MgO<20CaO<38SrO<56BaO。原因是_____________________________________________,
元素的金属性逐渐增强,金属氧化物对NOx的吸收能力逐渐增强。
(4)通过NOx传感器可监测NOx的含量,其工作原理示意图如下: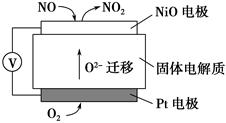
①Pt电极上发生的是________反应(填“氧化”或“还原”)
②写出NiO电极的电极反应式:_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com