
科目: 来源:湖北省期中题 题型:单选题
查看答案和解析>>
科目: 来源:湖北省期中题 题型:填空题
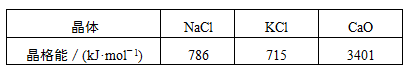
 到低的顺序是
到低的顺序是 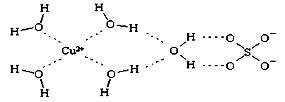
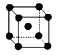

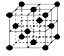
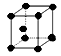
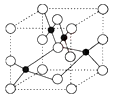
查看答案和解析>>
科目: 来源:辽宁省模拟题 题型:填空题

查看答案和解析>>
科目: 来源:吉林省期中题 题型:单选题
查看答案和解析>>
科目: 来源:期中题 题型:单选题
查看答案和解析>>
科目: 来源:期中题 题型:单选题
查看答案和解析>>
科目: 来源:模拟题 题型:填空题
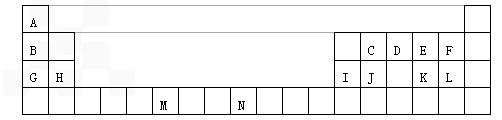
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.元素的价电子数总等于所在族的族序数 |
| B.NaOH晶体中阳离子和阴离子数目相等 |
| C.CsCl晶体中每个Cs+周围紧邻的Cl-和每个Cl-周围紧邻的Cs+个数相等 |
| D.[Co(NH3)6]3+中的N原子数与配位键数相等 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| B.[Cu(NH3)4]2+的空间构型为正四面体型 |
| C.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+ |
| D.在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com