
科目: 来源:不详 题型:单选题
 +O2↑。下列对此反应的说法中,不正确的是( )
+O2↑。下列对此反应的说法中,不正确的是( )| A.方框中的物质为Na2SO4 |
| B.Na2O2既是氧化剂,又是还原剂 |
| C.Na2FeO4既是氧化产物,又是还原产物 |
| D.2 mol FeSO4发生反应时,反应中共转移8 mol电子 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.阳离子只有氧化性,阴离子只有还原性 |
| B.含氧酸可作氧化剂而无氧酸不能 |
| C.在8NH3+3Cl2=N2+6NH4Cl反应中氧化剂与还原剂物质的量之比是2∶3 |
| D.已知还原性:Fe2+>Br-,可知反应2Fe3++2Br-=2Fe2++Br2不易进行 |
查看答案和解析>>
科目: 来源:不详 题型:单选题

 +2FeS+SO2(已配平),则下列关于该反应的说法错误的是( )。
+2FeS+SO2(已配平),则下列关于该反应的说法错误的是( )。| A.方框中的物质应为CuS |
| B.该反应的部分产物可用于硫酸工业 |
| C.反应中SO2既是氧化产物又是还原产物 |
| D.反应中若有1 mol SO2生成,则一定有4 mol电子发生转移 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.+6 | B.+3 | C.+2 | D.0 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.反应后溶液中c(NO3-)=0.85 mol·L-1 |
| B.反应后的溶液最多还能溶解1.82 g Fe |
| C.反应前HNO3溶液的浓度为1.0 mol·L-1 |
| D.1.12 L气体是NO、NO2的混合气体 |
查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
科目: 来源:不详 题型:填空题
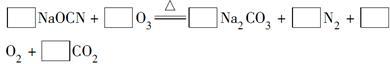
查看答案和解析>>
科目: 来源:不详 题型:填空题

 CH3OH(g)+H2O(g) ΔH。
CH3OH(g)+H2O(g) ΔH。查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.反应中消耗的Zn的质量为97.5 g |
| B.气体A中SO2和H2的体积比为1∶4 |
| C.反应中被还原的元素只有一种 |
| D.反应中共转移电子3 mol |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.0.15 mol/L | B.0.225 mol/L |
| C.0.30 mol/L | D.0.45 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com