
1.小明用如图所示装置进行“微粒是不断运动”的探究。一段时间后,可观察到紫色石蕊溶液变红,则物质A是( )
A.浓氨水 B.浓盐酸 C.浓硫酸 D.浓食盐水

2.在一只盛有稀硫酸的烧杯中漂浮着一块木块(右图)往烧杯中加入少量的某种固体物质后,木块浸没在液体中的体积变大(假设这些过程中溶液的体积变化忽略不计),则加入的固体物质可能是(
)

A.Ba(NO3)2 B.Fe C.Ba(OH)2 D.CuO
3.浓盐酸长时间的暴露在空气中,发生的变化是( )
A.溶液质量变大 B.溶液的酸性增强
C.溶质质量分数变小 D.溶液的pH变小
4.下列各组物质中,俗名、化学名称和化学式表示的是同一种物质的是:( )
A.烧碱、氧化钠 、Na2O B.纯碱、氢氧化钠、NaOH、
C.石灰石、碳酸钙、CaCO3 D.熟石灰、氧化钙、CaO
5.下列物质中都 含有水蒸气,既能用浓硫酸干燥,又能用氢氧化钠干燥固体的是 (
)
含有水蒸气,既能用浓硫酸干燥,又能用氢氧化钠干燥固体的是 (
)
A.SO2 B.HCl C.H2 D.CO2
6.下列离子能在pH=2的无色溶液中大量共存的是( )
A.SO42-、Fe3+、Na+、OH- B.K+、SO42-、Cu2+、NO3-
C.Cl-、K+、SO42-、Na+ D.Ca2+、Cl-、CO32-、Na+
7.如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一段时间后可见到小气球a膨胀鼓起。下表中的各组物质不出现上述现象的是( )

8.物质王国发生了一起团伙盗窃案,“警察”把三名“嫌疑犯”(分别是稀硫酸、氯化钠溶液和石灰水,)带回了“警察局”。上级派出下列四名“警察”分别去审问“他们”(即把“他们”鉴别出来)。能完成任务的“警察”是( )
A.硝酸银溶液“警察” B.稀盐酸“警察”
C. 无色酚酞试液“警察” D.纯碱 溶液“警察”
溶液“警察”
9.有a、b、c、d四种无色溶液 分别是碳酸钠、硫酸、氯化钡、盐酸中的一种,下表是它们之间反应的现象:试判断:a、b、c、d依次是( )
分别是碳酸钠、硫酸、氯化钡、盐酸中的一种,下表是它们之间反应的现象:试判断:a、b、c、d依次是( )
|
|
a |
b |
c |
d |
|
b |
无明显现象 |
———— |
有气体产生 |
有沉淀生成 |
|
c |
有气体产生 |
有气体产生 |
———— |
有沉淀生成 |
 A.H2SO4 Na2CO3
BaCl2 HCl B.HCl H2SO4
Na2CO3 BaCl2
A.H2SO4 Na2CO3
BaCl2 HCl B.HCl H2SO4
Na2CO3 BaCl2
C.Na2CO3 H2SO4 HCl BaCl2 D.BaCl2 HCl Na2CO3 H2SO4
10.某工厂排放的废水中含有硫酸,原来采用氢氧化钠溶液处理,通过调节流量阀,最终排出的溶液呈中性(见右图)。现改用氢氧化钾溶液处理以得到钾肥,若氢氧化钾溶液中溶质质量分数与原来所用氢氧化钠溶液中溶质质量分数相同(假设两种碱溶液的密度相同),在废水流量不变的情况下,碱的流量阀应作的调节为( )
A.保持不变 B.加大流量 C.减小流量 D.无法确定
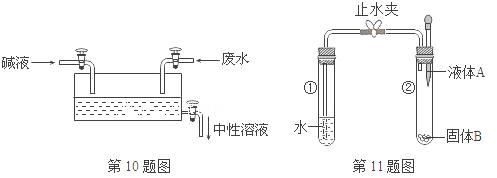
11.如右图所示,打开止水夹,将液体A滴入试管②中与固体B接触。若试管①中的导管口没有气泡产生,则液体A和固体B的组合可能是下列中的( )
)
A.稀盐酸和铁 B.水和生石灰
C.水和氢氧化钠 D.水和氯化钠
12.下列图像能正确反映所对应叙述关系的是( )
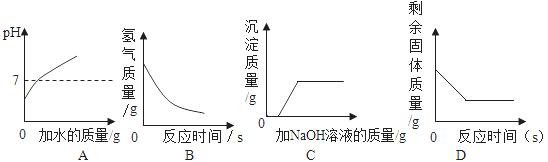
A.向pH=3的溶液中不断加水 B.一定量的稀硫酸与锌粒反应
C. 向H2SO4和CuSO4混合液中滴加NaOH D.煅烧一定质量的石灰石
向H2SO4和CuSO4混合液中滴加NaOH D.煅烧一定质量的石灰石
13.衣服上沾了铁锈(主要成分是Fe2O3),直接用水很难洗净,要除去白色衬衣上的铁锈,你认为比较适宜的液体是( )
A.白醋 B.酱油 C.酒精 D.洗洁精
14.下列物质在溶液中组内两两之间都能互相发生化学反应的是( )
A.硫酸铜、氯化钙、硝酸钠 B.硫酸、碳酸钾、氢氧化钡
C.氯化钙、碳酸钠、氢氧化钾 D.盐酸、硝酸钾、氢氧化锌
15.向烧杯中逐滴加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )

A.A B.B C.C D.D
16.物质发生化学变化常伴随着一些现象,下列需要借助酸碱指示剂才能观察到化学反应发生的是( )

17.如图两圆相交部分是五种物质中两两之间相互反应的示意图.下列对反应现象的说法中,错误的是( )
A.a处形成浅绿色溶液 B.b处形成大量气泡
C.c处的反应为中和反应 D.d处溶液呈红色

18.某同学不慎被蜜蜂蛰伤,蜜蜂的刺液是酸性的,为减轻疼痛可以在蛰伤处涂抹( )
A.葡萄汁 B.食醋 C.矿泉水 D.牙膏
19.下列推论正确的是( )
A.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
B.酸与碱反应生成盐和水,所以生成盐和水的反应一定是酸与碱的反应
C.用酚酞试液检验氢氧化钠溶液是否变质
D.碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液呈碱性
20.下列图像能正确表示对应变化关系的是 ( )
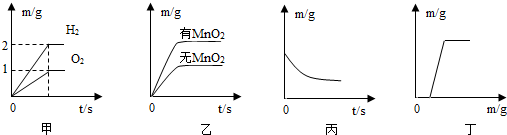
A.图甲:水通电分解产生的气体质量m与反应时间t的关系
B.图乙:两份完全相同的双氧水在有无MnO2的情况下,产生O2质量m与反应时
间t的关系
C.图丙:往锌中加入足量的稀H2SO4,产生的H2质量m与反应时间t的关系
D.图丁:表示往稀盐酸和CuCl2混合液中滴人NaOH溶液,产生的沉淀质量m2与
NaOH溶液质量m1的关系
21.分别把10gSO3、CaO、NaCl和CuSO4•5H2O分别溶于90g水中,所得溶液中溶质的质量分数最小的是 (该题都填溶质的化学式);所得溶液的pH<7的是 。
22.金属钠很软,可以用刀切割。切开外皮后,可以看到钠具有银白色的金属光泽。钠是热和电的良导体。钠的密度是0.97g/cm3,比水的密度小,钠的熔点是97.81℃,沸点是882.9℃。将金属钠放入水中,可以反应生成NaOH和H2;钠跟氧气混合加热生成淡黄色的过氧化钠(Na2O2)固体,钠跟CO2在加热条件下反应生成碳酸钠和单质碳。
(1)小刘同学用图A装置做钠跟氧气反应实验,观察到生成物中出现黑色固体,则该黑色固体是 (填化学式),试写出相应的化学反应方程式 。
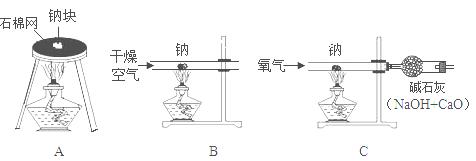
(2)为了探究黑色固体成分,小刘同学进行了下列探究。探究反应中CO2的来源:猜想①:CO2的来源于 ;猜想②:CO2的来源于 ;在上述两种来源中, (填序号)是CO2的主要来源;用图B和C装置实验的目的是 。
23.某同学为了证明白色晶体是(NH4)2SO4,他设计了两步程序:第一步:为了证明铵根离子的存在,必须的操作步骤是
,当观察到
现象时,证明有铵根离子存在。第二步:为了证明硫酸根离子存在,该学生设计了实验方案,请 你设计一个合理的
你设计一个合理的 实验方案
。
实验方案
。
24.王强家菜地里的蔬菜叶色发黄。周日,爸爸叫王强去买化肥硝酸铵(NH4NO3),当他赶到商场时,硝酸铵刚好卖完。
(1)根据所学的化学知识,你建议他购买 ,也能起到与硝酸铵相同的作用。
①氯化钾KCl ②尿素 CO(NH2)2 ③磷矿粉Ca3(PO4)2
(2)硝酸铵不能与碱性物质混合施用的原因是 。
25.某同学设计了如图两个实验,打开分液漏斗的活塞,他会看到实验1和实验2中澄清石灰水出现的现象相同:
(1)两个实验中,澄清石灰水中出现的共同现象是 ;
(2)解释澄清石灰水产生上述现象的原因:
实验1:
 ;
;
实验2: 。

26.已知Fe(OH)2是白色絮状沉淀,并极易被空气中的氧气氧化为Fe(OH)3红褐色沉淀。下图为Fe(OH)2制备实验的改进装置,使用该装置能在较长的时间内观察到生成的Fe(OH)2白色絮状沉淀,以下为实验过程:
(1)A试管中的 反应开始时,打开止水夹,B试管中能看到的现象为 。
反应开始时,打开止水夹,B试管中能看到的现象为 。
(2)A试管中的反应进行足够长的时间后,若要在该装置中得到Fe(OH)2,并在一段时间内防止它被氧气氧化为Fe(OH)3,下一步的实验操作是 。
(3)写出该装置中生成Fe(OH)2的化学方程式 。
28.某同学做实验时发现盛有NaOH溶液的试剂瓶口和橡胶塞上常有白色粉末出现。为了探究这种白色粉末的成分,设计如下实验,请你帮助完成实验报告。
|
实验步骤 |
实验现象 |
实验结论 |
|
(1)将白色粉末放于水中。 |
白色粉末溶于水,形成无色溶液 |
|
|
(2)将无色酚酞滴入步骤1形成的无色溶液中。 |
溶液颜色变红 |
该溶液呈 性 |
|
(3)在步骤2所形成的溶液中加入稀盐酸。并在试管口放一根燃烧的火柴。 |
产生大量气泡,并且溶 液由红色变成无色,燃 烧  的火柴熄灭了。 的火柴熄灭了。 |
溶液中含有 离子。白 色粉末中含有氢氧化钠变质 后生成的 。 |
完成步骤(3)中产生大量气泡的反应化学方程式 。
27.科学兴趣小组在调查一化工厂时,发现有个车间排出的废水澄清透明,呈黄色。为测定该废水中所含的物质,他们进行如下实验(假设能发生的反应均恰好完全反应):
(1 )用pH试纸测试,测得pH为2。
)用pH试纸测试,测得pH为2。
(2)取一定量废水溶液,加入Ba(NO3)2溶液,无现象。
(3)另取一定量废水溶液,加入AgNO3溶液后,过滤,得到白色沉淀A和滤液。
(4)向滤液中加入NaOH溶液,得到红褐色沉淀B。由此可知:该废水溶液呈
性;所得的红褐色沉淀B为
;废水溶液中肯定含有的盐是
 。
。
29.小敏对实验室用石灰石和稀盐酸制取二氧化碳后的废液,进行溶质成分鉴定。取废液上层清液50 克,逐滴加入质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克开始出现白色沉淀。继续滴加至沉淀不再产生,过滤,测得沉淀的质量为5克,并绘制了图象。
克,逐滴加入质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克开始出现白色沉淀。继续滴加至沉淀不再产生,过滤,测得沉淀的质量为5克,并绘制了图象。
(1)滴加的溶液中溶质属于 (选填“盐”或“碱”);
(2)10克碳酸钠溶液中含有的溶质质量是 克;
(3)图象中的a点数值是 ;
(4)废液中含有的溶质是 (写化学式);
(5)通过计算说明,图象横坐标中的b点表示的溶液的质量是多少克?
