
2012.高考江苏卷)某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
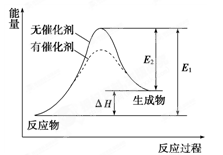
A.该反应为放热反应
B.催化剂能改变该反应的焓变
C.催化剂能降低该反应的活化能
D.逆反应的活化能大于正反应的活化能
2012.高考江苏卷)下列有关说法正确的是 ( )
( )
A.CaCO3(s) ====CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
C. N2(g)+3H2(g)
====2NH3(g) ΔH<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大
N2(g)+3H2(g)
====2NH3(g) ΔH<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大
D.水的离子积常数KW随着温度的升高而增大,说明水的电离是放热反应
2012.高考安徽卷)氢氟酸是一种弱酸,可用来刻蚀玻璃.已知25 ℃时:
①HF(aq)+OH-(aq) ====F-(aq)+H2O(l)
ΔH=-67.7 kJ.mol-1
②H+(aq)+OH-(aq) ====H2O(l)
ΔH=-57.3 kJ.mol-1
在20 mL 0.1 mol.L-1氢氟酸中加入V mL 0.1 mol.L-1 NaOH溶液.下列有关说法正确的是( )
A.氢氟酸的电离方程式及热效应可表示为:
HF(aq)  F-(aq)+H+(aq) ΔH=+10.4
kJ.mol-1
F-(aq)+H+(aq) ΔH=+10.4
kJ.mol-1
B.当V=20时,溶液中:c(OH-)=c(HF)+c(H+)
C.当V=20时,溶液中:c(F-)<c(Na+)=0.1 mol.L-1
D.当V>0时,溶液中一定存在:c(Na+)> c(F-)>c(OH-)>c(H+)
c(F-)>c(OH-)>c(H+)
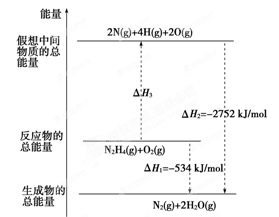
2012.高考重庆卷)肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示.已知断裂1 mol化学键所需的能量(kJ):N≡N为942、OO为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是( )
A.194 B.391
C.516 D.658
2012.高考天津卷)X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y 、M同主族,可形成MY2、MY3两种分子.
、M同主族,可形成MY2、MY3两种分子.
请回答下列问题:
(1)Y在元素周期表中的位置为________________________________________________________________________.
(2)上述元素的最高价氧化物对应的水化物酸性最强的是______________(写化学式),非金属气态氢化物还原性最强的是____________(写化学式).
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有____________________________(写出其中两种物质的化学式).
(4)X2M的燃烧热ΔH=-a kJ.mol-1,写出X2M燃烧反应的热化学方程式:________________________________________________________________________.
(5)ZX的电子式为________;ZX与水反应放出气体的化学方程式为________________________________________________________________________.

(6)熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如右),反应原理为:
2Z+FeG2放电充电Fe+2ZG
放电时,电池的正极反应式为________________________________________________________________________;
充电时,________(写物质名称)电极接电源的负极;该电池的电解质为_________________________________________ _______________________________.
_______________________________.
2012.高考浙江卷)甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整.向反应系统同时通入甲烷、氧气和水蒸汽,发生的主要化学反应有:
|
|
化学方程式 |
焓变 ΔH/kJ.mol-1 |
活化能Ea/kJ.mol-1 |
|
甲烷氧化 |
CH4(g)+2O2(g) ==== CO2(g)+2H2O(g) |
-802.6 |
125.6 |
|
CH4(g)+O2(g) ==== CO2(g)+2H2(g) |
-322.0 |
172.5 |
|
|
蒸汽重整 |
CH4(g)+H2O(g) ==== CO(g)+3H2(g) |
206.2 |
240.1 |
|
CH4(g)+2H2O(g) ====CO2(g)+4H2(g) |
165.0 |
243.9 |
回答下列问题:
(1)反应CO(g)+H2O(g) ====CO2(g)+H2(g)的ΔH=________kJ.mol-1.
(2)在初始阶段,甲烷蒸汽重整的反应速率________甲烷氧化的反应速率(填“大于”、“小于”或“等于”).
(3)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应CH 4(g)+H2O(g)
4(g)+H2O(g)  CO(g)+3H2(g)的KP=________;随着温度的升高,该平衡常数________(填“增大”、“减小”或“不变”).
CO(g)+3H2(g)的KP=________;随着温度的升高,该平衡常数________(填“增大”、“减小”或“不变”).
(4)从能量角度分析,甲烷自热重整方法的先进之处在于________________________________________________________________________.
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图:
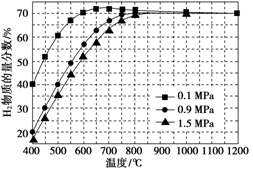
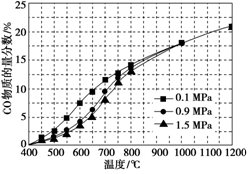
①若要达到H2物质的量分数>65%、CO物质的量分数<10%,以下条件中最合适的是________.
A.600 ℃,0.9 MPa B.700 ℃,0.9 MPa
C.800 ℃,1.5 MPa D.1000 ℃,1.5 MPa
②画出600 ℃,0.1 MP a条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图:
a条件下,系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图:
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是________________________________________________________________________.
专题五 化学反应中 的能量变化
的能量变化
[解析]选C.由图示可知,加入催化剂只是降低了正、逆反应的活化能,并没有改变反应的热量变化即焓变,C项正确.
[解析]选B.A项反应不能自发,说明复合判据ΔH-TΔS>0,即ΔH>TΔS. 由方程式可知ΔS>0,故ΔH>0,A项错误.
由方程式可知ΔS>0,故ΔH>0,A项错误.
B项镀铜铁制品镀层受损易形成铜铁原电池,铁较活泼作负极,腐蚀更快,B项正确.
C项,升高温度,平衡逆向移动,H2的平衡转化率减小,C项错误.
D项,水的电离是吸热反应,D项错误.
[解析]选B.A项,①-②得ΔH=-10.4 kJ/mol,A错.B项,V=20 mL时,HF与NaOH恰好完全反应生成NaF,由质子守恒可得:
c(OH-)=c(H+)+c(HF),B正确.
C项,由B 可知:c(F-)<c(Na+)
生成c(NaF)=0.05 mol.L-1故c(Na+)=0.05 mol.L-1,C项错误.
D项,当加NaOH量非常少时, 可能有:
可能有:
c(F-)>c(Na+)>c(H+)>c(OH-).
[解析]选B.由图知N2H4(g)+O2(g) ====N2(g)+2H2O(g) ΔH=-534 kJ/mol.可设断裂1 mol N—H键所需能量为x kJ,154 kJ+4x kJ+500 kJ-2752 kJ=-534 kJ可求得x=391.
[解析]由Y、M同主族,且可形成MY2、MY3两种分子可知Y为O元素,M为S元素;又因X、Y、Z、M、G分属三个短周期且原子序数依次增大,O元素、S元素分属二、三周期,那么X为H元素,Z为Na元素,G为Cl元素.Cl的非金属性最强则HClO4酸性最强,S元素的非金属性最弱则H2S还原性最强,O、Cl的单质或两元素之间形成的化合物用于水消毒剂的物质具有强氧化性,常见的有Cl2、O3、ClO2.
(6)放电时为 原电池,正极发生还原反应为Fe2++2e-====Fe,充电时相当于电解池,阴极发生还原反应,分析方程式知发生还原反应的物质应为钠,由图看出该电池的电解质为βAl2O3.
原电池,正极发生还原反应为Fe2++2e-====Fe,充电时相当于电解池,阴极发生还原反应,分析方程式知发生还原反应的物质应为钠,由图看出该电池的电解质为βAl2O3.
[答案](1)第二周期第ⅥA族
(2)HClO4 H2S
 (3)Cl2、O3、ClO2(任写两种,
(3)Cl2、O3、ClO2(任写两种, 其他合理答案均可)
其他合理答案均可)
(4)H2S(g)+O2(g) ====SO2(g)+H2O(l)
ΔH=-a kJ.mol-1
(5)Na+[H]-
NaH+H2O====NaOH+H2↑
(6)Fe2++2e-====Fe 钠 βAl2O3
[解析](1)由盖斯定律可知,ΔH=165.0 kJ.mol-1-206.2 kJ.mol-1=-41.2 kJ.mol-1.
(2)因蒸汽重整比甲烷氧化的活化能高,所以甲烷蒸汽重整的速率小.
(3 )因气体物质的量与气体分压成正比
)因气体物质的量与气体分压成正比 ,所以由平衡常数的定义知,Kp=,又因该反应为吸热反应,故升温时平衡常数增大.
,所以由平衡常数的定义知,Kp=,又因该反应为吸热反应,故升温时平衡常数增大.
(4)甲烷氧化会放出大量热量,而蒸汽重整需要吸收大量热能,所以甲烷自热重整方法的先进之处在于它能提高能量利用率.
(5)由题中所图可知H2物质的量分数>65%的条件为高于550 ℃、0.1 MPa或高于700 ℃、0.9 MPa或高于750 ℃、1.5 MPa,CO物质的量分数<10%的条件为低于750 ℃、1.5 MPa或低于700 ℃、0.9 MPa或650 ℃、0.1 MPa综合考虑应选700 ℃、0.9 MPa.
(6)因氧气能与氢气反应,所以当氧气过量时,氧气与氢气反应使H2的物质的量分数降低.
[答案](1)-41.2 (2)小于
(3) 增大
(4)系统内强放热的甲烷氧化反应为强吸热的蒸汽重整反应提供了所需的能量(其他合理答案均可)
(5)①B ②
(6)甲烷氧化程度过高,氢气和氧气反应(其他合理答案均可)