
相对原子质量H 1 O 16 N 14 S 32 Na 23 Mg 24 Cu 64 Fe 56 C 12 Cl 35.5 Al 27 P 31 Ca 40 K 39
1.以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是




A B C D
2.现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ⑧氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是 ( )
A.分液、萃取、蒸馏 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
3.用四氯化碳萃取碘水中的碘,下列说法中不正确的是 ( )
A. 实验中使用的主要仪器是分液漏斗
B. 碘在四氯化碳中的溶解度比在水中的溶解度大
C. 碘的四氯化碳溶液呈紫色
D. 分液时,水从分液漏斗下口流出, 碘的四氯化碳溶液从分液漏斗上口流出
4.下列有关0.1 mol.L-1 NaOH 溶液的叙述正确的是( )
A.1L该溶液中含有NaOH 40g
B.100ml该溶液中含有OH- 0.01mol
C.从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01 mol.L-1
D.在1L水中溶解4g NaOH即可配制得0.1 mol.L-1 NaOH 溶液
5.用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.标准状况下,22.4LH2O含有的分子数为1 NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.01NA
C.标准状况下,1 NA 个CO2分子占有的体积约为22.4L
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为1 NA
6.下列溶液中,跟100mL 0.5mol/L NaCl溶液所含的Cl-物质的量浓度相同的是( )
A.100mL 0.5mol/L MgCl2溶液 B.200mL 0.25mol/L CaCl2溶液
C.50ml 1mol/L NaCl溶液 D.25mL0.5mol/L AlCl3溶液
7.胶体区别于其它分散系的本质特征是 ( )
A.胶体粒子直径在1-100nm之间 B.胶体粒子带电荷
C.胶体粒子不能穿过半透膜 D.胶体粒子能够发生布朗运动
8.下列物质中,能够导电的电解质是 ( )
A.Cu丝 B.熔融的MgCl2 C.NaCl溶液 D.蔗糖
9.在某无色透明的酸性溶液中,能共存的离子组是 ( )
A.Na+ 、K+、SO42-、HCO3- B.Cu2+、K+、SO42-、NO3-
C.Na+、 K+、Cl-、 NO3- D.Fe3+、K+、SO42-、Cl-
10.能正确表示下列化学反应的离子方程式的是 ( )
A.氢氧化钡溶液与盐酸的反应 OH-+H+ = H2O
B.澄清的石灰水与稀盐酸反应 Ca(OH)2 + 2H+ = Ca2+ + 2H2O
C.铜片插入硝酸银溶液中 Cu + Ag+ = Cu2+ + Ag
D.碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2

1.计算483 g Na2SO4.10H2O中所含的Na+的物质的量是 SO42-的物质的量是 ,所含H2O分子的数目是 个。
2.将12.5克硫酸铜溶于水配成200mL溶液,该溶液中硫酸铜的物质的量浓度为______________________,稀释至500mL后,其物质的量浓度__________________。
若从稀释后的溶液中取出10mL,其中不变的物理量是__________________
A CuSO4物质的量浓度 B.含CuSO4的质量 C.溶液的密度
D. CuSO4的质量分数 E. CuSO4的物质的量
3.同温同压下,同体积的H2和CO2物质的量之比为___________,原子个数之
比__________,质量比___________;同温同压下,同质量的H2和CO2分子个数之比
________,原子个数之比__________,体积比为_______________;若两者所含原子
个数相等,它们的物质的量比是 ________ __。
4.若某原子的摩尔质量是M g /mol,则一个该原子的真实质量是 g。
5.用10 mL的0.1 mol.L-1 BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种
溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是_______________C
6.在标准状况下 ①6.72L CH4气体 ②3.01×1023个HCl气体分子
③13.6g H2S气体 ④0.2mol NH3, 下列对这四种气体的关系从大到小的排列是(用上述数字序号表示)
(1) 四种气体的物质的量_________________________
(2)标准状况下四种气体的体积_________________________
(3)四种气体的质量______________________________________
7.同温同压下,等质量的SO2和CO2相比较, 其物质的量比 _______________
体积比为 _______________ 密度比为 _______________
8. 有一真空瓶质量为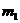 ,该瓶充入空气后质量为
,该瓶充入空气后质量为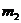 。在相同状况下,若改为充入某气体A时,总质量为
。在相同状况下,若改为充入某气体A时,总质量为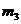 。则A的相对分子质量是 _______________
。则A的相对分子质量是 _______________
9.溶液中可能有下列阴离子中的一种或几种:SO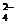 、S0
、S0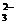 、CO
、CO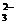 、Cl-。
、Cl-。
(1)当溶液中有大量H+存在时,则不可能有 ______ 存在。
(2)当溶液中有大量Ba2+存在时,溶液中不可能有 ______ 存在。
(3)当溶液中有 ______ 和 ______的阳离子存在时,上述所有阴离子都不可能存在。
10.写出下列反应的离子方程式:
(1)用稀硫酸清洗铁锈(Fe2O3) ________ __
(2)碳酸钠溶液与盐酸混合 ________ __
(3)硫酸铜溶液和氢氧化钡溶液混合 ________ __
(4)向足量澄清石灰水中通入二氧化碳 ________ _ _

1..某同学欲用98%的浓H2SO4(ρ=1.84g/cm3)配制成500mL 0.5mol/L的稀H2SO4溶液
(1)填写下列操作步骤:
①所需浓H2SO4的体积为 。
②将量取的浓H2SO4沿内壁慢慢注入盛有约100mL水的烧杯里,并不断搅拌,目的是 。
③立即将上述溶液沿玻璃棒注入 中,并用50mL蒸馏水洗涤烧杯2-3次,并将洗涤液注入其中,并不时轻轻振荡。
④加水至距刻度 处,改用 加水,使溶液的凹液面正好跟刻度相平。盖上瓶塞,上下颠倒数次,摇匀。
(2)请指出上述操作中一处明显错误: 。
(3)误差分析:(填偏高、偏低、无影响)
操作②中量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将 ;
若容量瓶中洗净后未干燥,残留少量水,则所配制的溶液浓度将 ;
操作⑤中,若定容时,眼睛俯视,则所配制的溶液浓度将
 (2)如何运用最简方法检验溶液中有无SO42-离子?
。如果有,应该如何除去SO42-离子?
。
(2)如何运用最简方法检验溶液中有无SO42-离子?
。如果有,应该如何除去SO42-离子?
。
(3)在粗盐经过溶解→过滤后的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。请问这步操作的目的是 。
(4)将经过操作(3)后的溶液过滤。请问这一操作能除掉哪些杂质?
3.现在NaOH 、Na2CO3、Ba(OH)2三种无色溶液,请选用一种试剂把它们鉴别出来,你选择的试剂是____________________,简述实验操作及现象和结论:
________________________________________________________________
_________________________________________________________________
_________________________________________________________________
与你选择的试剂进行实验有关的离子方程式为
_________________________________________________________
_______________________________________________________
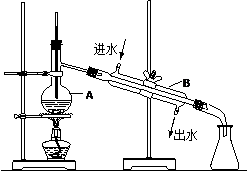 4如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
4如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
(1)图中的两处明显的错误是_____________________________________。
(2)A仪器的名称是______________,B仪器的名称是_______________。
(3)实验时A中除加入自来水外,还需加入少量__________________,其作用是__________________
在标准状况下,CO和CO2的混合气体质量36g,体积为22.4L,
则CO所占体积是 L,
CO的质量是 g,所含CO2的分子数是 个。