1. 下列物质中,在正常情况下不应该出现在人体内环境中的是
下列物质中,在正常情况下不应该出现在人体内环境中的是
A.抗体 B.糖原 C.胰岛素 D.氨基酸
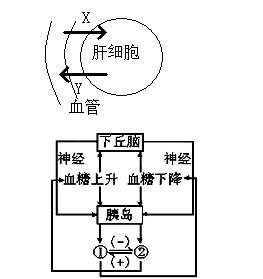
2.图5显示肝细胞代谢过程中的物质交换,
X和Y分别可代表
A.葡萄糖、CO2
B.氨基酸、胰岛素
C.肾上腺素、尿素
D.甘油三酯、脂肪酸
3. 人体血糖的生理调节过程如右图所示,下列有关
叙述错误的是
A.血糖下降,刺激胰岛分泌②,从而使血糖升高
B.血糖升高,刺激下丘脑通过神经支配胰岛分泌①
C.在血糖调节上,分泌物①与②表现为拮抗作用
D.人体内使血糖浓度升高的激素有②和甲状腺激素
4.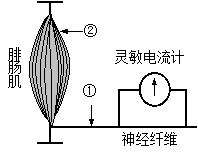 右图表示具有生物活性的蛙坐骨神经-腓肠肌标
右图表示具有生物活性的蛙坐骨神经-腓肠肌标
本,神经末梢与肌细胞的接触部位类似于突触,
称“神经-肌接头”。下列叙述错误的是
A.“神经-肌接头”处可发生电信号与化学信号的转变
B.电刺激①处,肌肉会收缩,灵敏电流计指针也会偏转
C.电刺激②处,神经纤维上的电流计会记录到电位变化
 D.神经纤维上兴奋的传导方向与膜内的电流方向相同
D.神经纤维上兴奋的传导方向与膜内的电流方向相同
5.神经元细胞膜内外的离子可以影响膜电位和突触传递过程,如细胞内Ca2+的升高促进突触小泡向突触前膜移动,而K+流出细胞将会导致细胞膜内电位更负。则下列情形中不利于神经递质释放的是
A.Na+流入细胞内 B.Ca2+流入细胞内
 C.K+流出细胞
D.突触小泡与突触前膜融合
C.K+流出细胞
D.突触小泡与突触前膜融合
6.人肝细胞合成的糖原储存在细胞内,合成的脂肪不储存在细胞内,而是以VLDL(脂肪与蛋白质复合物)形式分泌出细胞外。下列叙述正确的是
A.VLDL 的合成与核糖体无关 B.VLDL 以自由扩散方式分泌出细胞外
C.胰高血糖素可促进肝细胞内糖原的合成
D.肝细胞内糖原的合成与分解可影响血糖含量
7. 已知反应X + Y == M + N为放热反应,下列说法正确的 A.因该反应为放热反应,故不必加热就可发生
B.X的能量一定高于M C.M和N的总能量一定高于X和Y的总能量 D.X和Y的总能量一定高于M和N的总能量
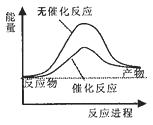
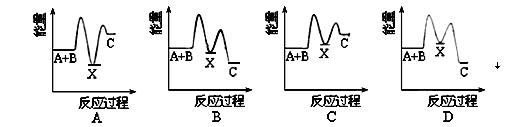
8. 反应A+B→C(△H<0)分两步进行:①A+B→X(△H<0),②X→C(△H<0)。下列示意图中,能正确表示总反应过程中能量变化的是
 9. 碘与氢气反应的热化学方程式是
① I2(g) + H2(g)
9. 碘与氢气反应的热化学方程式是
① I2(g) + H2(g) 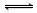 2HI(g) ΔH=-9.48 kJ • mol-1
② I2(s) + H2(g)
2HI(g) ΔH=-9.48 kJ • mol-1
② I2(s) + H2(g) 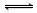 2HI(g) ΔH= +26.48 kJ • mol-1
下列说法正确的是
A.①的产物比②的产物稳定
B.I2(s) = I2(g) ΔH=+17.00 kJ.mol-1
C.②的反应物总能量比①的反应物总能量低
D.1mol I2(g)中通入1 mol
H2(g),发生反应时放热9.48 kJ
2HI(g) ΔH= +26.48 kJ • mol-1
下列说法正确的是
A.①的产物比②的产物稳定
B.I2(s) = I2(g) ΔH=+17.00 kJ.mol-1
C.②的反应物总能量比①的反应物总能量低
D.1mol I2(g)中通入1 mol
H2(g),发生反应时放热9.48 kJ
10.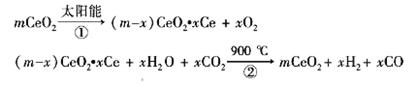 某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO。其过程如下:
某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变为H2、CO。其过程如下:
下列说法不正确的是
A.该过程中CeO2是催化剂,质量没有减少
B.该过程实现了太阳能向化学能的转化
C.右图中ΔH1=ΔH2+ΔH3
D.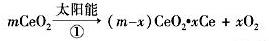 ΔH >0
ΔH >0
11. 下列说法正确的是 A.右图可表示水分解过程中的能量变化 B.若 2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol,
则碳的燃烧热为110.5 kJ/mol C.需要加热的反应一定是吸热反应,
常温下能发生的反应一定是放热反应
D.已知:I:H2(g) + Cl2(g)== 2HCl (g) ΔH=-a kJ/mol,
II: 则断开1 mol H-Cl键所需的能量为(a+ b+ c) kJ/mol
则断开1 mol H-Cl键所需的能量为(a+ b+ c) kJ/mol
12. 在1200℃时,天然气脱硫工艺中会发生下列反应:
H2S(g) +  O2(g) = SO2(g) + H2O (g)
ΔH1
O2(g) = SO2(g) + H2O (g)
ΔH1
2H2S(g) + SO2(g) =  S2(g) + 2H2O(g)
ΔH2
H2S(g) +
S2(g) + 2H2O(g)
ΔH2
H2S(g) +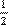 O2(g) = S(g) + H2O(g)
ΔH3
O2(g) = S(g) + H2O(g)
ΔH3
2S(g) = S2 (g) ΔH4 则△H4的正确表达式为 A.ΔH4 = 3/2 (ΔH1+ΔH2-3ΔH3) B.ΔH4 = 2/3 (ΔH1+ΔH2-3ΔH3) C.ΔH4 = 2/3 (3ΔH3-ΔH1-ΔH2) D.ΔH4 = 3/2 (ΔH1-ΔH2-3ΔH3)
13. 下列热化学方程式或离子方程式中,正确的是:
A.甲烷的标准燃烧热为-890.3kJ.mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3kJ.mol-1
B.500℃、30MPa下,将0.5molN2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:
N2(g)+3H2(g)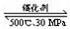 2NH3(g) ΔH=-38.6kJ.mol-1
C.氯化镁溶液与氨水反应:Mg2+ +
2OH-=Mg(OH)2↓
D.氧化铝溶于NaOH溶液:Al2O3 + 2OH-+3H2O=2AlO- 2+ H2O
2NH3(g) ΔH=-38.6kJ.mol-1
C.氯化镁溶液与氨水反应:Mg2+ +
2OH-=Mg(OH)2↓
D.氧化铝溶于NaOH溶液:Al2O3 + 2OH-+3H2O=2AlO- 2+ H2O
14.已知真空中两个静止的相同金属小球(可看为质点)带电量分别为-2.0×10-8C和+4.0×10-8C,当相距0.2m时,其间作用力F,将两金属球相接触后再放回原来位置,则其间作用力为:
A.F/8 B.F/4. C.F/3 D.F/2
15.如图所示为电场中的一条电场线,A、B为其上的两点,EA、EB和UA、 UB.分别表示A、B两点的电场强度和电势,则以下说法正确的是:
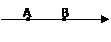 A.EA>EB
B.EA<EB
A.EA>EB
B.EA<EB
C.UA<UB D.UA>UB
16.取一对用绝缘支柱支持的金属导体A和B,使它们彼此接触,起初它们不带电,现在把带正电荷的球C移近导体A,如图,用手触摸一下A,放开手,再移去C,再把A和B分开,此时A和B上带电情况是:
A.A和B都带负电 B.A和B不带电
C.A带负电,B不带电 D.A和B都带正电
17.对于一个电容器,下列说法中正确的是:
A.电容器所带的电量越多,电容越大
B.电容器两极板间的电势差越大,电容越大
C.电容器所带的电量增加一倍,两极板间的电势差也增加一倍
D.电容器两极板间的电势差减小到原来的1/2,它的电容也减小到原来的1/2
18.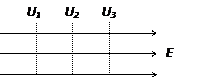 如图2所示,实线是电场线,虚线是等势面,且相邻等势面间的电势差相等,令U2=0,一正电荷在等势面U3上时,具有动能20J,它运动到U1时速度为零,那么,当该电荷的电势能为4J时,其动能大小为:
如图2所示,实线是电场线,虚线是等势面,且相邻等势面间的电势差相等,令U2=0,一正电荷在等势面U3上时,具有动能20J,它运动到U1时速度为零,那么,当该电荷的电势能为4J时,其动能大小为:
A.4J B.6J
C.10J D.16J
19.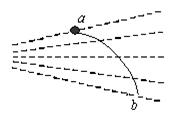 如图1所示,某同学在研究电子在电场中的运动时,得到了电子由a点运动到b点的轨迹(图中实线所示),图中未标明方向的一组虚线可能是电场线,也可能是等势面,则下列判断不正确的是:
如图1所示,某同学在研究电子在电场中的运动时,得到了电子由a点运动到b点的轨迹(图中实线所示),图中未标明方向的一组虚线可能是电场线,也可能是等势面,则下列判断不正确的是:
A.如果图中虚线是电场线,电子在a点电势能较小
B.如果图中虚线是等势面,电子在b点动能较大
C.不论图中虚线是电场线还是等势面,a点的场
强都大于b点的场强
D.不论图中虚线是电场线还是等势面,a点的电
势都高于b点的电势
20.一对平行金属板A、B间电压变化如图2所示,一个不计重力的带负电的粒子原静止在O点处,下面几种关于粒子的运动情况的说法中正确的是:
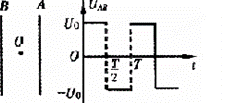 A.在t=0时无初速释放,则粒子一定能打到A板上
A.在t=0时无初速释放,则粒子一定能打到A板上
B.在t=0时无初速释放,粒子在满足一定条件的情况下才会打到A板上
C.t=0时无初速释放,则则粒子一定不能打到A板上
D.t=T/4时无初速释放,粒子一定能打到A板上
II 非选题
21.
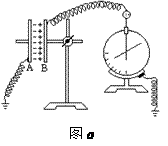 (1)李明与张华采用如图a所示的实验装置探究影响平行板电容器电容的因素,实验前两人首先用干电池对两极板充电,并保持两极板电量不变,然后将极板A接地,平行板电容器的极板B与一个灵敏的静电计相接.第一次两人保持极板间距离不变,仅将A极板向上移动,发现静电计指针偏角变大,说明两极板间的正对面积的变化影响了电容C的大小,由此两人得出结论为
;第二次两人保持极板间正对面积不变,仅将A极板向左移动,增大电容器两极板间的距离时,发现静电计指针偏角也变大,说明两极板间的距离变化影响了电容C的大小,由此两人得出结论为
;第三次两人保持极板间正对面积不变,极板间距离也不变,在两板间插入一玻璃片,发现静电计指针偏角变小,说明两极板间的绝缘介质的变化影响了电容C的大小,由此两人得出结论为
.
(1)李明与张华采用如图a所示的实验装置探究影响平行板电容器电容的因素,实验前两人首先用干电池对两极板充电,并保持两极板电量不变,然后将极板A接地,平行板电容器的极板B与一个灵敏的静电计相接.第一次两人保持极板间距离不变,仅将A极板向上移动,发现静电计指针偏角变大,说明两极板间的正对面积的变化影响了电容C的大小,由此两人得出结论为
;第二次两人保持极板间正对面积不变,仅将A极板向左移动,增大电容器两极板间的距离时,发现静电计指针偏角也变大,说明两极板间的距离变化影响了电容C的大小,由此两人得出结论为
;第三次两人保持极板间正对面积不变,极板间距离也不变,在两板间插入一玻璃片,发现静电计指针偏角变小,说明两极板间的绝缘介质的变化影响了电容C的大小,由此两人得出结论为
.
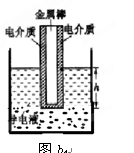
(2) 李明与张华两人利用上述探究的结论,对实验进行了改动,如图b所示.将一金属棒用绝缘皮包住后与导电液体构成一个电容器,将金属棒和导电液体分别与直流电源的两极相连接,从电容C或导电液与金属棒间的电压U的变化就能反映液面的升降情况。电源接通,若此后电容C减小,反映h ;电源接通再断开,若此后电压U减小,反映h .
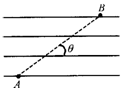
22.一个带正电的微粒,从A点射入水平方向的匀强电场中,微粒沿直线AB运动,如图,AB与电场线夹角θ=30°,已知带电微粒的质量m=1.0×10-7kg,电量q=1.0×10-10C,A、B相距L=20cm.(取g=10m/s2,结果保留二位有效数字)求:
(1)说明微粒在电场中运动的性质,要求说明理由.
(2)电场强度的大小和方向?
 (3)要使微粒从A点运动到B点,电场力做了多少功?
(3)要使微粒从A点运动到B点,电场力做了多少功?
23.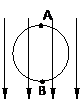 有一匀强电场,其场强为E,方向竖直向下。把一个半径为r的光滑绝缘环,竖直置于电场中,环面平行于电场线,环的顶点A穿有一个质量为m、电量为q(q>0)的空心小球,如图所示。当小球由静止开始从A点下滑到最低点B时,小球受到环的压力多大?
有一匀强电场,其场强为E,方向竖直向下。把一个半径为r的光滑绝缘环,竖直置于电场中,环面平行于电场线,环的顶点A穿有一个质量为m、电量为q(q>0)的空心小球,如图所示。当小球由静止开始从A点下滑到最低点B时,小球受到环的压力多大?
24.如图所示是示波器的示意图,竖直偏转电极的极板长L1=4cm,板间距离d=1cm。板右端距离荧光屏L2=18cm,(水平偏转电极上不加电压,没有画出)电子沿中心线进入竖直偏转电场的速度是v=1.6×107m/s,电子电量e=1.6×10-19C,质量m=0.91×10-30kg。
(1)要使电子束不打在偏转电极上,加在竖直偏转电极上的最大偏转电压U不能超过多大?
(2)若在偏转电极上加U/2 的偏转电压,则打在荧光屏距O点多远处?
25.(14分) W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X元素的原子核外电子层数等于最外层电子数,Z元素原子核内有29个质子,能生成砖红色的Z2O和黑色的ZO两种氧化物。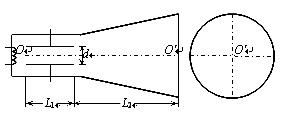 ⑴ W位于元素周期表第_________周期第_________族。W的气态氢化物稳定性比H2O(g) __________(填“强”或“弱”)。
⑵ Y的原子结构示意图是
,Y的原子半径比X的__________(填“大”或“小”)。
⑶ Y的最高价氧化物对应水化物的浓溶液与Z的单质在加热时反应的化学方程式是
_______________________________________________________________。
⑷ 已知下列数据: 3Fe(s)+ 2O2(g)
=Fe3O4(s);ΔH=-1118. 4 kJ.mol-1
2X(s) +
⑴ W位于元素周期表第_________周期第_________族。W的气态氢化物稳定性比H2O(g) __________(填“强”或“弱”)。
⑵ Y的原子结构示意图是
,Y的原子半径比X的__________(填“大”或“小”)。
⑶ Y的最高价氧化物对应水化物的浓溶液与Z的单质在加热时反应的化学方程式是
_______________________________________________________________。
⑷ 已知下列数据: 3Fe(s)+ 2O2(g)
=Fe3O4(s);ΔH=-1118. 4 kJ.mol-1
2X(s) +  O2(g)=X2O3(s);ΔH=-1675.8 kJ•mol-1
则X的单质和Fe3O4(s)反应的热化学方程式是: 。
O2(g)=X2O3(s);ΔH=-1675.8 kJ•mol-1
则X的单质和Fe3O4(s)反应的热化学方程式是: 。
26. (14分) 某实验小组用0.55 mol/L NaOH溶液和0.25 mol/L H2SO4溶液进行中和热的测定。 Ⅰ.配制0.55 mol/L NaOH溶液
 ⑴ 若实验中大约要使用240 mL NaOH溶液,至少需要称量NaOH固体 g。
⑵ 从下图中选择称量NaOH固体所需要的仪器有(填字母): 。
⑴ 若实验中大约要使用240 mL NaOH溶液,至少需要称量NaOH固体 g。
⑵ 从下图中选择称量NaOH固体所需要的仪器有(填字母): 。
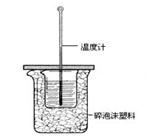
 Ⅱ.测定中和热的实验装置如图所示。
Ⅱ.测定中和热的实验装置如图所示。
⑶图中缺少的仪器名称是 。 ⑷ 写出H2SO4(aq)、稀NaOH(aq)反应中和热的热化学方程式(已知中和热数值为57.3 kJ/mol)。 。
⑸ 取50 mL NaOH溶液和50 mL硫酸溶液进行实验,实验数据如下表。
|
实验 编号 |
起始温度t1/℃ |
终止温度
t2/℃ |
温度差平均值(t2-t1)/℃ |
||
|
H2SO4 |
NaOH |
平均值 |
|||
|
1 |
26.2 |
26.0 |
26.1 |
29.3 |
|
|
2 |
27.0 |
27.4 |
27.2 |
30.5 |
|
|
3 |
25.9 |
25.9 |
25.9 |
29.4 |
|
|
4 |
26.4 |
26.2 |
26.3 |
29.6 |
近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g.℃)。则中和热ΔH= kJ/mol(精确到0. 1)。
27. (14分) 将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH1=+ 48. 5 kJ.mol -1
②CH3OH(g)+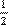 O2(g)=CO2(g)+2H2(g) ΔH2=-194. 0 kJ.mol -1
O2(g)=CO2(g)+2H2(g) ΔH2=-194. 0 kJ.mol -1
⑴ 根据①推知:CH3OH(l)+H2O(g)=CO2(g)+3H2(g) 的ΔH ΔH1(填“>”、“=”或“<”)。
⑵
根据②推知: CH3OH(g) + O2 (g) == CO2(g) + 2H2O(l)
放出的热量
194. 0kJ(填“>”、“=”、“<”或“不能确定”)。
O2 (g) == CO2(g) + 2H2O(l)
放出的热量
194. 0kJ(填“>”、“=”、“<”或“不能确定”)。
⑶ 反应②中的能量变化如右图所示,则△H2=
(用含E1、E2或E3的式子表示)。
⑷ 生产过程中,若将CH3OH(g)、H2O(g)、O2(g)按一定比例混合,可以实现热量的零排放和零补充,则进料气中H2O(g)与O2(g)的体积比为 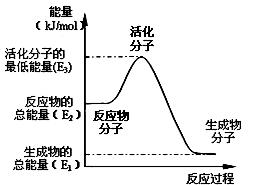 。
。
28. (16分) 白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。
(1)已知298 K时白磷、红磷完全燃烧的热化学方程式分别为
P4(白磷,s)+5O2(g)===P4O10(s) ΔH1=-2 983.2 kJ.mol-1
P(红磷,s)+O2(g)===P4O10(s) ΔH2=-738.5 kJ.mol-1
则该温度下白磷转化为红磷的热化学方程式为_____________________________。
(2)已知298 K时白磷不完全燃烧的热化学方程式为
P4 (白磷,s)+3O2(g)===P4O6(s) ΔH=-1638 kJ.mol-1。在某密闭容器中加入124 g白磷和4. 5mol O2,控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为__________,反应过程中放出的热量为 。
(3)已知白磷和PCl3的分子结构如图所示,现提供以下化学键的键能(kJ.mol-1):P-P 198,Cl-Cl 243,P-Cl 331。

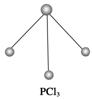
则反应P4(白磷,s)+6Cl2(g)===4PCl3(s)的反应热ΔH=______________。
29.(14分)内环境是人体细胞生活的直接环境,内环境的温度、渗透压、pH及各种化学物质的含量,正常情况下能够维持相对稳定的状态,这是人体完成各项生命活动的必要条件。
(1)能与毛细血管壁细胞直接进行物质交换的具体内环境是________________。
(2)人体内环境的各种理化性质及化学物质含量会发生变化的原因是_________、______________。
(3)人体维持体温相对稳定的调节方式有______________________________。
(4)尝试构建人体肝脏内血浆、组织液、成熟红细胞内液间O2、CO2扩散的模型(①在图形框间用实线箭头表示O2,用虚线箭头表示CO2。②不考虑CO2进入成熟红细胞内液)。[
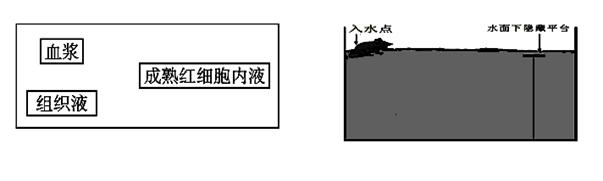
30.(16分)为探究铅中毒对大鼠学习记忆的影响,将大鼠分为四组,其中一组饮水,其余三组饮醋酸铅溶液,60 天后进行检测。检测a:用下图水迷宫(池水黑色,大鼠无法看到平台)进行实验,大鼠从入水点入水,训练其寻找水面下隐蔽平台,重复训练4 天后撤去平台,测定大鼠从入水点到原平台水域的时间;检测b:测定脑组织匀浆铅含量及乙酰胆碱酯酶(AchE)活性。AchE 活性检测原理:AchE 可将乙酰胆碱(Ach)水解为胆碱和乙酸,胆碱与显色剂显色,根据颜色深浅计算酶活性。
|
组别 |
醋酸铅溶液浓度 /g.L-1 |
脑组织铅含量 /g.gprot-1 |
AchE 活性 /U.mgprot-1 |
到达原平台水域时间/s |
|
① |
0 |
0.18 |
1.56 |
22.7 |
|
② |
0.05 |
0.29 |
1.37 |
23.1 |
|
③ |
1 |
0.57 |
1.08 |
26.9 |
|
④ |
2 |
1.05 |
0.76 |
36.4 |
请回答:
(1)表中用于评价大鼠学习记忆能力的指标是 ,通过该指标可知 组大鼠学习记忆能力最弱。
(2)Ach是与学习记忆有关的神经递质,该递质由突触前膜释放进入 ,与突触后膜上的受体结合,引发突触后膜 变化。Ach 发挥效应后在 酶的催化下水解,本实验是通过检测单位时间内的
生成量,进而计算该酶的活性。
(3)表中结果表明:脑组织铅含量越高,Ach 水解速度越 。
(4)水迷宫实验过程中,使短期记忆转化为长期记忆的措施是 ,以此强化神经元之间的联系。
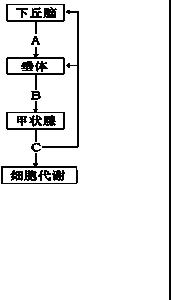
31.(24分)右图为甲状腺激素分泌的分级调节示意图,其中A、B和C表示三种不同的激素。回答下列问题:
(1)A、B和C三种激素的名称依次是 、
、 。
(2)当机体受到某种刺激时,血液中C的含量增加,则集体的产热量会 ,成年个体神经系统的兴奋性会 。
(3)怀孕母亲缺碘时,C分泌量下降,通过反馈调节,使A和B的分泌量 ,结果甲状腺增生,胎儿的发育会受到影响,尤其 的发育受到的影响
最大。反馈调节是指 。