
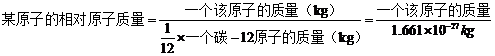
[特别提醒]
1.相对原子质量只是一个比值。
2.相对原子质量的国际单位制单位为1,一般不写 出,不能认为相对原子质量
出,不能认为相对原子质量 没有单位。
没有单位。
3.一种碳原子是指原子核内有6个质子和 6个中子的碳原子,即:碳-12。
6个中子的碳原子,即:碳-12。
4. 原子的实际质量与其相对原子质量成正比。
原子的实际质量与其相对原子质量成正比。
5.计算时常用相对原子质量的近似值。
6.相对原子质量≈质子数+中子数
注意:整个原子的质量几乎都集中在原子核上,因为质子和中子的质量大约相等,都约等于碳12原子质量的1/12,即与等于1个氢原子的质量,电子的质量很小,仅仅约等于质子质 量的1/1836,因此原子的质量主要集中在原子核上。
量的1/1836,因此原子的质量主要集中在原子核上。
7 .等质量的不同微粒,相对原子质量与微粒数目
.等质量的不同微粒,相对原子质量与微粒数目
 成反比。
成反比。
1.离子的定义:带电的原子或原子团叫做离子。离 子也是 的一种微粒。
子也是 的一种微粒。
说明: 原子得到或失去电子从而带上电荷,就变成离子。原子失去电子变成阳离子,阳离子带正电荷,原子得到电子变成阴离子,阴离子带负电荷。
2.离子的写法:元素符号右上角,电荷的数字在前符号在后,“1”可以省略。
如:阳离子:Na+、Mg2+、Al3+ 等
 阴离子:Cl-、O2- 等
阴离子:Cl-、O2- 等
3.离子与原子的比较
区别:①电性 不同:离子带电,原子不带电
不同:离子带电,原子不带电
②性质不同:离子稳定,原子一般不稳定
③结构不同:在原子里,核电荷数=质子数=核外电子数
在离子里, 核电荷数=质子数 ≠ 核外电子数
核电荷数=质子数 ≠ 核外电子数
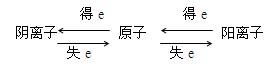 联系:
联系:
4.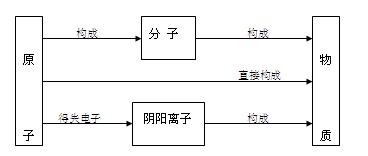
 物质由微粒构成
物质由微粒构成