
1.二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是
A.利用金属钠或金属钾 B.利用燃烧法 C.利用红外光谱法 D.利用核磁共振氢谱
2.下列有关实验叙述正确的是
A. 除去苯中混有的苯酚可加入浓溴水后过滤
B. 向酸性KMnO4溶液中滴加维生素C溶液,KMnO4溶液褪色,说明维生素C有还原性
C. 向淀粉溶液中滴加稀硫酸后,加热,再加入新制Cu(OH)2加热,没有出现红色沉淀,说明淀粉
没有发生水解反应
D. 向NaOH溶液中加入溴乙烷,加热,再加入AgNO3溶液,产生沉淀,说明溴乙烷发生了水解反应
3.下列物质的保存方法不正确的是
A.少量金属钠保存在煤油中 B.浓硝酸盛放在无色瓶中
C. 少量白磷保存在冷水中 D.氢氧化钠溶液盛放在橡胶塞的试剂瓶中
4.下列除杂质的方法不正确的是
A.氢氧化铁胶体中的铁离子和氯离子可用渗析法除去
B.硬脂酸钠中混有少量的甘油,用盐析法除去
C.乙酸乙酯中混有少量乙酸,用饱和碳酸钠溶液洗涤后分液
D.氯化钠中有少量氯化铵,加过量的烧碱溶液后加热蒸干
5.某有机物有如下性质:①能和银氨溶液共热得到银镜;②加入碳酸氢钠无变化;③与含酚酞的氢氧
化钠溶液共热,发现红色褪去。则该有机物可能是
 A.乙醇 B.乙醛
C.乙酸 D.甲酸乙酯
A.乙醇 B.乙醛
C.乙酸 D.甲酸乙酯
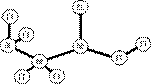
6.某期刊封面上有如下一个分子的球棍模型图。图中“棍”代表单键或双键或三键。不同颜色的球代表不同元素的原子,该模型图可代表一种
A.卤代羧酸 B.酯 C.氨基酸 D.醇钠
7.下列实验装置、试剂选用或操作正确的是
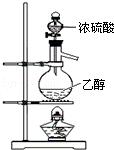
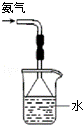

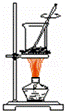
A. 实验室制乙烯 B. 用水吸收氨气 C. 稀释浓硫酸 D.海带灼烧成灰
8.下列实验操作符合要求的是
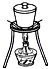
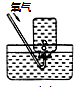
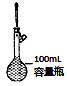
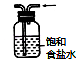
A. 定容 B. 收集氨气 C. 高温煅烧石灰石 D. 除去氯气中的氯化氢
9.除去下列物质中所含的杂质,选用的试剂正确的是
|
选项 |
物质(杂质) |
试剂 |
|
A |
Al2O3(SiO2) |
NaOH溶液 |
|
B |
FeCl2溶液(FeCl3) |
Fe粉 |
|
C |
CO2(SO2) |
Na2CO3溶液 |
|
D |
NaHCO3溶液(Na2CO3) |
Ca(OH)2溶液 |
10.右图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是
|
选项 |
X |
收集气体 |
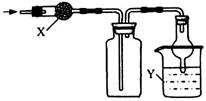 Y Y |
|
A |
碱石灰 |
氯化氢 |
水 |
|
B |
碱石灰 |
氨气 |
水 |
|
C |
氯化钙 |
一氧化氮 |
氢氧化钠 |
|
D |
氯化钙 |
二氧化硫 |
氢氧化钠 |
11.分子式为C5H12O并能与金属钠反应放出氢气的有机物有(不含立体异构)
A.6种 B.7种 C. 8种 D.9种
12.下列说法不正确的是
A.己烷有4种同分异构体,它们的熔点、沸点各不相同
B.甲醛能发生氧化反应、还原反应和聚合反应
C.油脂皂化反应得到高级脂肪酸盐与甘油
D.聚合物()可由单体CH3CH=CH2和CH2=CH2加聚制得
13.在下列条件下,两种气体的分子数一定相等的是
A.同密度、同压强的N2和C2H4 B.同温度、同体积的O2和N2
C.同体积、同密度的C2H4和CO D.同压强、同体积的O2和N2
14.下列说法正确的是
A.为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可.
B.做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸。如果在沸腾前发现忘记加沸石,应立即
停止加热,冷却后补加.
C.在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在
SO或SO
D.溴乙烷与NaOH乙醇溶液共热产生的气体通入KMnO4酸性溶液中,溶液褪色,说明产生的气体为
乙烯.
15.设NA为阿伏加德罗常数的值,下列说法正确的是
A.2.0gH218O与D2O的混合物中所含中子数为NA
B.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
C.标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5 NA
D.50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA
16.设NA为阿伏加德罗常数的值,下列说法正确的是
A.11.2 L Cl2与4.25 g NH3所含有的原子数一定相等
B.标准状况下36 g H2O与1.204×1024个O2分子所占的体积
C. 100 mL 0.1 mol/L AlCl3溶液中,Al3+个数为0.01NA
D. 0.1 mol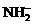 所含电子数约为6.02×1023个
所含电子数约为6.02×1023个
17.设NA为阿伏加德罗常数的数值,下列说法正确的是
A.18gH2O含有10 NA个质子 B.1mol己烷含有18NA个化学键
C. 22.4L氨水含有NA个NH3分子 D.56g铁片投入足量浓H2SO4中生成NA个SO2分子
18.下列说法正确的是
A.按系统命名法 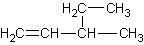 的名称为3-乙基-1-丁烯
的名称为3-乙基-1-丁烯
B.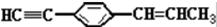 最多有7个碳原子在一条直线上。
最多有7个碳原子在一条直线上。
C.由2-氯丙烷制取1,2-丙二醇CH2CH(OH)CH2OH时,经过的反应消去→加成→取代
D.蛋白质和油脂都属于高分子化合物,一定条件下能水解
20.绿原酸的结构简式如图,下列有关绿原酸的说法不正确的是 ( )
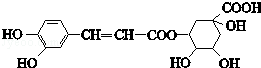
A. 分子式为C16H18O9 B. 能与Na2CO3反应
C. 能发生取代反应和消去反应 D. 0.1mol绿原酸最多与0.8molNaOH反应
21.K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O2 CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
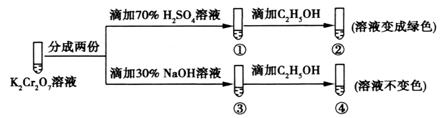
结合实验,下列说法不正确的是
A.①中溶液橙色加深,③中溶液变黄 B.②中Cr2O72-被C2H5OH还原
C.对比②和④可知K2Cr2O7酸性溶液氧化性强 D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色
22.用下列装置(尾气处理已略去)进行相关实验,能实现实验目的的是
|
|
实验目的 |
a中试剂 |
b中试剂 |
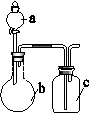 c中试剂 c中试剂 |
|
A |
比较H2CO3、H2SiO3的酸性 |
醋酸溶液 |
碳酸钠 |
硅酸钠溶液 |
|
B |
比较Cl2、I2的氧化性 |
浓盐酸 |
高锰酸钾 |
碘化钾溶液 |
|
C |
制备NaHCO3 |
盐酸 |
大理石 |
饱和碳酸钠溶液 |
|
D |
证明C2H2有还原性 |
饱和食盐水 |
电石 |
酸性高锰酸钾溶液 |
23.下列选项中的实验及现象得出的结论不正确的是)
|
|
实验 |
现象 |
结论 |
|
A |
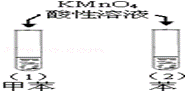 |
试管(1)中紫色消失,试管(2)中紫色没有消失 |
甲苯中苯环使甲基的活性增强 |
|
B |
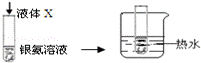 |
试管内壁有银镜生成 |
X具有还原性,且X一定属于醛 |
|
C |
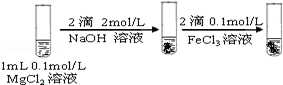 |
先生成白色沉淀,滴加FeCl3溶液后,生成红褐色沉淀 |
Fe(OH)3是比Mg(OH)2更难溶的电解质 |
|
D |
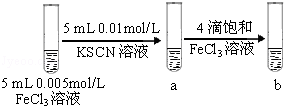 |
试管b比试管a中溶液的红色深 |
增大反应物浓度,平衡向正反应方向移动 |
24. 氢叠氮酸(HN3)与醋酸酸性相近。氢叠氮酸盐(NaN3)稳定,但撞击发生爆炸生成氮气。下列有关氢叠氮酸及其盐的说法中不正确的是
A.固体HN3属于分子晶体 B.HN3的水溶液呈弱酸性
氢叠氮酸(HN3)与醋酸酸性相近。氢叠氮酸盐(NaN3)稳定,但撞击发生爆炸生成氮气。下列有关氢叠氮酸及其盐的说法中不正确的是
A.固体HN3属于分子晶体 B.HN3的水溶液呈弱酸性
C.NaN3的水溶液呈酸性 D.NaN3可用于汽车防撞保护气囊
25.已知四种盐的溶解度(S)曲线如右图所示,下列说法不正确的是
A.将NaCl溶液蒸干可得NaCl固体
B.可用MgCl2和NaClO3制备Mg(ClO3)2
C.将MgCl2溶液蒸干可得MgCl2固体
D.Mg(ClO3)2中混有少量NaCl杂质,可用重结晶法提纯
桃江一中2017届高三第一次月考化学答卷(只交答卷)
姓名: 班级:
|
题目 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
|
答案 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
题目 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
24 |
25 |
|
|
答案 |
|
|
|
|
|
|
|
|
|
|
|
|
|
二 非选择题(共50分 )
26.(10 分)制印刷电路板的废液中含有大量的CuCl2、FeCl2和FeCl3,可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,实现循环使用.取废液按如下流程在实验室进行模拟实验: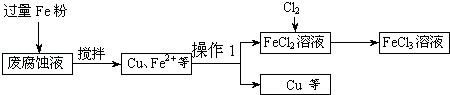
已知:铁氰化钾溶液与Fe2+反应生成带有特征蓝色的沉淀。
(1)操作1的名称是 .上述方法获得的铜粉中含有杂质,除杂所需的试剂是 。
(2)Cl2可用固体KClO3与浓HCl常温下反应制备,反应的化学方程式为
。
(3)图1是模拟实验制备Cl2并通入FeCl2溶液中获得FeCl3溶液过程的部分装置.

从图2中挑选所需的仪器,完成上述模拟实验装置设计,并画出简图(添加必要的塞子、玻璃导管、橡胶管.固定装置可略去),标明容器中所装试剂.写出Cl2通入FeCl2溶液中发生反应的离子方程式 .
(4)实验中,确认FeCl2已全部转化为FeCl3溶液的方法是
.
27.(14分、每空2分) 以下是某学习小组对乙二酸的某些性质进行研究性学习的过程:
[研究课题]探究乙二酸的某些性质
[查阅资料]乙二酸(HOOC-COOH)俗称草酸,草酸晶体的化学式为H2C2O4.2H2O;草酸在100℃时开始升华,157℃时大量升华,并开始分解;草酸蒸气在低温下可冷凝为固体;草酸钙不溶于水,草酸蒸气能使澄清石灰水变浑浊。
[提出猜想]
猜想一:乙二酸具有不稳定性
根据草酸晶体的组成,该小组同学猜想其受热分解产物为CO、CO2和H2O。 设计方案:⑴请用下列装置组成一套探究并验证其产物的实验装置(草酸晶体分解装置略,连接导管 略去)
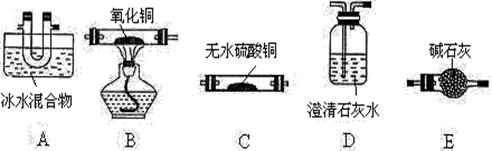
① 装置的连接顺序为:A→( )→D→( )→B→D (共2分)
② 实验时,在点燃B处酒精灯之前,应进行的操作是 。装置中碱石灰的作用是 。 检验产物中有CO的实验现象 是 。
③ 整套装置存在不合理之处为 。
猜想二:乙二酸具有弱酸性 设计方案:
⑵ 该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是 (填字母)。
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
猜想三:乙二酸具有还原性 设计方案:
(3) 该小组同学向酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色并
产生一种气体,从而判断草酸具有较强的还原性。该反应的离子方程式为
。
28.(10分)联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料。
(1)联氨分子的结构式为 ,其中氮的化合价为 。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为
。
(3)①2O2(g)+N2(g)=N2O4(l) △H1 ②N2(g)+2H2(g)=N2H4(l) △H2
③O2(g)+2H2(g)=2H2O(g) △H3 ④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol
上述反应热效应之间的关系式为△H4= ,联氨和N2O4可作为火箭推进剂的主要原因为 。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,(已知:N2H4+H+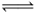 N2H5+的K=8.7×107;KW=1.0×10-14),联氨与硫酸形成的酸式盐的化学式为
。
N2H5+的K=8.7×107;KW=1.0×10-14),联氨与硫酸形成的酸式盐的化学式为
。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是
.联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2 kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 ____________________________________________________________________ 。
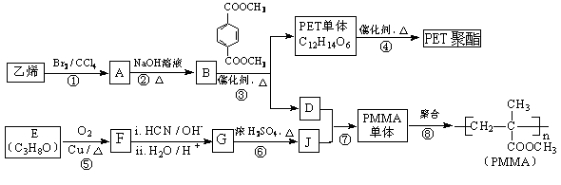
29.(16分)高分子材料PET聚酯树脂和PMMA的合成路线如下:
 已知:
已知:
Ⅰ. RCOOR’+ R’’18OH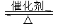 RCO18OR’’+R’OH(R、R’、R’’代表烃基)
RCO18OR’’+R’OH(R、R’、R’’代表烃基)
Ⅱ. 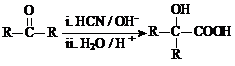 (R、R’代表烃基)
(R、R’代表烃基)
(1)①的反应类型是 。
(2)②的化学方程式为 。
(3)PMMA单体的官能团名称是 、 。
(4)F的核磁共振氢谱显示只有一组峰,⑤的化学方程式为
。
(5)G的结构简式为 。
(6)下列说法正确的是________(填字母序号)。
a.⑦为酯化反应 b.B和D互为同系物 c.D的沸点比同碳原子数的烷烃高
d. 1 mol 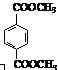 与足量NaOH溶液反应时,最多消耗4 mol NaOH
与足量NaOH溶液反应时,最多消耗4 mol NaOH
(7)J的某种同分异构体与J具有相同官能团,且为顺式结构,其结构简式是 。
(8)写出由PET单体制备PET聚酯并生成B的化学方程式
18 (1) ① 装置的连接顺序为:A→( C )→D→( E )→B→D (此问共2分)
② 应进行的操作是: 收集D处气体,检验CO气体的纯度。
装置中碱石灰的作用是: 除去气体中的CO2 和水,提高CO的浓度。
检验产物中CO的实验现象是: B中黑色固体变红色,D中澄清石灰水变浑浊。
③ 整套装置存在不合理之处为: 没有CO尾气的处理装置
(2) B、C
(3) 离子方程式: 2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O
12.有机物PAS﹣Na是一种治疗肺结核药物的有效成分,有机物G是一种食用香料,以甲苯为原料合成这两种物质的路线如下:
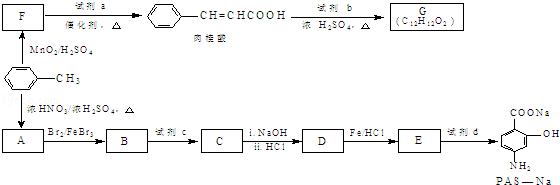
已知:①
②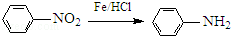
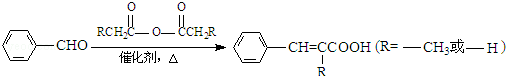
③
回答下列问题:
(1)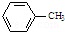 生成A的反应类型是 取代反应 .
生成A的反应类型是 取代反应 .
(2)F中含氧官能团的名称是 醛基 ;试剂a的结构简式为 H3COOOCCH3 .
(3)写出由A生成B的化学方程式: 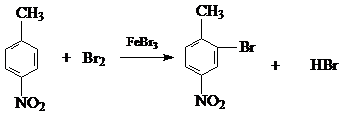 .
.
(4)质谱图显示试剂b的相对分子质量为58,分子中不含甲基,且为链状结构,写出肉桂酸与试剂b生成G的化学方程式: 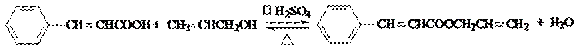
(5)当试剂d过量时,可以选用的试剂d是 C (填字母序号).
a.Na2CO3 b.NaOH c. NaHCO3
(6)写出C与NaOH反应的化学方程式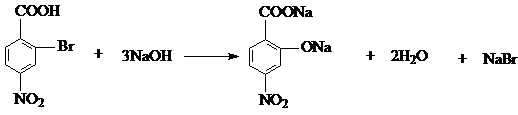 .
.
(7)肉桂酸有多种同分异构体,符合下列条件的有 6 种.
a.苯环上有三个取代基; b.能发生银镜反应,且1mol该有机物最多生成4mol Ag.
由上述符合条件的同分异构体中,写出苯环上有两种不同化学环境氢原子的有机物的结构简式(任写一种即可) 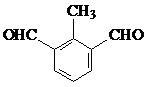 或
或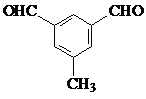 .
.