
1.下列有关乙醇的物理性质的应用中不正确的是( )
A.由于乙醇的密度比水小,所以乙醇中的水可以通过 分液的方法除去
分液的方法除去
 B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的 有效成分
有效成分
C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇容易挥发,所以才有俗语“酒好不怕巷子深”的说法
2.不能证明乙醇分子中有一 个氢原子与其他氢原子不同的方法是( )
个氢原子与其他氢原子不同的方法是( )
A.1 mol乙醇燃烧生成3 mol水
B.1 mol乙醇催化氧化生成1 mol乙醛
C.1 mol乙醇跟足量的钠反应得到0.5 mol H2
D.乙醇与水能以任意比互溶
3.下列关于羟基和氢氧根的说法中,不正确的是( )
A.羟基比氢氧根少一个电子
B.两者的组成元素相同
C.羟基不带电,氢氧根带一个单位负电荷
D.羟基比氢氧根性质稳定
4.向装有乙醇的烧杯中投入一小块金属钠,下列对该实验现象的描述中正确的是( )
A.钠块开始反应时,浮在乙醇液面的上面
B.钠块熔化成小球
C.钠块与乙醇的反应比钠块与水的反应剧烈
D.钠块表面有气体放出
5.(2015.东营高一检测)乙醇是一种比较理想的可再 生能源,目前新兴起的车用乙醇汽油就是掺加一定比例乙醇的汽油。下列说法中正确的是( )
生能源,目前新兴起的车用乙醇汽油就是掺加一定比例乙醇的汽油。下列说法中正确的是( )
A.在相同状况下,同体积的乙醇气体和乙烷气体都完全燃烧,耗氧量相同
B.在相同状况下,同体积的乙醇气体和乙烯气体都完全燃烧,放热量相同
C.用乙醇作燃料不会导致“温室效应”
D.用乙醇作燃料不会导致酸雨
6.如 图所示装置,持续通入X气体,可以看到a处有红色物质生成,b处变成蓝色,c处得到液体,则X
图所示装置,持续通入X气体,可以看到a处有红色物质生成,b处变成蓝色,c处得到液体,则X 气体可能是( )
气体可能是( )
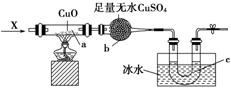
A.H2 B.CO和H2
C.NH3 D.CH3CH2OH(g)
7.在常压下和100 ℃条件下,把乙醇汽化为蒸气 ,然后和乙烯以任意比例混合,其混合气体为V L,将其完全燃烧,需消耗相同条件下的氧气的体积是( )
,然后和乙烯以任意比例混合,其混合气体为V L,将其完全燃烧,需消耗相同条件下的氧气的体积是( )
A.2V L B.2.5V L
 C.3V L D.无法计算
C.3V L D.无法计算
8.某饱和一元醇CnH2n+1OH 14.8 g和足量的金属钠反应生成氢气2.24 L(标准状况),则燃烧3.7 g该醇生成的水的物质的量为( )
A.0.05 mol B.0.25 mol
C.0.5 mol D.0.75 mol
9.为了探究乙醇和金属钠反应的原理,做了如下四 个实验:
个实验:
甲:向小烧杯中加入无水乙醇,再放入一小块金属钠,观察现象,并收集产生的气体。
乙:设法检验甲收集到的气体。
丙:向试管中加入3 mL水,并加入绿豆粒大小的金属钠,观察现象。
丁:向试管中加入3 mL乙醚(CH3CH2OCH2CH3),并加入绿豆粒大小的金属钠,发现无明显变化。回答以下问题:
(1) 乙中检验气体的实验方法_____________________________________,得出的结论是________________。
(2)从结论上分析,该实验选取水和乙醚做参照物的原因是_____________。
(3)丙的目的是欲证明__________________________;丁的目的是欲证明____________________________;根据丙和丁的结果,可以证明乙醇和金属钠反应的化学方程式应为_____________________________。
10.有关催化剂的催化机理等问题可 以从“乙醇催化实验”得到一些认识,某教师设计了下图所示装置(夹持装置
以从“乙醇催化实验”得到一些认识,某教师设计了下图所示装置(夹持装置 已省略),其实验操作为:先按图安装好实验装置,关闭活塞a、b、c,在铜网的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,有节奏(间歇性)地通入气体。在M处观察到明显的实验现象,试回答以下问题:
已省略),其实验操作为:先按图安装好实验装置,关闭活塞a、b、c,在铜网的中间部分加热片刻,然后打开活塞a、b、c,通过控制活塞a和b,有节奏(间歇性)地通入气体。在M处观察到明显的实验现象,试回答以下问题:
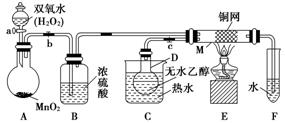
(1)A中发生反应的化学方程式为________________________________,B的作用是________,C中热水的作用是________________________。
(2)M处发生反应的总的化学方程式为_ ____________________________。
____________________________。
(3)从M管中可观察到的现象是_______________,从中可认识到该实验过程中催化剂________(填“参加”或“不参加”)化学反应,还可以认识到催化剂起催化作用需要一定的_____________________________。