
5.分子的性质
[考点归纳]
1.分子间作用力
(1)定义:物质分子之间普遍存在的相互作用力,称为分子间作用力。分子间作用力最常见的是范德华力和氢键,氢键不属于化学键,其强度比化学键弱得多,但它比范德华力稍强。(2)范德华力:范德华力主要影响物质的熔点、沸点、硬度等物理性质。范德华力越强,物质的熔点、沸点越高,硬度越大。一般来说组成和结构相似的物质,随着相对分子质量的增加,范德华力逐渐增大,如F2<Cl2<Br2<I2,CF4<CCl4<CBr4;同分异构体中,支链越多,范德华力越小;相对分子质量相近的分子,极性越大,范德华力越大。
(3)氢键:已经与电负性很强的原子形成共价键的氢原子(该氢原子几乎为裸露的质子)与另一个分子中电负性很强的原子之间的作用力,称为氢键。常用A-H…B表示氢键,A、B的电负性越大,B原子的半径越小,氢键的键能越大。氢键具有一定的方向性和饱和性,氢键包括分子内氢键和分子间氢键两种,分子间氢键的作用,形成的“缔合分子”增大了分子间作用力,使得物质的熔沸点升高(如水)、溶解度增大(如氨)、电离度降低(如氢氟酸为弱酸)等,由于分子内的氢键作用,形成具有“环状结构”的物质,减小了分子间的作用力,使物质的熔沸点降低、溶解度减小等。
[易错提醒]“几乎裸露的质子(H)”与“氮、氧、氟”原子之间才可能形成氢键,其他原子与氢原子不能形成氢键,例如乙醇(CH3CH2OH)甲基(-CH3)上的氢原子与水中的氧原子之间不能形成氢键。有氢键的分子间也有范德华力,但有范德华力的分子间不一定有氢键;一个氢原子只能形成一个氢键,这就是氢键的饱和性;氢键主要影响物质的物理性质。
2.分子极性的判断
(1)根据键的类型及分子的立体构型判断,非极性分子、极性分子的判断,首先看键是否有极性,然后再看各键的空间排列状况。键无极性,分子必无极性(O3除外);键有极性,各键空间排列均匀,使键的极性相互抵消,分子无极性;键有极性,各键空间排列不均匀,不能使键的极性相互抵消,分子有极性。
(2)根据中心原子最外层电子是否全部成键判断,分子中的中心原子最外层电子若全部成键,此分子一般为非极性分子;分子中的中心原子最外层电子若未全部成键,此分子一般为极性分子。如CH4、BF3、CO2等分子中的中心原子的最外层电子均全部成键,它们都是非极性分子。而H2O、NH3、NF3等分子中的中心原子的最外层电子均未全部成键,它们都是极性分子。
3.分子的性质
(1)分子的溶解性:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。若溶剂和溶质分子之间可以形成氢键,则溶质的溶解度增大(“相似相溶”的规律)。随着溶质分子中憎水基个数的增大,溶质在水中的溶解度减小。如甲醇、乙醇和水以任意比互溶,而戊醇在水中的溶解度明显减小。
(2)分子的手性:手性异构指的是具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为镜像,在三维空间里不能重叠的现象,具有手性异构体的分子叫手性分子,在有机物分子中,连有四个不同基团或原子的碳原子叫手性碳原子,含有手性碳原子的分子是手性分子,如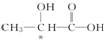 。
。
(3)无机含氧酸分子的酸性:无机含氧酸可写成(HO)mROn,如果成酸元素R相同,则n值越大,R的正电性越高,使R-O-H中O的电子向R偏移,在水分子的作用下越易电离出H+,酸性越强,如HClO<HClO2<HClO3<HClO4。无机含氧酸分子之所以能显示酸性,是因为其分子中含有-OH,而-OH上的H原子在水分子的作用下能够变成H+而显示一定的酸性。
[过关练习]
1.H2O2分子是含有________键和________键的______(填“极性”或“非极性”)分子,H2O2难溶于CS2的理由是:_____________。
2.氨的沸点________(填“高于”或“低于”)膦(PH3),原因是_________________________。
3.1 mol乙醛分子中含有σ键的数目为________,乙酸的沸点明显高于乙醛,其主要原因是___________________________。
4.已知苯酚(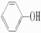 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________(填“>”或“<”)Ka(苯酚),其原因是________________________。
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)________(填“>”或“<”)Ka(苯酚),其原因是________________________。
5.比较下列锗卤化物的熔点和沸点,分析其变化规律及原因:________________。
|
|
GeCl4 |
GeBr4 |
GeI4 |
|
熔点/℃ |
-49.5 |
26 |
146 |
|
沸点/℃ |
83.1 |
186 |
约400 |
6.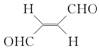 分子在水中的溶解度于2丁烯。
分子在水中的溶解度于2丁烯。
7.HCHO分子的立体构型为________形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质)_______________________________________。
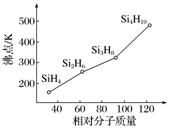
8.有一类组成最简单的有机硅化合物叫硅烷。硅烷的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是___________________。
9.在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型是_____杂化,不同层分子间的主要作用力是_______。
10.三氯化铁常温下为固体,熔点282 ℃,沸点315 ℃,在300 ℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体中存在的微粒间作用力有_______。
11.X、Y两者物理性质有差异的主要原因是__________。
|
代号 |
结构简式 |
水中溶解度/g(25 ℃) |
熔点/ ℃ |
沸点/ ℃ |
|
X |
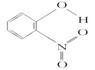 |
0.2 |
45 |
100 |
|
Y |
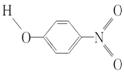 |
1.7 |
114 |
295 |
H2)2分子中C原子的杂化方式为_____,1mol该分子中σ键的数目为__________,该物质易溶于水的主要原因是_______________________________________________。
13.F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)===2ClF3(g) ΔH=-313 kJ.mol-1,F-F键的键能为159 kJ.mol-1,Cl-Cl键的键能为242 kJ.mol-1,则ClF3中Cl-F键的平均键能为________kJ.mol-1。ClF3的熔、沸点比BrF3的________(填“高”或“低”)。
14.一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。
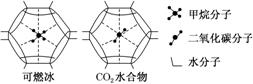
“可燃冰”中分子间存在的2种作用力是________。为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0.586nm,根据下述图表,从物质结构及性质的角度分析,该设想的依据是______________________。
|
参数 |
|
|
|
分子 |
分子直径/nm |
分子与H2O的结合能 |
|
E/kJ.mol-1 |
|
|
|
CH4 |
0.436 |
16.40 |
|
CO2 |
0.512 |
29.91 |
15.维生素B1的结构式如图,晶体溶于水的过程中要克服的微粒间作用力有________。
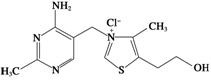
高三化学 考点点点过 5.分子的性质(选修3)参考答案
参考答案
1.[解析]H2O2是极性分子,分子内既有极性键,又有非极性键,而CS2为非极性分子,根据“相似相溶”规律,H2O2难溶于CS2。
[答案]极性 非极性 极性H2O2为极性分子,而CS2为非极性溶剂,根据“相似相溶”规律,H2O2难溶于CS2
2.[解析]氨分子之间形成氢键,分子间作用力增大,故沸点高于膦(PH3)
[答案]高于 NH3分子间可形成氢键
3.6NA CH3COOH分子间存在氢键
4.<  中形成分子内氢键,使其更难电离出H+
中形成分子内氢键,使其更难电离出H+

6.[解析]该有机物分子易与水分子形成分子间氢键,而2丁烯则不能,故该有机物在水中的溶解度大于2丁烯
[答案]大
7.平面三角 加成产物CH3OH分子之间能形成氢键
8.硅烷为分子晶体,随相对分子质量增大,分子间作用力增强,熔沸点升高
9.[解析]由于该晶体具有和石墨相似的层状结构,所以B原子采取sp2杂化,同层分子间的作用力是范德华力,由于“在硼酸[B(OH)3]分子中,B原子与3个羟基相连”虽然三个B-O都在一个平面上,但σ单键能够旋转,使O-H键位于两个平面之间,因而能够形成氢键,从而使晶体的能量最低,达到稳定状态。
[答案]sp2,氢键
10.极性共价键、范德华力
11.N、O、F X物质形成分子内氢键,Y物质形成分子间氢键,分子间氢键使分子间作用力增大
12.sp2 7NACO(NH2)2分子与水分子之间能形成氢键
 [答案]172 低
[答案]172 低
14.[解析]可燃冰中存在分子间作用力即范德华力,另外水分子间还存在氢键。分子与H2O的结合能越大表明越容易与H2O结合。
[答案]氢键、范德华力 CO2的分子直径小于笼状结构空腔直径,且与H2O的结合能大于CH4
15.离子键、氢键、范德华力