
1.下列说法不正确的是
A.雷雨时,可增加土壤中硝酸盐类氮肥的含量
B.许多领域中用液氮制得低温环境
C.造成光化学烟雾的罪魁祸首是SO2
D.正常雨水因溶有CO2,其pH约为5.6,而酸雨的pH小于5.6
[答案]C
2. 硅及其化合物是重要的无机材料,下列有关说法正确的是
硅及其化合物是重要的无机材料,下列有关说法正确的是
A.反应SiO2+2C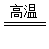 2CO↑+Si,每生成1 mol Si转移4 mol e−
2CO↑+Si,每生成1 mol Si转移4 mol e−
B.光纤的主要成分是硅单质,它质量轻且对光的传输能力强
C.光纤可以将光能转化为电能,是制造光电池的最佳材料
D.陶瓷、水泥、金刚砂及所有的玻璃都是硅酸盐产品
[答案]A
[解析]标出选项A反应前后元素的化合价,分析反应前后化合价的变化,可知A说法正确;光纤是光导纤维的简称,其主要成分是二氧化硅,B说法错误;制造光电池的材料是晶体硅,C说法错误;金刚砂的主要成分是碳化硅,石英玻璃的主要成分是二氧化硅,都不是硅酸盐产品,故D说法错误。
3.下列叙述正确的是
A.Na2SiO3是硅酸盐,但不能溶于水
B.电影银幕用水玻璃浸泡,主要是为了防腐
C.建筑工业常用水玻璃作黏合剂
D.用水玻璃浸泡铁道的木制枕木,主要是为了防火
[答案]C
[解析]Na2SiO3既是硅酸盐,又是钠盐,硅酸盐大多难溶于水,而钠盐均易溶于水;浸泡银幕主要是为了防火,而浸泡枕木主要是为了防腐;水玻璃有黏合作用,常作黏合剂。
4.用氧化物的形式表示硅酸盐的组成,不正确的是
A.钙沸石[Ca(Al2Si3O10).3H2O]:CaO.Al2O3.3SiO2.3H2O
B.镁橄榄石(Mg2SiO4):2MgO.SiO2
C.钾云母(K2H4Al6Si6O24):K2O.2H2O.3Al2O3.6SiO2
D.高岭石[Al2(Si2O5)(OH)4]:Al2O3.2SiO2.2H2O
[答案]C
5. 下面对氯的叙述,正确的是
下面对氯的叙述,正确的是
A.液氯可使湿的红布条褪色,所以液氯具有漂白性
B.氯气没有漂白性,但通入品红溶液中,品红的红色褪去
C.在通常情况下,氯气可以和任何金属直接化合
D.氯气有毒,可以用澄清的石灰水吸收尾气;久置的氯水最终变为稀盐酸
[答案]B
[解析]次氯酸具有漂白性,液氯没有漂白性,A项错误;氯气没有漂白性,但通入品红溶液中,氯气和水反应生成的次氯酸使品红褪色,B项正确;在点燃或加热的情况下,氯气可以和大多数金属直接化合,C项错误;氯气有毒,可以用氢氧化钠溶液吸收尾气,而澄清石灰水浓度太小,吸收效果不好,D项错误。
6.将紫色石蕊溶液滴入NaOH溶液中,溶液变蓝色,再通入氯气,溶液由蓝色先变成红色,最后颜色慢慢褪去,其原因是
①氯气有漂白性 ②氯气与NaOH溶液反应 ③氯气的水溶液呈酸性 ④次氯酸有漂白性
⑤氯化钠有漂白性
A.①④ B.②③④ C.①②③ D.④⑤
[答案]B
[解析]Cl2与NaOH溶液反应生成NaCl和NaClO,当Cl2过量时,Cl2与水反应生成HCl和HClO,溶液呈酸性,因此使石蕊变红色,而HClO有漂白性,又使溶液褪色。
7.下列说法正确的是
A.因为SO2具有漂白性,所以它能使品红溶液、溴水、KMnO4(H+)、石蕊溶液褪色
B.能使品红溶液褪色的不一定是SO2
C.SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同
D.SO2和Cl2等物质的量混合后同时通入装有湿润的有色布条的集气瓶中,漂白效果更好
[答案]B
8. 下列制取SO2、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的的是
下列制取SO2、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的的是
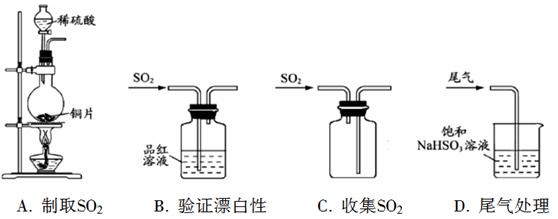
[答案]B
[解析]A、铜和稀硫酸不反应,选项A错误;B、二氧化硫可使品红溶液褪色,选项B正确;C、二氧化硫密度比空气大,应将进气管伸到瓶底,用向上排空气法收集,选项C错误;D、二氧化硫在饱和亚硫酸氢钠溶液中溶解度很小,不可用于吸收尾气,选项D错误。答案选B。
9.下面是实验室制取氨气的装置和选用的试剂,其中错误的是
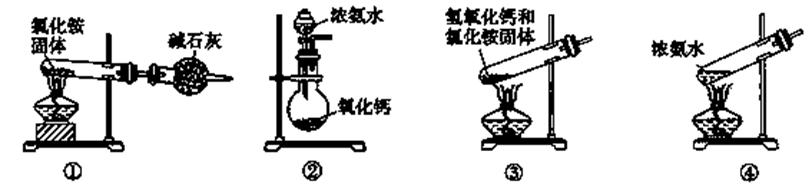
A.①③ B.②③ C.①④ D.②④
[答案]A
[解析]实验室用铵盐与碱加热制取氨气,常用NH4Cl与Ca(OH)2反应,固体与固体反应,因为有水生成,试管口应向下倾斜,③错误。在浓氨水中加入CaO,CaO与水反应放出大量的热,使NH3.H2O分解放出氧气;加热浓氨水,加快氨气挥发,②④正确。①是错误的,因为氯化铵分解生成的NH3与HCl冷却后会重新生成NH4Cl,不能得到NH3。
10.氮的多样性主要体现在含氮化合物及其性质的多样性上,下列说法正确的是
A.Fe2+、Mg2+、Cl−、 能大量共存于pH=0的溶液中
能大量共存于pH=0的溶液中
B.1 L浓度为1 mol.L−1的氨水中含有NA个NH3.H2O
C.除去Cu粉中混有的CuO,向混合物中滴加适量稀硝酸
D.不论是浓硝酸还是稀硝酸,与铜反应均体现出硝酸的酸性和强氧化性
[答案]D

11.在给定条件下,下列选项所示的物质间转化均能实现的是
A.Fe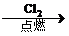 FeCl2
FeCl2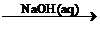 Fe(OH)2
Fe(OH)2
B.S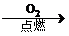 SO3
SO3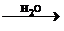 H2SO4
H2SO4
C.CaCO3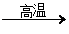 CaO
CaO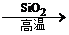 CaSiO3
CaSiO3
D.NH3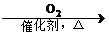 NO
NO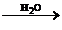 HNO3
HNO3
[答案]C
[解析]A.铁与氯气反应只能生成氯化铁,A错误;B.硫在空气或氧气中燃烧只能生成二氧化硫,B错误;C.两步均能实现,C正确;D.NO不与H2O反应,D错误。
12.下列离了方程式表达正确的是
A.铜片溶于稀硝酸产生无色气体:Cu+4H++2 ===Cu2++2NO2↑+H2O
===Cu2++2NO2↑+H2O
B.将铁粉加人稀硫酸中:2Fe+6H+===2Fe3++3H2↑
C.硫酸亚铁酸性溶液中加入过氧化氢:2Fe2++ H2O2+2H+===2Fe3++2H2O
D.向NaClO溶液中通入少量SO2:2ClO−+SO2+H2O
=== 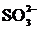 +2HClO
+2HClO
[答案]C
[解析]A项,铜片溶于稀硝酸产生无色气体应为NO,正确的离子方程式为:3Cu+8H++2 ===3Cu2++2NO↑+4H2O,故A错误;B项,铁与稀硫酸反应生成Fe2+,正确的离子方程式为:Fe+2H+===Fe2++H2↑,B错误;C项,Fe2+在酸性条件下被H2O2氧化成Fe3+,H2O2中−1价O被还原,离子方程式为:2Fe2++ H2O2+2H+===2Fe3++2H2O,C正确;D项,ClO−与SO2发生氧化还原反应,因为SO2少量,所以剩余ClO−会结合H+生成HClO,故反应的离子方程式为:3ClO−+SO2+H2O===Cl−+2HClO+
===3Cu2++2NO↑+4H2O,故A错误;B项,铁与稀硫酸反应生成Fe2+,正确的离子方程式为:Fe+2H+===Fe2++H2↑,B错误;C项,Fe2+在酸性条件下被H2O2氧化成Fe3+,H2O2中−1价O被还原,离子方程式为:2Fe2++ H2O2+2H+===2Fe3++2H2O,C正确;D项,ClO−与SO2发生氧化还原反应,因为SO2少量,所以剩余ClO−会结合H+生成HClO,故反应的离子方程式为:3ClO−+SO2+H2O===Cl−+2HClO+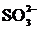 ,D错误。
,D错误。
13.下图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是
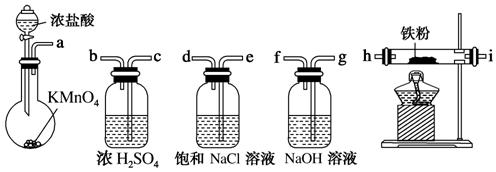
A.a-b-c-d-e-e-f-g-h
B.a-e-d-c-b-h-i-g
C.a-d-e-c-b-h-i-g
D.a-c-b-d-e-h-i-f
[答案]B
[解析]按制气→除HCl→除H2O→制备FeCl3→吸收Cl2顺序连接。
14.在一定温度和压强下,将一个容积为15 mL的试管充满NO2后,倒置于一个盛水的水槽中,当试管内液面上升至一定高度不再变化时,相同条件下再通入O2,若要使试管内液面仍保持在原高度,则应通入O2体积为
A.3.75 mL B.7.5 mL C.8.75 mL D.10.5 mL
[答案]C
15.(9分)为了探究新制饱和氯水的组成和性质而进行了下列科学实验,请根据要求回答问题:
(1)请写出新制饱和氯水中含有氯元素的物质的化学式:______________________________。
(2)若不再进行更多的实验,请说明能快速判断氯水中含有Cl2的主要依据:_________________。
(3)取适量新制饱和氯水滴入品红溶液后褪色,可得出氯气与水反应的产物具有漂白性,请你评价该结论是否合理?________。若不合理,请说明理由(若合理,则无需填写):_______________________。
(4)先观察了氯水的外观性质以后,又用胶头滴管将该氯水逐滴滴入含有酚酞的NaOH溶液中,边滴边振荡,并连续观察现象,发现溶液的红色逐渐褪去而得无色溶液。根据预测,实验中溶液红色褪去的原因可能有两种,请用简要的文字说明:
①_________________________________________________。
②_________________________________________________。
他们又要通过实验进一步探究溶液红色褪去的原因究竟是上述中的①还是②。
[实验步骤]
①取试管内的无色溶液3 mL盛于另一支洁净的试管中;
②______________________________,振荡试管。
[实验现象及结论]
①若________,则证明溶液红色褪去的原因是①而不是②;
②若________,则证明溶液红色褪去的原因是②而不是①。
[答案](1)Cl2、HCl(或Cl−)、HClO(1分)
(2)氯水显浅黄绿色(1分)
(3)不合理(1分) 没有事先证明干燥的氯气无漂白性(1分)
(4)①HCl和HClO中和了NaOH(1分) ②HClO氧化了酚酞(1分)
[实验步骤]②再向试管内滴加2滴NaOH溶液(1分)
[实验现象及结论]①恢复红色(1分) ②仍为无色(1分)
 主的HClO。可滴加NaOH溶液来验证红色褪去的原因。滴入少量NaOH后溶液显红色,说明还存在酚酞,红色褪去的原因是HCl和HClO与NaOH发生了反应;若加入NaOH不再显红色,说明溶液中不存在酚酞,即酚酞已被HClO氧化。
主的HClO。可滴加NaOH溶液来验证红色褪去的原因。滴入少量NaOH后溶液显红色,说明还存在酚酞,红色褪去的原因是HCl和HClO与NaOH发生了反应;若加入NaOH不再显红色,说明溶液中不存在酚酞,即酚酞已被HClO氧化。
16.(12分)A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
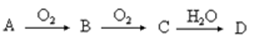
(1)若A为H2S,D的水溶液能使湿润的蓝色石蕊试纸变红,B为刺激性气味气体,写出B→C转化的化学反应方程式:________________________________________。
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红:A的化学式为______,实验室制备气体A的化学反应方程式__________________________,A→B转化的化学方程式为_____________________________________________________。
(3)若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,则B是(填化学式)________, C可作为呼吸面具的填充剂,C与二氧化碳发生反应的化学方程式为________________________________,C与水发生反应的离子方程式为___________________________________________________。
[答案](1)2SO2+O2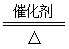 2SO3(2分)
2SO3(2分)
(2)NH3(1分) 2NH4Cl+Ca(OH)2
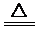 CaCl2+2NH3↑+ 2H2O(2分) 4NH3+5O2
CaCl2+2NH3↑+ 2H2O(2分) 4NH3+5O2 4NO + 6H2O(2分)
4NO + 6H2O(2分)
(3)Na2O(1分) 2Na2O2+2CO2===2Na2CO3+O2(2分) 2Na2O2+2H2O===4Na++4OH−+ O2↑(2分)

17.(9分)某研究性学习小组同学拟分析某市空气的质量情况,测定该市空气中SO2的含量并制定下列研究方案:
Ⅰ.资料表明,SO2具有较强的还原性,能与高锰酸钾酸性溶液发生反应:5SO2+2 +2H2O===5
+2H2O===5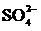
+2Mn2++4H+。
Ⅱ.设计实验方案:利用SO2的还原性使SO2和已知浓度及体积的高锰酸钾酸性溶液反应。
Ⅲ.选择分析地点:某工业区、某公园、某居民小区、某商业区、某交通枢纽。
Ⅳ.选择分析时间:晴天、风速较小时;晴天、风速较大时;雨前;雨后。
Ⅴ.对测定的结果进行初步分析并向相关单位提出建议。
(1)该小组同学拟用如图所示装置定量分析空气中SO2的含量。
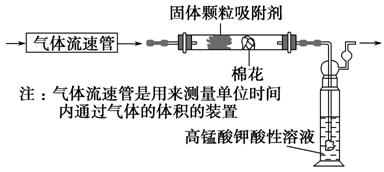
①通入空气前应进行的实验操作是________________________________;
②当观察到实验的现象为________________________________________时,应停止通空气;
③实验过程中需测量并记录的数据是_________________________________。
(2)如图表示该小组同学根据实验测得的该市不同地区空气中SO2的含量。
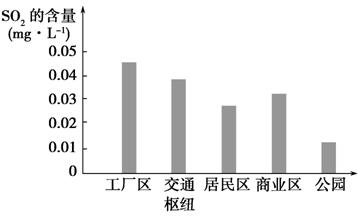
①工厂区、交通枢纽SO2含量明显高于其他地区的原因是_____________;
②请向当地有关部门提出一条减少工厂区SO2排放的建议:__________________________。
(3)下表是该小组同学测得的不同天气情况下的城市空气中SO2的平均含量。请分析雨后或风速较大时SO2平均含量较低的原因:
①_____________________________________________________;
②_____________________________________________________。
|
天气情况 |
平均风速(m.s−1) |
空气中SO2的平均含量(mg.L−1) |
|
雨前 |
2.0 |
0.03 |
|
雨后 |
2.2 |
0.01 |
|
晴 |
23 |
0.015 |
|
晴 |
0.9 |
0.03 |
[答案](1)①检查装置的气密性(1分)
②高锰酸钾酸性溶液刚好褪色(1分)
③通入空气至高锰酸钾酸性溶液刚好褪色所需要的时间(1分)
(2)①工厂尾气、汽车尾气中SO2含量较高(1分)
②提高脱硫技术(或改用更洁净的能源或提高尾气的处理技术或对尾气进行综合利用等合理答案均可) (1分)
(3)①下雨时SO2与水反应降低了雨后空气中SO2的含量(2分)
②风速越大,气体扩散速度越大,空气中SO2浓度越小(2分)

18.(8分)将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
(1)NO、NO2的体积分别为_________、__________。
(2)待产生的气体全部逸出后,向溶液中加入V mL a mol.L−1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原HNO3溶液的浓度为________。
[答案](1) 5.824 L(2分) 5.376 L (2分)
(2) 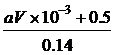 mol.L−1 (4分)
mol.L−1 (4分)
[解析](1)设生成NO的物质的量为x,NO2的物质的量为y。
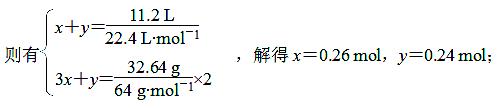
则V(NO)=0.26 mol×22.4 L.mol−1=5.824 L;
V(NO2)=0.24 mol×22.4 L.mol−1=5.376 L。
(2)由原子守恒得:
n(HNO3)=n(气体) +n(NaOH)
所以c(HNO3)=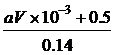 mol.L−1。
mol.L−1。