
1.2016年12月,中共中央、国务院印发了《关于全面推行河长制的意见》,进一步加强水污染治理工作。下列做法不应该提倡的是
A.用碱性废水中和处理酸性废水
B.将工业废液排入海洋以减少河道污染
C.生活污水无害化处理后用于绿化灌溉
D.推广使用高效、低毒农药,减轻水体污染
2.下列有关物质的性质与用途具有对应关系的是
A.明矾易溶于水,可用作净水剂
B.氢氧化铝具有两性,可用于治疗胃酸过多
C.二氧化硅的熔沸点很高,可用于光导纤维
D.氢氧化镁受热分解吸热且生成熔点高的MgO,可用做灭火材料
3.下列物质的转化在给定条件下能实现的是
A.NaCl(aq) NaHCO3(s)
NaHCO3(s) Na2CO3(s)
Na2CO3(s)
B.CuCl2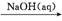 Cu(OH)2
Cu(OH)2 Cu
Cu
C.Al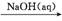 NaAlO2(aq)
NaAlO2(aq) NaAlO2(s)
NaAlO2(s)
D.MgO(s) Mg(NO3)2(aq)
Mg(NO3)2(aq) Mg(s)
Mg(s)
4.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.在含有大量HCO3―的溶液中:Na+、NO3-、Cl-、AlO2-
B. 0.1mol.L-1Ca(ClO)2 溶液:K+、Na+、I-、Cl-
C.pH=1的溶液:Al3+、Ag(NH3)2+、Cl-、SO42-
D.加入KSCN 显红色的溶液:Na+、Mg2+、Cl-、SO42-
5.下列指定反应的离子方程式正确的是
A.漂白粉中加入浓盐酸:ClO-+Cl-+2H+ Cl2↑+H2O
Cl2↑+H2O
B.氯化铝溶液中加入过量氨水:Al3++4NH3.H2O AlO2-+4NH4++2H2O
AlO2-+4NH4++2H2O
C.等物质的量的MgCl2、Ba(OH)2和HCl溶液混合:Mg2++2OH- Mg(OH)2↓
Mg(OH)2↓
D.硫酸氢钠溶液与氢氧化钡溶液恰好反应呈中性:
H++SO42-+Ba2++OH- H2O+BaSO4↓
H2O+BaSO4↓
6.巧妙的实验设计有助于更好地解决问题。下列装置不能达到实验目的的是

A. 用装置甲验证HCl气体易溶于水
B.用装置乙验证SO2具有漂白性
C.装置丙中X若为四氯化碳,可用于吸收氨气,并防止倒吸
D. 用装置丁检验NH4Cl分解产生的气体
7.下列物质的性质、用途正确的是
A.合金的硬度大,熔点也高
B.Na2SiO3是制备硅胶和木材防火剂的原料
C.浓硫酸、浓硝酸都具有强氧化性,不能盛放在金属容器中
D.二氧化硫具有还原性,浓硫酸具有强氧化性,所以不能用浓硫酸干燥二氧化硫
8.在pH=2的透明溶液中,下列各组离子能大量共存的是
A.NH4+、Ca2+、HCO3-、Cl- B.K+、AlO2-、NO3-、CO32-
C.Na+、Cu2+、Br-、SO42- D.Al3+、Fe2+、SO42-、NO3-
9.下列说法正确的是
A.过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2NA
B.因硝酸铵受热易分解爆炸,实验室常用加热氯化铵固体的方法制备氨气
C.测定氯水pH时,可用pH试纸蘸取少量待测液,并与标准比色卡比较
D.向氢氧化钠中逐滴加入FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热,即制
得Fe(OH)3胶体
10.通过以下反应可获得新型能源二甲醚(CH3OCH3)。下列说法不正确的是
①C(s) +H2O(g)═CO(g)+H2(g) △H1=a kJ•mol﹣1
②CO(g)+H2O(g)═CO2(g)+H2(g) △H2=b kJ•mol﹣1
③CO2(g)+3H2(g)═CH3OH(g)+H2O(g) △H3=c kJ•mol﹣1
④2CH3OH(g)═CH3OCH3(g)+H2O(g) △H4=d kJ•mol﹣1
A.反应①、②为反应③提供原料气
B.反应③也是 CO2资源化利用的方法之一
C.反应CH3OH(g)═0.5CH3OCH3(g)+0.5H2O(l)的 △H=d/2kJ•mol﹣1
D.反应 2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)的 △H=(2b+2c+d ) kJ•mol﹣1
11.下列离子方程式书写正确的是
A.向Mg(OH)2悬浊液中加入FeCl3溶液:3OH- + Fe3+ == Fe(OH)3↓
B.淀粉碘化钾溶液在空气中变蓝:4I-+O2+2H2O == 4OH-+2I2
C.用FeSO4除去酸性废水中的Cr2O:Cr2O+Fe2++14H+===2Cr3++Fe3++7H2O
D.次氯酸钠溶液中通入少量二氧化硫气体:2ClO- + SO2 + H2O == 2HClO + SO32-
12.根据下列实验操作和现象所得到的结论正确的是
|
选项 |
实验操作和现象 |
结论 |
|
A |
室温下,向硅酸钠溶液中通入适量CO2,溶液变浑浊 |
碳酸的酸性比硅酸的强 |
|
B |
室温下,向FeCl3溶液中加入少量铜粉,铜粉溶解 |
Cu的还原性比Fe的强 |
|
C |
某溶液中加入盐酸酸化的氯化钡溶液产生白色沉淀 |
该溶液中含SO42- |
|
D |
某溶液中加入氢氧化钠浓溶液,未产生能使湿润的红色石蕊试纸变蓝的气体。 |
该溶液中无NH4+ |
13.甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(部
分产物已略去),下列各组物质中不能按图示关系转化的是
|
选项 |
物质转化关系 |
甲 |
乙 |
丙 |
丁 |
|
A |
 |
NaOH |
NaHCO3 |
Na2CO3 |
CO2 |
|
B |
C |
CO
|
CO2 |
O2 |
|
|
C |
Fe |
Fe(NO3)3 |
Fe(NO3)2 |
HNO3 |
|
|
D |
AlCl3 |
NaAlO2 |
Al(OH)3 |
NaOH |
14.①14Cu2++5FeS2+12H2O=7Cu2S+5Fe2++24H++3SO42-
②Mn2++S2O82-+H2O=MnO4-+SO42-+ H+
对上述两个反应判断正确的是
A.①②反应中SO42-都是氧化产物
B.两个反应中电子转移数目都是10mol
C.①反应中的硫元素部分被氧化,部分被还原
D.氧化性:S2O82- > MnO4-
15.已知:SO32-+I2+H2O SO42-+2I-+2H+。某溶液中可能含有Na+、NH4+、Fe2+、K+、I-、SO32- 、SO42-,且所有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是
SO42-+2I-+2H+。某溶液中可能含有Na+、NH4+、Fe2+、K+、I-、SO32- 、SO42-,且所有离子物质的量浓度相等。向该无色溶液中滴加少量溴水,溶液仍呈无色。下列关于该溶液的判断正确的是
A.肯定不含I- B.肯定不含SO42-
C. 肯定含有SO32- D.肯定含有NH4+
16. (14分)X、Y、Z、W四种化合物均由短周期元素组成。其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有右图转化关系(部分反应物、产物及反应条件已略去)。请回答:
(14分)X、Y、Z、W四种化合物均由短周期元素组成。其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无味气体。这四种化合物具有右图转化关系(部分反应物、产物及反应条件已略去)。请回答:
(1)Y的电子式是 。
(2)X与Y在溶液中反应的离子方程式是 。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。
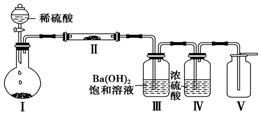
①装置Ⅰ中反应的化学方程式是 ,
装置Ⅱ中反应的化学方程式是 。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是 ,所需仪器装置是 。 (从上图选择必要装置,填写编号)。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时生成X,该反应的化学方程式是 。
17.(14分)铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:
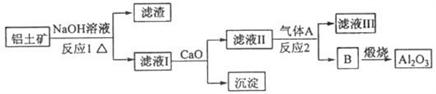
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:

回答下列问题:
(1)写出反应1的化学方程式 , 。
(2)滤液Ⅰ中加入CaO生成的沉淀是 ,反应2中通入过量气体A的离子方程式为 。
(3)E可作为建筑材料,化合物C是 ,写出由D制备冰晶石的化学方程式 。
(4)电解制铝的化学方程式是 。
18.(14分)氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl微溶于水,不溶于稀酸,可溶于Cl-浓度较大的体系,在潮湿的空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:

(1)溶解步骤的温度控制在60~70℃,原因是防止温度过高 、防止温度过低 。该步骤中Cu 与NH4NO3反应的离子方程式为 (N元素被还原到最低价) 。
 (2)还原步骤发生反应的离子方程式为
。
(2)还原步骤发生反应的离子方程式为
。
(3)滤液的主要成分为 (写化学式),洗净过滤所得固体应选用 (填序号)。
A.盐酸 B.硫酸 C.硝酸
(4)(NH4)2SO3的用量与Cu2+沉淀率的关系如图5所示,工业上n[(NH4)2SO3]/n(Cu2+)采用0.6最为适宜,此时(NH4)2SO3略过量,其原因是 。
19.(16分)(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下,回答下列问题:

①操作Ⅰ、Ⅱ的名称分别是 、 。写出滤液中加稍过量的NH4HCO3溶液的离子方程式 。
②写出在空气中煅烧FeCO3的化学方程式 。
(2)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定。
5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
a. 称取3.000g绿矾(FeSO4.7H2O)产品,溶解,在250mL容量瓶中定容;
b. 量取25.00mL待测溶液于锥形瓶中;
c. 用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①在实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯外,还需要的仪器 、 。
②计算上述样品中FeSO4.7H2O的质量分数。(写出计算过程,结果保留四位有效数字。)
20.(10分)辉铜矿的主要成分是Cu2S,可用于制取金属铜和铜盐。
(1)己知部分反应的热化学方程式如下:
C(s)+S2(g) =CS2(g) ΔH1=akJ.mol-1
Cu2S(s)+H2(g)=2Cu(s)+H2S(g) ΔH2=bkJ.mol-1
2H2S(g)=2H2(g)+S2(g) ΔH3=ckJ.mol-1
则C(s)+2Cu2S(s)=4Cu(s)+CS2(g)的ΔH= kJ.mol-1(用含 a、b、c 的代数式表示)。
(2)从辉铜矿中浸取铜元素,可用FeCl3作浸取剂。
①反应Cu2S+4FeCl3=2CuCl2+4FeCl2+S,每生成Imol CuCl2,反应中转移电子的物质的量为 ;浸取时,在有氧环境下可维持Fe3+较高浓度。有关反应的离子方程式是 。
②浸取过程中加入洗涤剂溶解硫时,铜元素的浸取率的变化见图1。其原因是 。

③353K时,向FeCl3浸取液中加入CuCl2,能加快铜元素的浸取速率,其反应原理可用化学方程式表示为: , CuCl+FeCl3=CuCl2+FeCl2。
21. (12分)Ni2+与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验Ni2+。

(1) Ni2+基态核外电子排布式为____________。
(2) 1 mol丁二酮肟分子中含有σ键的数目为________mol。
(3) 丁二酮肟镍分子中碳原子的杂化轨道类型为__________。
(4) Ni(CO)4是一种无色液体,沸点为43℃,熔点为-19.3 ℃。Ni(CO)4的晶体类型是________。
(5)与CO互为等电子体的二价阴离子为____________,Ni(CO)4中Ni与CO的C原子形成配位键,不考虑空间构型,Ni(CO)4的结构可用示意图表示为____________。