
1.下列能量的转化过程中,属于化学变化的是 ( )
A.水力发电 B.煤燃烧发电 C.太阳能热水器提供热水 D.电取暖器取暖
2.保护我们生存的环境是全人类都必须重视的问题。下列做法与环境保护无关的是( )
A.锅炉用水经过软化后再使用 B.农业上合理使用农药和化肥
C.工业污水经过处理后再排放 D.公交车用压缩天然气作燃料
3. 物质是由各种粒子构成的。若用“ ”表示水分子。下列从粒子的角度对物质的变化或性质作出的解释中错误的是( )
物质是由各种粒子构成的。若用“ ”表示水分子。下列从粒子的角度对物质的变化或性质作出的解释中错误的是( )
 A.湿衣服晾干了是因为“ ”不断运动到空气中去了
A.湿衣服晾干了是因为“ ”不断运动到空气中去了
 B.氧气经加压降温变为蓝色液体时,“ ”间的间隔减小了
B.氧气经加压降温变为蓝色液体时,“ ”间的间隔减小了

 C.水通电分解时“ ”和“ ”发生了重新组合
C.水通电分解时“ ”和“ ”发生了重新组合
 D.保持氢气化学性质的最小粒子是“ ”
D.保持氢气化学性质的最小粒子是“ ”
4.钛和钛的合金被认为是21世纪重要的金属材料,具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工,钛合金与人体有很好的“相容性”。根据钛的上述性质,下列的用途不切合实际的是( )
A.用于制造船舶 B.用于制造航天器
C.用于作保险丝 D.用于制造人造骨
5.下列反应的化学方程式书写正确的是( )
A.细铁丝在氧气中燃烧:4Fe
+ 3O2 2Fe2O3
2Fe2O3
B.铁与稀盐酸反应:2Fe + 6HCl = 2FeCl3 + 3H2↑
C.不能用铁制容器配制波尔多液的原因:2Fe + 3CuSO4 = Fe2(SO4)3 + 3Cu
D.用赤铁矿炼铁Fe2O3
+ 3CO 2Fe + 3CO2
2Fe + 3CO2
6.由于温度降低到可燃物着火点以下而使火焰熄灭的是( )


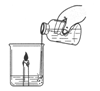


A B C D
7.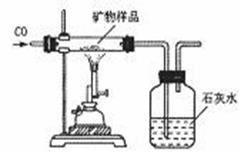 如图是某同学设计的冶炼铁的实验装置,下列有关说法中正确的是( )
如图是某同学设计的冶炼铁的实验装置,下列有关说法中正确的是( )
A.该实验开始时应先通CO一段时间,再加热
B.该反应属于置换反应
C.该实验设计合理,没有任何缺陷
D.该反应与CO还原CuO的反应原理、装置完全相同
8.某学校九年级化学兴趣小组为了测定Fe、Cu、Ag三种金属的活动性顺序,设计了四种实验方案,每种方案所用试剂如下,你认为其中不可行的方案是( )
A.Cu、Ag、FeSO4溶液 B.Fe、Ag、CuSO4溶液
C.Fe、Cu、稀盐酸、AgNO3溶液 D.Cu、FeSO4溶液、AgNO3溶液
9.一些食物的近似PH如下表:
|
食物 |
苹果 |
葡萄 |
牛奶 |
玉米粥 |
|
pH |
2.9-3.3 |
3.5-4.5 |
6.3-6.6 |
7.2-8.0 |
人的胃液中含有盐酸,对于胃酸过多的人,空腹时最适宜使用上述食物中的 ( )
A.苹果 B.葡萄 C.牛奶 D.玉米粥
10.CO在高温下还原a g四氧化三铁,得到b g铁,则铁的相对原子质量是 ( )
A.64b/(3a–b) B.24b/(a–b) C.3(a–b)/64b D.64b/3(a–b)
11.“把下列物质混合,能得到溶液的是 ( )
A.冰加到水中 B.植物油加到水中 C.碘加入酒精中 D.面粉加到水中
12.将适量的 ①Ca ②CaO ③Ca(OH)2 ④CaCO3 分别投入到等质量、等质量分数的稀盐酸中,恰好完全反应后,所得溶液中溶质的质量分数的大小关系正确的是( )
A.①>②>③>④ B.①>②=④>③ C.④>③>②>① D.④>①>②=③
13.有一课外活动小组在饱和的石灰水溶液中,加入少量生石灰,再降至室温,下列对出现的情况,描述完全正确的一组是 ( )
①溶液的溶质质量分数不变 ②原饱和溶液的溶剂量减少
③原饱和溶液的溶质质量减少 ④饱和溶液总质量增加
A.① B.①② C.①②③ D.①②③④
14.向100g水中不断加入固体A或改变温度,得到相应的溶液①-⑤。下列说法正确的是( )

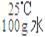
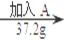 ①
①  ②
②  ③
③  ④
④ ⑤
⑤
资料:A的溶解度
|
温度/℃ |
20 |
30 |
40 |
50 |
60 |
|
溶解度/g |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
A.②④⑤的溶液为饱和溶液 B.④⑤中A的质量分数相等
C.②中A的质量分数最大 D.①③④⑤为不饱和溶液
15.向装有50g稀硫酸的小烧杯中,不断慢慢滴加10%的氢氧化钡溶液至过量。有关量的变化情况见下图(横坐标表示氢氧化钡溶液的质量,纵坐标表示小烧杯中一些量的变化)。其中肯定不正确的是( )

16.(4分)写出符合下列意义的化学符号
(1)2个铁离子 (2)氦气
(3)2个水分子 (4)+2价的镁元素
17.(4分)从Ca 、C 、 S 、H 、O 、N六种元素中选择适当的化学用语按要求填空。
(1)人体中元素含量最高的是 ;
(2)常用作干燥剂的一种酸 ;
(3)能作为燃料的一种氧化物是 ;
(4)既可用来消毒杀菌,又可用来改良酸性土壤的一种碱是__ ___;
18.(5分)右图是有关氧气的知识结构图(部分反应条件省略。参加反应的氧气为足量)。请回答下列问题:
(1) 反应①的化学方程式为 。
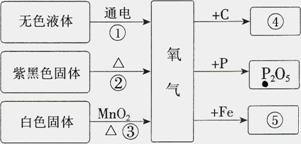 (2)反应③中二氧化锰的作用是
。
(2)反应③中二氧化锰的作用是
。
(3)物质④是由3g碳和6g氧气完全反应
得到的气体(碳和氧气均无剩余),
属于 (填序号)。
A.单质 B.化合物 C.混合物
(4)其中带点元素的化合价为 。
(5)写出反应②的化学方程式: 。
19.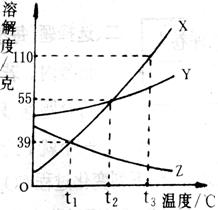 (3分)右图为X、Y、Z三种固体物质的溶解度曲线。回答下列问题:
(3分)右图为X、Y、Z三种固体物质的溶解度曲线。回答下列问题:
(1) ① t30C时,X、Y、Z三种物质溶解度的大小关系 。
② t30C时,将等质量的X、Y、Z溶于水,都刚好形成饱和溶液则需
加入水的质量由多到少的顺序是 。
(2)分别将X、Y、Z的饱和溶液从t30C降温到t10C时,三种溶液中溶质
的质量分数由大到小的顺序是 。
20.(2分)将等质量、等质量分数的盐酸和火碱两种溶液充分混合后,加入几滴紫色石蕊试液,最终溶液
显 色;如果将等质量、等质量分数的硫酸和烧碱两种溶液充分混合后,加入几滴紫色石蕊试
液,最终溶液显 色。
21.(4分)按照题目要求写出化学方程式:
(1)一个能生成二氧化碳的化合反应:
(2)一个能生成二氧化碳的分解反应:
(3)一个能生成二氧化碳的置换反应:
(4)一个能生成二氧化碳的复分解反应: 。
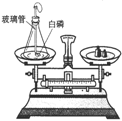
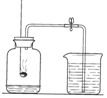
22.(5分)将下列四个实验所验证或探究的目的填写在横线上,并回答相关问题.

|


|
|
|
|
(1)在实验A中使用的计量仪器是______________ (填仪器的名称,下同)。在上述四个实验中有三个实验都使用了的同一种仪器是____________。
(2)在实验D中观察到的现象是_____________________________。在实验A和实验C中观察到的相同现象是_____________________,在实验A和实验C中反应的化学方程式是_______________________。
23.(7分)我们知道二氧化碳与水反应生成碳酸,那么二氧化硫与水是否也能反应生成一种酸呢?某实验小组对此进行探究,设计的探究过程如下。请你回答其中的有关问题:
(1)做出假设: ;
(2)设计方案:先验证水能否使蓝色石蕊试纸变色,再验证二氧化硫气体能否使干燥的蓝色石蕊试纸变色,最后验证二氧化硫气体能否使湿润的蓝色石蕊试纸变红,实验装置和药品如图:
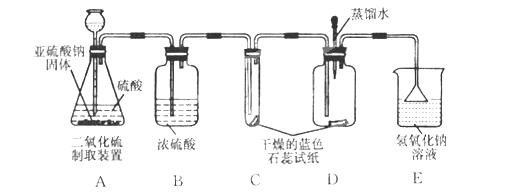
(3)查阅资料:你认为该实验小组需要掌握的资料内容中应包括(填序号)
①二氧化硫易溶于水 ②酸能使湿润的蓝色石蕊试纸变红 ③SO2不与浓硫酸反应 ④二氧化硫有毒,能与碱溶液反应生成盐和水
(4)实验:
①实验过程中装置C内石蕊试纸的颜色始终没有变化,这说明 。
②装置D中胶头滴管中的蒸馏水在二氧化硫气体生成之前滴到蓝色石蕊试纸上,未见试纸颜色发生变化,当有二氧化硫气体通过时发现湿润的蓝色石蕊试纸变红。此现象说明 ,此过程中反应的化学方程式为 。
③装置E的作用是 。
(5)结论:原假设 (填“成立”或“不成立”)
24.(7分)某课外活动小组为了测定铜铁合金中铁的质量分数,现取铜铁合金样品20.0g,将80.0g稀硫酸平均分成4份,分4次逐渐加入到样品中,每次充分反应后测得剩余固体质量 见下表:
|
次 数 |
1 |
2 |
3 |
4 |
|
加入稀硫酸质量/g |
20.0 |
20.0 |
20.0 |
20.0 |
|
剩余固体质量/g |
17.2 |
14.4 |
13.0 |
X |
(1)试确定:X的值为 ;铜铁合金中铁的质量分数为 ;
(2)求稀硫酸中溶质质量分数为多少?(答案保留0.1%,写出解题过程)
(全卷共四个大题 满分:70分 与物理共用120分钟 请将正确答案填写在答题卷上) 可能用到的相对原子质量:C-12 H-1 O-16 Cl-35.5 Na-23 Fe-56 S-32 Ca-40 Ba-137 参考答案
化学参考答案
一、选择题(每小题2分,每小题只有一个正确选项,共30分)

21.(4分)C + O2
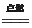 CO2 (其它合理答案均可,下同) H2CO3 === H2O +
CO2↑
CO2 (其它合理答案均可,下同) H2CO3 === H2O +
CO2↑
C + 2CuO 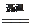 2Cu + CO2 ↑ CaCO3 + 2HCl === CaCl2 + H2O
+CO2 ↑
2Cu + CO2 ↑ CaCO3 + 2HCl === CaCl2 + H2O
+CO2 ↑
三、实验探究题(本大题2个小题,共12分)
22.(5分)托盘天平 烧杯 下层蜡烛先熄灭,上层蜡烛后熄灭 生成大量白烟
4P + 5O2 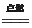 2P2O5
2P2O5
23.(7分)二氧化硫和水反应生成一种酸 ①②③④ 二氧化硫单独不能使蓝色石蕊变红 水单独不能使蓝色石蕊变红,而水和二氧化硫反应生成一种酸使蓝色石蕊变红 SO2 + H2O == H2SO3 吸收二氧化硫,防止污染空气 成立(答案要与第一空对应)
四、计算题(本大题1个小题,共6分)
24.(6分) 13.0 35% 24.5%(解题过程略)