
1. 在一个基态多电子的原子中,不可能有两个完全相同的电子。( )
答案:√
2. 如果某一基态原子3p能级上仅有2个电子,它们的自旋状态必然相反。( )
答案:×
3. M层全充满而N层为4s2的原子与核外电子排布为1s22s22p63s23p63d64s2的原子位于同一族。( )
答案:×
4. 2p能级有1个未成对电子的基态原子的价电子排布为2s22p5。( )
答案:×
5. N原子最外层电子的轨道表示式:
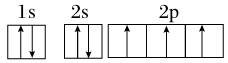
( )
答案:×
6. 24Cr原子的电子排布式是1s22s22p63s23p63d44s2。( )
答案:×
7. 价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素。( )
答案:×
8. 因同周期元素的原子半径从左到右逐渐减小,故第一电离能必依次增大。( )
答案:×
9. 凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键。( )
答案:×
10. CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的。( )
答案:×
11. SiF4和SO的中心原子均为sp3杂化。( )
答案:√
12. NH的电子式为[H\o(\s\up7(H\s\do5(..H]+,呈平面形结构。( )
答案:×
13. CS2为V形的极性分子。( )
答案:×
14. C2H2分子中σ键与π键的数目比为1∶1。( )
答案:×
15. 水加热到很高温度都难分解是因水分子间存在氢键。( )
答案:×
16. CH2Cl2和CCl4均是四面体构型的非极性分子。( )
答案:×
17. 分子晶体中分子间作用力越大,分子越稳定。( )
答案:×
18. 只要含有金属阳离子的晶体就一定是离子晶体。( )
答案:×
19. 某元素气态基态原子的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,当它与氯气反应时可能生成的阳离子是X3+。( )
答案:×
20. 具有下列电子排布式的原子中,①1s22s22p63s23p2、②1s22s22p3、③1s22s22p2、④1s22s22p63s23p4,原子半径最大的是①。( )
答案:√
21. ①Na、K、Rb;②N、P、As;③O、S、Se;④Na、P、Cl,元素的电负性随原子序数增大而递增的是④。( )
答案:√
22. 具有下列最外层电子排布式的原子中,①3s23p1、②3s23p2、③3s23p3、④3s23p4第一电离能最大的是③。( )
答案:√
23. 分子晶体中,共价键键能越大,该分子晶体的熔、沸点一定越高。( )
答案:×
24. 原子晶体中,共价键越强,熔点越高。( )
答案:√
25. 某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体。( )
答案:×
26. 二氧化硅和干冰晶体熔化时所克服的作用力类型相同。( )
答案:×
27. 分子晶体中不一定含有共价键,离子晶体中一定含有离子键。( )
答案:√
28. 离子晶体中每个离子周围均吸引着6个带相反电荷的离子。( )
答案:×
1. 微粒结构示意图
Na+________
Cl________
Fe________
Fe3+________
N________
答案:
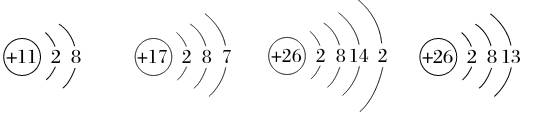
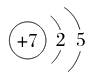
2. 核外电子排布式
Na+________________
Cl-________________
Fe________________
Fe3+________________
N________________
Cr________________
Cu________________
Ti________________
Ni________________
答案:1s22s22p6 1s22s22p63s23p6
1s22s22p63s23p63d64s2 1s22s22p63s23p63d5
1s22s22p3 1s22s22p63s23p63d54s1
1s22s22p63s23p63d104s1 1s22s22p63s23p63d24s2
1s22s22p63s23p63d84s2
3. 轨道表示式
Mg________________
N________________
O________________
Fe原子的外围电子轨道表示式________
Cr原子的外围电子轨道表示式________
答案:
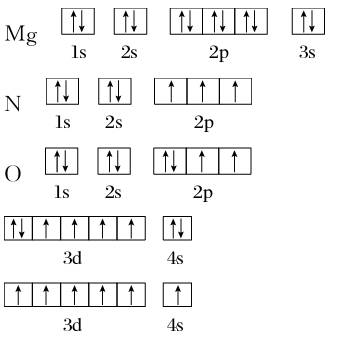
1. 常见分子的空间构型及中心原子杂化类型
|
|
空间构型 |
杂化类型 |
|
CH4 |
|
|
|
NH3 |
|
|
|
H2O |
|
|
|
CO2 |
|
|
|
BeCl2 |
|
|
|
BF3 |
|
|
|
C2H2 |
|
|
|
C2H4 |
|
|
|
苯 |
|
|
答案:
|
|
空间构型 |
杂化类型 |
|
CH4 |
正四面体 |
sp3 |
|
NH3 |
三角锥形 |
sp3 |
|
H2O |
V形 |
sp3 |
|
CO2 |
直线形 |
sp |
|
BeCl2 |
直线形 |
sp |
|
BF3 |
平面正三角形 |
sp2 |
|
C2H2 |
直线形 |
sp |
|
C2H4 |
平面形 |
sp2 |
|
苯 |
平面正六边形 |
sp2 |
2. 常见晶体结构模型
|
晶体 |
晶体结构 |
晶体详解 |
|
|
原子晶体 |
金刚石 |
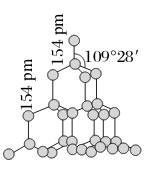 |
(1)每个碳与____个碳以共价键结合,形成________结构。 (2)键角均为________。 (3)最小碳环由6个C组成且六原子不在同一平面内。 (4)每个C参与4条C-C键的形成,C原子数与 C-C键数之比为____。 |
|
SiO2 |
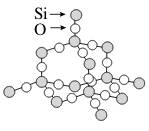 |
(1)每个Si与____个O以共价键结合成________结构。 (2)每个正四面体占有1个Si,4个“O”,n(Si)∶n(O)=________。 (3)最小环上有________个原子,即________个O,________个Si。 |
|
|
分子晶体 |
干冰 |
 |
(1)8个CO2分子构成立方体且在6个面心又各占据1个CO2分子。 (2)每个CO2分子周围等距且紧邻的CO2分子有____个。 |
|
离子晶体 |
NaCl (型) |
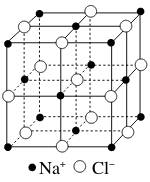 |
(1)每个Na+(Cl-)周围等距且紧邻的Cl-(Na+)有____个,每个Na+周围等距且紧邻的Na+有____个。 (2)每个晶胞中含____个Na+和____个Cl-。 |
|
CsCl (型) |
 |
(1)每个Cs+周围等距且紧邻的Cl-有____个,每个Cl-周围等距且紧邻的Cs+有____个。 (2)如图为____个晶胞,每个晶胞中含____个Cs+,____个Cl-。 |
|
|
金属晶体 |
简单立方堆积 |
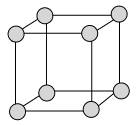 |
典型代表________ 空间利用率________ 配位数为________ |
|
体心立方堆积 |
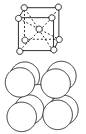 |
典型代表________ 空间利用率________ 配位数为________ |
|
|
面心立方堆积 |
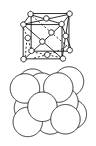 |
典型代表________ 空间利用率________ 配位数为________ |
|
|
六方最密堆积 |
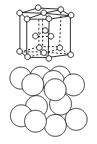 |
典型代表________ 空间利用率________ 配位数为________ |
答案:
|
晶体 |
晶体结构 |
晶体详解 |
|
|
原子晶体 |
金刚石 |
 |
(1)每个碳与4个碳以共价键结合,形成正四面体结构。 (2)键角均为109°28′。 (3)最小碳环由6个C组成且六原子不在同一平面内。 (4)每个C参与4条C-C键的形成,C原子数与 C-C键数之比为1∶2。 |
|
SiO2 |
 |
(1)每个Si与4个O以共价键结合成正四面体结构。 (2)每个正四面体占有1个Si,4个“O”,n(Si)∶n(O)=1∶2。 (3)最小环上有12个原子,即6个O,6个Si。 |
|
|
分子晶体 |
干冰 |
 |
(1)8个CO2分子构成立方体且在6个面心又各占据1个CO2分子。 (2)每个CO2分子周围等距且紧邻的CO2分子有12个。 |
|
离子晶体 |
NaCl (型) |
 |
(1)每个Na+(Cl-)周围等距且紧邻的Cl-(Na+)有6个。每个Na+周围等距且紧邻的Na+有12个。 (2)每个晶胞中含4个Na+和4个Cl-。 |
|
CsCl (型) |
 |
(1)每个Cs+周围等距且紧邻的Cl-有8个,每个Cl-周围等距且紧邻的Cs+有8个。 (2)如图为8个晶胞,每个晶胞中含1个Cs+。1个Cl-。 |
|
|
金属晶体 |
简单立方堆积 |
 |
典型代表Po 空间利用率52% 配位数为6 |
|
体心立方堆积 |
 |
典型代表Na、K、Fe 空间利用率68% 配位数为8 |
|
|
面心立方堆积 |
 |
典型代表Cu、Ag、Au 空间利用率74% 配位数为12 |
|
|
六方最密堆积 |
 |
典型代表:Mg、Zn、Ti 空间利用率74% 配位数为12 |