1、 光电池可用作计算器、人造卫星的动力,如图所示。下列分析正确的是( )
光电池可用作计算器、人造卫星的动力,如图所示。下列分析正确的是( )
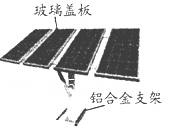 A.硅是将太阳能转换为电能的常用材料
B.玻璃盖板是由纯碱、石灰石与石英制得的晶体
C.支架用铝合金而不用铝是利用了其熔点高于铝的特点
D.光电池制造中不会产生任何化学污染
A.硅是将太阳能转换为电能的常用材料
B.玻璃盖板是由纯碱、石灰石与石英制得的晶体
C.支架用铝合金而不用铝是利用了其熔点高于铝的特点
D.光电池制造中不会产生任何化学污染
2、可逆反应2NO2 2NO+O2在恒容密闭容器中进行,下列情况达到平衡状态的是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②混合气体的平均相对分子质量不再改变
③NO2、NO、O2的反应速率之比为2:2:1
④混合气体的颜色不再改变
⑤混合气体的密度不再改变
A.①②④
B.②③⑤
C.①②⑤
D.①②④⑤
2NO+O2在恒容密闭容器中进行,下列情况达到平衡状态的是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②混合气体的平均相对分子质量不再改变
③NO2、NO、O2的反应速率之比为2:2:1
④混合气体的颜色不再改变
⑤混合气体的密度不再改变
A.①②④
B.②③⑤
C.①②⑤
D.①②④⑤
3、 从如图所示的某气体反应的能量变化分析,以下判断错误的是( )
从如图所示的某气体反应的能量变化分析,以下判断错误的是( )
 A.这是一个放热反应
B.该反应可能需要加热
C.生成物的总能量低于反应物的总能量
D.反应物比生成物更稳定
A.这是一个放热反应
B.该反应可能需要加热
C.生成物的总能量低于反应物的总能量
D.反应物比生成物更稳定
4、有A、B、C、D四块金属片,用导线两两相连插入稀硫酸中,可以组成各种原电池.若A和B相连时,A为负极;C与D相连时,C溶解,D上有氢气生成;A与C相连时,C为正极;B与D相连时,电子由D极经导线流向B极,则这四种金属的活泼性由强到弱的顺序为( ) A.A>B>C>D B.A>C>D>B C.C>A>D>B D.B>D>C>A
5、下列有关电池叙述正确的是( ) A.水果电池是高效环保的家用电池 B.锌锰干电池是一种常用的二次电池 C.锌锰干电池碳棒是负极,锌片是正极 D.锌锰干电池工作一段时间后锌外壳逐渐变薄
6、为了解决目前存在的世界性能源危机,新的替代能源主要包括 ( ) ①核能②柴草③焦碳④太阳能⑤氢能⑥液化石油气⑦水煤气⑧天然气 A.②③⑥⑦ B.①④⑤ C.③⑥⑦⑧ D.①②④
7、 一种“即食即热型快餐”适合外出旅行时使用。其内层是用铝箔包裹的、并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是( )
A.浓硝酸与水 B.生石灰与水C. 熟石灰与水 D.氯化钠与水
一种“即食即热型快餐”适合外出旅行时使用。其内层是用铝箔包裹的、并已加工好的真空包装食品,外层则是分别包装的两包化学物质,使用时拉动预留在外的拉线,使这两种化学物质反应,此时便可对食物进行加热,这两包化学物质最合适的选择是( )
A.浓硝酸与水 B.生石灰与水C. 熟石灰与水 D.氯化钠与水
8、 航天飞机用的铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为:2NH4ClO4
航天飞机用的铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为:2NH4ClO4 N2↑+ 4H2O+Cl2↑+2O2↑+Q,下列对此反应叙述中错误的是( )
N2↑+ 4H2O+Cl2↑+2O2↑+Q,下列对此反应叙述中错误的是( )
A.反应属于分解反应、B.上述反应瞬间产生大量高温气体推动航天飞机飞行
C.反应从能量变化上说,主要是化学能转变为热能和动能
D.在反应中高氯酸铵只起氧化剂作用
9、下列装置中,能构成原电池的是( )
 A.只有(甲) B.只有(乙) C.只有(丙) D.除(乙)均可以
A.只有(甲) B.只有(乙) C.只有(丙) D.除(乙)均可以
10、 -定条件下,可逆反应2A(g) B(g)+3C(g),在下列四种状态中,反应处于平衡状态的是( )
B(g)+3C(g),在下列四种状态中,反应处于平衡状态的是( )
|
选项 |
正反应速率 |
逆反应速率 |
|
A |
v(A)=2mol.L-1.min-1 |
 v(B)=2mol.L-1.min-1 v(B)=2mol.L-1.min-1 |
|
B |
WWW.v(A)=2mol.L-1.min-1 |
v(C)=2mol.L-1.min-1 |
|
C |
v(A)=1mol.L-1.min-1 |
v(B)=2mol.L-1.min-1 |
|
D |
v(A)=1mol.L-1.min-1 |
v(C)=1.5mol.L-1.min-1 |
11、研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电。关于该电池的下列说法不正确的是( )
A.水既是氧化剂又是溶剂 B.放电时正极上有氢气生成
C.放电时OH-向正极移动 D.总反应
12、下列叙述不正确的是( )
A.根据一次能源与二次能源的划分,氢气为二次能源
B.电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源
C.火电是将燃料中的化学能直接转化为电能的过程
 D.在火力发电时,化学能转化为热能的过程实际上是氧化还原反应发生的过程,伴随着能量的变化
D.在火力发电时,化学能转化为热能的过程实际上是氧化还原反应发生的过程,伴随着能量的变化
13、如图所示的装置中,属于原电池的是( )
A. B.
B.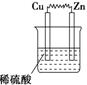 C.
C.  D.
D.
14、 下列说法不正确的是( )
下列说法不正确的是( )
A.物质发生化学反应都伴随着能量变化。B.化学反应的速率和限度均可通过改变化学反应条件而改变。C.可逆反应只是代表少数反应。D.化学反应达到平衡状态时,正反应速率与逆反应速率相等。
15、在下列平衡体系中,保持温度一定时,改变某物质的浓度,混合气体的颜色会改变;改变压强时,颜色也会改变,但平衡并不移动,这个反应是( )
A.2NO+O2 2NO2 B.N2O4
2NO2 B.N2O4 2NO2 C.Br2(g)+H2
2NO2 C.Br2(g)+H2 2HBr D.6NO+4NH3
2HBr D.6NO+4NH3 5N2+3H2
5N2+3H2
16、在下列影响化学反应速率的外界因素中,肯定能使化学反应速率加快的方法是( )
①升高温度②加入正催化剂③增大反应物浓度④将固体块状反应物磨成末⑤增大压强
A.①②③⑤ B.①②④⑤ C.①③④⑤ D.①②③④
17、在反应2SO2+18O2 2SO3中,其中氧气用18O标记上,其中含有18O的物质有( )
A.SO2 B.SO2 O2 SO3 C.O2
SO3 D.SO2
SO3
2SO3中,其中氧气用18O标记上,其中含有18O的物质有( )
A.SO2 B.SO2 O2 SO3 C.O2
SO3 D.SO2
SO3
18、一定条件下,在密闭容器中,能表示反应X(g)+2Y(g)=2Z(g) 一定达到化学平衡状态的是( )
 ① X、Y、Z的物质的量之比为1:2:2② X、Y、Z的浓度不再发生变化③ 容器中的压强不再发生变化④ 单位时间内生成n mol Z,同时生成2n mol Y
A.①② B.①④ C.②③ D.③④
① X、Y、Z的物质的量之比为1:2:2② X、Y、Z的浓度不再发生变化③ 容器中的压强不再发生变化④ 单位时间内生成n mol Z,同时生成2n mol Y
A.①② B.①④ C.②③ D.③④
19、在10℃时某化学反应速率为0.1 mol/(L•s),若温度每升高10℃反应速率增加到y原来的2倍。为了把该反应速率提高到1.6 mol/(L•s),该反应需在什么温度下进行( ) A.30℃ B.40℃ C.50℃ D.60℃
20、201905年德国化学家哈伯发明了合成氨的方法。他因此获得了1918年度诺贝尔化学奖。哈伯法合成氨需要在20-50 MPa的高压和500 ℃的高温下,用铁作催化剂,且氨转化率10%-15%。2005年6月27日美国化学会刊报道,美国俄勒冈大学的化学家使用了一种名为transFe(DMeOPrPE)2Cl2的铁化合物。用transFe(DMeOPrPE)2Cl2作催化剂,在常温常压下合成出氨,反应可表示为N2+3H2 2NH3,有关说法正确的是( )
A.不同的催化剂对化学反应速率影响均相同
B.新法合成与哈伯法相比不需要在高温条件下,可节约大量能源,极具发展远景
C.新法合成能在常温下进行是因为不需要断裂化学键
D.哈伯法合成氨是吸热反应,新法合成氨是放热反应
2NH3,有关说法正确的是( )
A.不同的催化剂对化学反应速率影响均相同
B.新法合成与哈伯法相比不需要在高温条件下,可节约大量能源,极具发展远景
C.新法合成能在常温下进行是因为不需要断裂化学键
D.哈伯法合成氨是吸热反应,新法合成氨是放热反应
21、(6分)
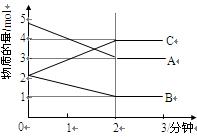
某温度下,在2 L的密闭容器中,X、Y、Z三种物质随时间变化的曲线如图所示。
 由图中数据分析:该反应的化学方程式为: 。反应开始至2 min ,Z的平均反应速率为 。
由图中数据分析:该反应的化学方程式为: 。反应开始至2 min ,Z的平均反应速率为 。
22、(9分)
在由铜片、锌片和200 mL稀硫酸组成的原电池中,若锌片口只发生电化学腐蚀,当在铜片上共放出2.24 L气体(标准状况)时,稀H2SO4刚好用去一半,则产生这些气体消耗锌 g,共有 mol电子通过导线,原H2SO4溶液的浓度是 mol/L
23、(10分)
分析下列实例,根据已有的知识和经验,填写下表。

24、(9分)
可逆反应aA(g)+bB(g)=cC(g)+dD(g),取a mol A和b mol B置于V L容器内1 min后,测得容器内A的浓度为x mol•L-1,这时B的浓度为________,C的浓度为________,这段时间内反应的平均速率若以物质A的浓度变化来表示,应为_________________。
25、(6分)
某可逆反应进行过程中,在不同反应时间各物质的量的变化情况如图所示。则该反应的化学方程式为_____________;反应开始至2分钟,能用C表示反应速率吗?________(填“能”或“不能”),原因____________。