
1.N2的结构可以表示为 ,CO的结构可以表示为
,CO的结构可以表示为 ,其中椭圆框表示π键,下列说法中不正确的是( )
,其中椭圆框表示π键,下列说法中不正确的是( )
A.N2分子与CO分子中都含有三键
B.CO分子中有一个π键是配位键
C.N2与CO互为等电子体
D.N2与CO的化学性质相同
解析 由题意可知N2分子中N原子之间、CO分子中C、O原子之间均通过2个π键,一个σ键,即三键结合,其中,CO分子中1个π键由O原子单方面提供孤电子对,C原子提供空轨道通过配位键形成。N2化学性质相对稳定,CO具有比较强的还原性,两者化学性质不同。
答案 D
2.下列物质的分子中既有σ键,又有π键的是( )
①HCl ②H2O ③O2 ④H2O2 ⑤C2H4 ⑥C2H2
A.①②③ B.③④⑤⑥
C.①③⑥ D.③⑤⑥
解析 单键一定是σ键,双键或三键中有一个σ键,其余均是π键。
答案 D
3.关于键长、键能和键角的说法中不正确的是( )
A.键角是描述分子立体结构的重要参数
B.键长的大小与成键原子的半径和成键数目有关
C.键能越大,键长就越长,共价化合物也就越稳定
D.键角的大小与键长、键能的大小无关
解析 C项应是键能越大,键长越短,共价化合物就越稳定。
答案 C
4.下列有关化学键的叙述,正确的是( )
A.离子化合物中一定含有离子键
B.单质分子中均不存在化学键
C.含有极性键的分子一定是极性分子
D.含有共价键的化合物一定是共价化合物
解析 A项,离子化合物中一定含有离子键,A项正确;B项,H2、O2等单质分子中均存在共价键,B项错误;C项,CO2分子中含有极性键,但CO2分子属于非极性分子,C项错误;D项,某些离子化合物(如NaOH)中也含有共价键,D项错误。
答案 A
5.(2015.南昌专练)CH、-CH3、CH都是重要的有机反应中间体,有关它们的说法正确的是( )
A.它们互为等电子体,碳原子均采取sp2杂化
B.CH 与 NH3、H3O+ 互为等电子体,立体构型均为正四面体形
C.CH 中的碳原子采取 sp2 杂化,所有原子均共面
D.CH 与OH- 形成的化合物中含有离子键
解析 A项,CH为 8e-,-CH3 为 9e-,CH 为 10e- ;B项,三者均为三角锥形;C项,CH 中 C 的价电子对数为3 , 为 sp2 杂化,平面三角形;D项,CH3OH 中不含离子键。
答案 C
6.用价层电子对互斥理论预测H2S和BF3的立体构型,下列结论中正确的是( )
A.直线形;三角锥形 B.V形;三角锥形
C.正四面体;正四面体 D.V形;平面三角形
解析 在判断分子的立体构型的时,关键是看分子的中心原子是否存在孤电子对,而不能简单地从组成上看,要注意价层电子对互斥理论和分子立体构型的区别和联系。在H2S中,价电子对数为4,若无孤电子对存在,则其应为正四面体构型,但中心原子S上有两对孤电子对,且孤电子对也要占据中心原子周围的空间,它们相互排斥,因此H2S为V形。在BF3中,价电子对数为3,其中心原子B上无孤电子对,因此BF3为平面三角形。
答案 D
7.(2015.周口市西华一中月考)以下微粒含配位键的是( )
①N2H ②CH4 ③OH- ④NH ⑤Fe(CO)3
⑥Fe(SCN)3 ⑦H3O+ ⑧[Ag(NH3)2]OH
A.①②④⑦⑧ B.③④⑤⑥⑦
C.①④⑤⑥⑦⑧ D.全部
解析 ①N2H的结构式为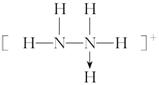 ;⑦H3O+的结构式为
;⑦H3O+的结构式为 ;Fe(CO)3、Fe(SCN)3、[Ag(NH3)2]OH均为配合物,中心离子(或原子)与配体之间均含配位键。
;Fe(CO)3、Fe(SCN)3、[Ag(NH3)2]OH均为配合物,中心离子(或原子)与配体之间均含配位键。
答案 C
8.(2015.绵阳模拟)下列描述正确的是( )
A.CS2为V形极性分子
B.SiF4与SO的中心原子均为sp3杂化
C.C2H2分子中σ键与π键的数目比为1∶1
D.水加热到很高温度都难分解是因水分子间存在氢键
解析 CS2为直线形非极性分子;SiF4与SO的中心原子的价层电子对数均为4,因此中心原子均为sp3杂化;C2H2分子中σ键与π键的数目比为3∶2;水加热到很高温度都难分解是因O-H键的键能较大。
答案 B
9.(2015.西安调研)下列无机含氧酸分子中酸性最强的是( )
A.HNO2 B.H2SO3 C.HClO3 D.HClO4
解析 对于同一种元素的含氧酸,成酸元素的化合价越高,其含氧酸的酸性越强,如HN+3O2<HN+5O3,H2S+4O3<H2S+6O4,HCl+5O3<HCl+7O4。观察A、B、C、D四个选项,HNO2、H2SO3、HClO3中的中心元素N、S、Cl都未达到其最高价,其酸性不够强,只有D选项中的HClO4中的Cl元素为+7价,是Cl元素的最高价,使H-O-ClO3中O原子的电子向Cl原子偏移,在水分子作用下,容易电离出H+,酸性最强。
答案 D
10.[2013.江苏化学,21A(2)(3)(4)(5)]元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是________。
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是________________。
(3)Y与Z可形成YZ。
①YZ的空间构型为________(用文字描述)。
②写出一种与YZ互为等电子体的分子的化学式:________。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为________。
解析 X的核外电子排布式为1s22s22p63s23p63d104s2,为30号元素锌。Y核外电子排布式为1s22s22p63s23p4,为16号元素硫,Z为氧。(1)H2S中硫原子有2对孤电子对,2个成键原子,所以S原子杂化类型为sp3。(2)在乙醇中的溶解度H2O大于H2S,是因为水分子与乙醇间能形成分子间氢键。(3)①SO中由于硫原子是sp3杂化类型,所以为空间正四面体构型。②与SO互为等电子体的分子可以采用“左右移位,同族替换”的方法,SO→SiF4→SiCl4→CCl4等。(4)[Zn(NH3)4]2+中Zn2+与NH3之间以配位键相连,共4个σ键,加上4个NH3的12个σ键,共16个σ键。
答案 (1)sp3
(2)水分子与乙醇分子之间形成氢键
(3)①正四面体 ②CCl4或SiCl4等
(4)16 mol或16×6.02×1023个
11.(2015.郑州模拟)波尔多液是果农常用的一种杀菌剂。氯吡苯脲是一种西瓜膨大剂(植物生长调节剂),其组成结构和物理性质见下表。
|
分子式 |
结构简式 |
外观 |
熔点 |
溶解性 |
|
C12H10 ClN3O |
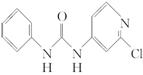 |
白色结晶粉末 |
170-172 ℃ |
易溶于水 |
回答下列问题:
(1)氯吡苯脲晶体中,氮原子的杂化轨道类型为________。
(2)氯吡苯脲晶体中,微粒间的作用力类型有________。
A.离子键 B.金属键
C.极性键 D.非极性键
E.配位键 F.氢键
(3)查文献可知,可用2氯4氨吡啶与异氰酸苯酯反应,生成氯吡脲。
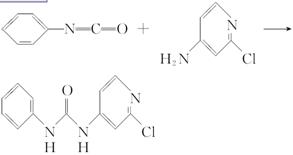
反应过程中,每生成1 mol氯吡苯脲,断裂________个σ键、断裂________个π键。
(4)波尔多液是果农常用的一种杀菌剂,是由硫酸铜和生石灰制得。若在波尔多液的蓝色沉淀上,再喷射氨水,会看到沉淀溶解变成蓝色透明溶液,得到配位数为4的配合物。铜元素基态原子排布式为________________________________。
(5)上述沉淀溶解过程的离子方程式___________________________________
_________________________________________________________________。
解析 (1)氮原子在氯吡苯脲中以2种形式出现,一是N-N,另一是N===N,前者1+3=4,sp3杂化,后者1+2=3,sp2杂化。(3)反应过程中,异氰酸苯酯断裂的N===N中1根π键,2氯4氨吡啶断裂的是1根σ键。(5)溶解过程是Cu(OH)2蓝色沉淀溶解在氨水中生成四氨合铜离子,形成蓝色透明溶液。
答案 (1)sp2、sp3杂化 (2)C、D (3)NA NA
(4)1s22s22p63s23p63d104s1或[Ar]3d104s1 (5)Cu(OH)2+4NH3.H2O===[Cu(NH3)4]2++2OH-+4H2O
12.(2015.唐山市一模)已知:A、B、C、D、E、F六种元素,原子序数依次增大。A原子核外有两种形状的电子云,两种形状的电子云轨道上电子数相等;B是短周期中原子半径最大的主族元素;C元素3p能级半充满;E是所在周期电负性最大的元素;F是第四周期未成对电子最多的元素。
试回答下列有关的问题:
(1)写出F元素的电子排布式:__________________。
(2)已知A元素的一种氢化物分子中含四个原子,则在该化合物的分子中A原子的杂化轨道类型为________。
(3)已知C、E两种元素形成的化合物通常有CE3、CE5两种。这两种化合物中一种为非极性分子,一种为极性分子,属于极性分子的化合物的分子立体构型是________。
(4)B、C、D、E的第一电离能由大到小的顺序是__________________________________________________________________
_____________________________________________________(写元素符号)。
四种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是_________________________________________________________
________________________________________________________(写化学式)。
解析 A、B、C、D、E、F六种元素,原子序数依次增大,由“A原子核外有两种形状的电子云,两种形状的电子云轨道上电子云相等”推出A为O,由“B是短周期中原子半径最大的元素”推出B为Na,由“C元素3p能级半充满”推出C为P,由“F是第四周期未成对电子最多的元素”推出F为Cr,由“E是所在周期电负性最大的元素”及原子序数大小关系推出E为Cl,则D为S。(2)含四个原子的A的氢化物为H2O2,其氧原子的杂化轨道类型为sp3杂化。(3)CE3和CE5为PCl3和PCl5,PCl3是极性分子,立体构型为三角锥形,PCl5为非极性分子。(4)同周期主族元素第一电离能从左到右呈现增大的趋势,但第ⅤA族反常,第一电离能由大到小的顺序是Cl>P>S>Na。四种元素最高价氧化物对应的水化物分别是NaOH、H3PO4、H2SO4、HClO4,NaOH是碱,H3PO4是中强酸,H2SO4、HClO4都是强酸,物质的量浓度相同时,pH由大到小顺序为NaOH>H3PO4>HClO4>H2SO4。
答案 (1)1s22s22p63s23p63d54s1(或[Ar]3d54s1)
(2)sp3 (3)三角锥形
(4)Cl>P>S>Na NaOH>H3PO4>HClO4>H2SO4
13.随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分是CH4)为原料经合成气(主要成分为CO、H2)制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁[Fe(CO)5]等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:
(1)[Fe(CO)5]中铁的化合价为0,写出铁原子的基态电子排布式:________________________________________________________________。
(2)与CO互为等电子体的分子和离子分别为________和________(各举一种即可,填化学式),CO分子的电子式为________,CO分子的结构式可表示成________。
(3)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有________,CH3OH的熔、沸点比CH4高,其主要原因是__________________________________。
(4)CH3CHO分子中,-CH3中的碳原子采取________杂化方式,-CHO中的碳原子采取________杂化方式。
13.随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分是CH4)为原料经合成气(主要成分为CO、H2)制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁[Fe(CO)5]等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:
(1)[Fe(CO)5]中铁的化合价为0,写出铁原子的基态电子排布式:__________________________________________________________________。
(2)与CO互为等电子体的分子和离子分别为________和________(各举一种即可,填化学式),CO分子的电子式为________,CO分子的结构式可表示成________。
(3)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有________,CH3OH的熔、沸点比CH4高,其主要原因是____________________________________。
(4)CH3CHO分子中,-CH3中的碳原子采取________杂化方式,-CHO中的碳原子采取________杂化方式。
解析 (1)Fe原子的基态核外电子排布式为1s22s22p63s23p63d64s2或[Ar]3d64s2。(2)N2、CN-与CO互为等电子体;因为N2的电子式为∶N∶∶N∶,所以CO的电子式为∶C∶∶O∶,其结构式为 (有一个配位键)。
(有一个配位键)。
(3)CH4、CH3OH中的碳原子均为四面体结构碳原子,采取sp3杂化;由于CH3OH是极性分子,且存在分子间氢键,所以CH3OH的熔、沸点较高。(4)CH3CHO的结构式为 ,甲基碳原子采取sp3杂化,醛基碳原子采取sp2杂化。
,甲基碳原子采取sp3杂化,醛基碳原子采取sp2杂化。
答案 (1)1s22s22p63s23p63d64s2或[Ar]3d64s2
(2)N2 CN- ∶C∶∶O∶ 
(3)CH4、CH3OH CH3OH分子有极性,同时分子之间还存在着氢键的作用
(4)sp3 sp2
[选做题]
14.(2015.福建理综,31节选)(1)下列关于CH4和CO2的说法正确的是________(填序号)。
a.固态CO2属于分子晶体
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d.CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
(2)Ni能与CO形成正四面体形的配合物Ni(CO)4,1 mol Ni(CO)4中含有________ mol σ键。
(3)一定条件下,CH4和CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物俗称“可燃冰”。
|
参数 分子 |
分子直径/nm |
分子与H2O的结合能E/kJ.mol-1 |
|
CH4 |
0.436 |
16.40 |
|
CO2 |
0.512 |
29.91 |
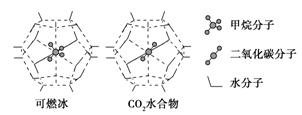
①“可燃冰”中分子间存在的2种作用力是__________________________。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0. 586 nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是______________________________________________。
解析 (1)a项,固态CO2是由CO2分子通过分子间作用力结合而成的分子晶体,正确;b项,CH4分子中含有极性共价键,但由于该分子中的共价键排列对称,因此该分子是非极性分子,错误;c项,固态时CH4和CO2都是分子晶体,分子之间通过分子间作用力结合,分子间作用力越强,物质的熔沸点就越高,而不是取决于分子内共价键的强弱,错误;d项,CH4分子中碳原子形成的都是σ键,C原子采取sp3杂化,而CO2分子中的C原子与两个O原子形成的是碳氧双键,含有2个σ键和2个π键,C原子采取sp杂化,正确。故答案选a、d。(2)Ni能与CO形成正四面体型的配合物Ni(CO)4,在每个配位体中含有1个σ键,在每个配位体与中心原子之间也形成1个σ键,所以1 mol Ni(CO)4中含有8 mol σ键。(3)①“可燃冰”中分子间存在的2种作用力分别是分子间作用力(也叫范德华力)和氢键。②根据表中的数据可知,笼状结构的空腔直径为0.586 nm,大于CO2分子的直径(0.512 nm),而且CO2与H2O分子之间的结合力大于CH4,因此可以实现用CO2置换出“可燃冰”中CH4的设想。
答案 (1)ad (2)8
(3)①氢键、范德华力 ②CO2的分子直径小于笼状空腔直径,且与H2O的结合力大于CH4