
1、某元素R的最高价氧化物的水化物分子式是HnRO2 n-2,则其气态氢化物中R元素的化合价是 ( )
A.3n-10
B.12-3n  C.3n-4 D.3n-12
C.3n-4 D.3n-12
2、具有下列特征的原子一定是非金属元素的是( )
A.最外层电子数大于4
B.具有负化合价
C.最高价氧化物对应水化物是酸
D.具有可变化合价
3、某元素原子序数为85,下面关于该元素说法不正确的是:( )
A.它的银盐不溶于水
B.它的氢化物很不稳定
 C.它的单质是白色固体
C.它的单质是白色固体
D.该元素位于元素周期表第六周期、第十七列
4、短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4。下列说法正确的是( )
A.W、Y、Z的电负性大小顺序一定是Z>Y>W
B.Y、Z形成的分子的空间构型可能是正四面体
C.W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
D.WY2分子中σ键与π键的数目之比为2:1
5、X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素,X+既无电子也无中子,Z原子的最外层电子数与最内层相等,Y、Z的最高正价之和与Q的最高正价相等,W的最高正价与最低负价代数和为0。X的单质与Q的单质混合强光照时可发生爆炸。下列说法正 确的是( )
确的是( )
A.直接电解海水可获得Z的单质
B.原子半径:Q>W>Z>Y>X
C.Q的含氧酸一定是强酸
D.Q的一种氧化物可作为自来水的杀菌消毒剂
6、下列排序正确的是( )
A.沸点:PH3<NH3<H2O
B.碱性:Ba(OH)2<Ca(OH)2<KOH
C.熔点:MgBr2<SiCl4<BN
D.酸性:H2CO3<HClO <HNO3
7、原子总数相同、电子总数或价电子总数相同的互为等电子体,等电子体具有结构相似的特征。下列各对粒子中,空间结构相似且互为等电子体的是( )
A.CS2与NO2 B.C6H6与B3N3H6
C.H2O与NH3 D.PCl3与BF3
8、下列有关化学用语的说法不正确的是( )
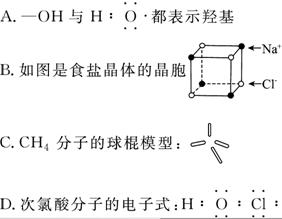
9、下列说法或有关化学用语的表达正确的是( )
A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
B.基态Fe原子的外围电子排布图为
C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大
D.根据原子核外电子排布的特点,在Fe元素周期表中位于ds区
10、下列对一些实验事实的理论解释正确的是( )
|
选项 |
实验事实 |
理论解释 |
|
A |
氮原子的第一电离能大于氧原子 |
氮原子2p能级半充满 |
|
B |
足球烯(C60)在苯中的溶解度大 |
足球烯是原子晶体 |
|
C |
金刚石的熔点低于石墨 |
金刚石是分子晶体,石墨是原子晶体 |
|
D |
HF的沸点高于HCl |
HF的相对分子质量小于HCl |
11、下列关于晶体的说法正确的组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、、H2O、H2S晶体的熔点依次降低
④离子化合物中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和1 2个O2-相紧邻
2个O2-相紧邻
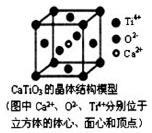
⑥金刚石硬度很大是因为金刚石的分子间作用力很强
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠溶于水时离子键被破坏
A.①②③⑥ B.①②④ C.③⑤⑦ D.③⑤⑧
12、现有三种元素的基态原子的电子排布式:①1s22s22p63s23p4;②ls22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是( )
A.第一电离能:③>②>①
B.原子半径:③>②>①
C.电负性:③>②>①
D.最高正化合价:③>②>①
13、下列各组微粒的空间构型相同的是( )
①NH3和H2O ②NH和H3O+
③NH3和H3O+ ④O3和SO2
⑤CO2和BeCl2 ⑥SiO和SO
⑦BF3和Al2Cl6
A.全部 B.除④⑥⑦以外
C.③④⑤⑥ D.②⑤⑥
14、关于化学式[TiCl(H2O)5]Cl2.H2O的配合物的下列说法中正确的是( )
A.配位体是Cl-和H2O,配位数是9
B.中心离子是Ti4+,配离子是[TiCl(H2O)5]2+
C.内界(做配体的)和外界中的Cl的数目比是1∶2
D.加入足量AgNO3溶液,所有Cl-均被完全沉淀
15、最近发现一种由钛(Ti)原子和碳原子构成的气态团簇分子,分子模型如图所示,其中圆圈表示钛原子,黑点表示碳原子,则它的化学式为( )

A.TiC B.Ti13C14
C.Ti4C7 D.Ti14C13
16、下列有机物分子中有手性的是( )
A.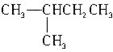 B. HCHO
B. HCHO
C.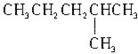 D.
D.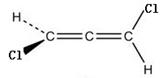
17、有5种元素X、Y、Z、Q、T。X原子M层上有2个未成对电子且无空轨道;Y原子的特征电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的P能级上只有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述不正确的是( )
A.元素Y和Q可形成化合物Y2O3
B.T和Z各有一种单质的空间构型为正四面体形
C.X的最高价氧化物的立体构型为三角锥型
D.ZO2是极性键构成的非极性分子,Z原子的杂化方式为sp杂化
18、下列叙述错误的是( )
①离子键没有方向性和饱和性,而共价键有方向性和饱和性 ②配位键在形成时,是由成键双方各提供一个电子形成共用电子对 ③金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用 ④在冰晶体中,既有极性键、非极性键,又有氢键 ⑤化合物NH4Cl和CuSO4.5H2O都存在配位键 ⑥NaCl、HF、CH3CH2OH、SO2都易溶于水,但原因 不完全相同( )
不完全相同( )
A.①③ B.②④
C.②⑤ D.④⑥
19、下列关于晶体的说法中,不正确的是( )
①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性 ②含有金属阳离子的晶体一定是离子晶体 ③共价 键可决定分子晶体的熔、沸点 ④MgO的晶格能远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小 ⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列 ⑥晶体尽可能采取紧密堆积方式,以使其变得比较稳定 ⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl和NaCl晶体中阴、阳离子的配位数都为6
键可决定分子晶体的熔、沸点 ④MgO的晶格能远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小 ⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列 ⑥晶体尽可能采取紧密堆积方式,以使其变得比较稳定 ⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl和NaCl晶体中阴、阳离子的配位数都为6
A.①②③ B.②③④
C.④⑤⑥ D.②③⑦
20、已知H3PO3为二元酸,为中强酸,而H3AsO3的酸性与H3PO3差异很大,为极弱的 酸。下列描述中不正确的是( )
酸。下列描述中不正确的是( )
A.H3PO3的结构为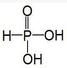
B.H3AsO3的结构为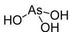
C.H3As O3与H3PO3一样,也为二元酸
O3与H3PO3一样,也为二元酸
D.H3AsO3为三元酸,且价层电子对构型为正四面体。
21、X、Y、Z、W、R、E是六种短周期元素,右图是这六种元素的主要化合价与其原子序数的关系,下列说法不正确的是( )
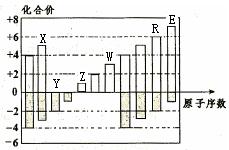
A.原子半径:Z>W>R>E
B.R的气态氢化物比X的气态氢化物沸点高
C.Z与Y可形成含共价键且熔融状态能导电的化合物
D.Z的最高价氧化物对应水化物与W的最高价氧化物对应水化物能发生 反应
反应
22、下列说法正确的是( )
A.含有离子键和共价键的化合物一定是离子化合物
B.11H2O、 12H2O、13H2O互为同位素
C.目前人们已发现的元素种类数目与原子种类数目相同
D.1H的质量数为1,所以氢元素的相对原子质量近似为1
Ⅱ卷(共56分)
23.(12分)有A、B、C、D、E、F六种微粒,其中A-E五种微粒均由两种元素组成且均含10个电子,它们有如图所示的转化关系:
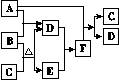
(1)写出微粒的空间构型:A________、C________。
(2)六种微粒中互为等电子体的是________(写微粒的化学式)。
(3)A-E五种微粒中含有配位键的是________(写微粒的化学式)。
(4)与E所含元素相同的18电子分子为_____________,其电子式为_________________。
(5)E极易溶于D,其原因是________________________________________________。
(6)将过量的F滴加到CuSO4溶液中,生成深蓝色的溶液,向该深蓝色的溶液中加入乙醇,析出深蓝色固体,加入乙醇的作用是_________________,将得到的深蓝色固体中的2个配体用Cl-取代,可得到两种产物,该深蓝色固体中配离子的立体构型为________________________(填“平面正方形”或“正四面体”)。
24、(16分)下表标出的是元素周期表的一部分元素,回答下列问题:
|
1 |
|
|
|
|||||||||||||||
|
2 |
|
|
|
|
D |
|
B |
A |
|
|||||||||
|
3 |
J |
I |
H |
|
C |
G |
F |
E |
||||||||||
|
4 |
L |
K |
|
|
|
|
|
|
|
|
M |
|
|
|
|
|
N |
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)表中用字母标出的14种元素中,化学性质最不活泼的是___________(用元素符号表示),最高价氧化对应的水化物碱性最强的是______________(用化学式表示),氢化物最稳定的是___________(用化学式表示),常温下单质为液态的非金属元素是__________(用元素符号表示)。
(2)M的基态原子的价电子排布式为_________________,属于______区元素。向M和氨水的混合物中不断通入氧气,M不断溶解,形成深蓝色的溶液,写出该反应的化学反应方程式______________________________________________。
(3)这14种元素中第一电离能最小的是________(用元素符号表示,下同),电负性最大的是_________ _____,I、H、C、G四种元素的第一电离能从大到小的顺序为_______________________________。
_____,I、H、C、G四种元素的第一电离能从大到小的顺序为_______________________________。
(4)这些元素中除稀有气体外第三周期中原子半径最小的是___________(填元素符号),这些元素中除稀有气体外第三周期中离子半径最小的是________(填离子符号)。
(5)J和B可以形成原子个数比为1:1的化合物,用电子式表示该化合物的形成过程____________________________________________________________。
25、(共14分)(1)石墨晶体属于___________晶体(填晶体类型),它能够导电的原因是__________________________________________________________________。
(2)金刚石属于___________晶体(填晶体类型),其中碳原子的配位数为_________________。若碳原子的原子半径为r,则晶胞的边长为__________(用r 表示),金刚石的密度为______________(用r 表示)。
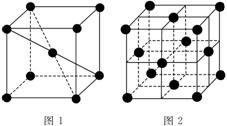
(3)1 183 K以下纯铁晶体的基本结构单元如图1所示,1 183 K以上转变为图2所示结构的基本结构单元,在1中铁原子的配位数为________;其中为密堆积的是__________(填“1”或“2”);1中的空间利用率为_____________。
(4)如图为NaCl晶体结构图,图中直线交点处为NaCl晶体中Na+与Cl-所处的位置(不考虑体积的大小)。该晶胞可以看成Cl-做_____________堆积(填堆积类型),Na+填充在
Cl-组成_____________空隙内(填空隙名称),用 Cl-的半径r表示该空隙的孔径大小为_______________,且Na+填充该空隙的填充率为________________,决定该填充率大小的因素是_____________________________________________________。

26.(14分)已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F。其中A原于核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中只有两对成对电子;C元素的电离能数据如下表; D元素的电负性是同周期元素中最大的; F原子最外层电子数与B的相同,其余各层均充满电子。
|
各级电离能 |
电离能数值kJ/mol |
|
第一电离能 |
578 |
|
第二电离能 |
1817 |
|
第三电离能 |
2745 |
|
第四电离能 |
11575 |
|
第五电离能 |
14830 |
|
第六电离能 |
18376 |
请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1) B和D形成的化合物的熔点比C和D形成的化合物的熔点________(填“高”或“低”),理由是______________________________________________________________;冶炼C单质时加入的降低熔点的物质中含有的化学键类型有______________________(填“离子键”或“共价键”或“配位键”)
(2)E的价电子排布图为_ ________________________,E的最高价氧化物对应的水化物的浓溶液与F的单质反应的化学方程式为_____________________________________________。
________________________,E的最高价氧化物对应的水化物的浓溶液与F的单质反应的化学方程式为_____________________________________________。
(3)碳元素与E形成的化合物是_____________键形成的__________________ 分子(填“极性”或“非极
分子(填“极性”或“非极 性”);其中碳原子的杂化方式为__________,该分子中含有σ键和π键的数目之比为________________。
性”);其中碳原子的杂化方式为__________,该分子中含有σ键和π键的数目之比为________________。
(4)A、C形成的化合物具有高沸点和高硬度,是一种新型无机非金属材料,则其化学式为________,其晶体中所含的化学键类型为________。
长安一中2015~2016学年度第二学期第一次月考