
1.[2012贵阳中考35(4)题1分]化学能改善我们的生活环境,提高生活质量,推动社会的进步。请根据所学的化学知识回答下列问题。
燃烧与我们的生活以及社会的发展有着密切的联系。通过对如图的分析你发现可燃物燃烧不仅需要氧气,还需同时具备的条件是________________________________________________________________________。
2.(2015贵阳中考31题 4分)通过化学实验,可以体验探究的过程,也可以从事实中得出结论或规律。分别设计简单的实验,完成下表内容,达到实验目的。
|
实验 |
实验步骤 |
实验现象 |
实验结论 |
|
(1)燃烧条件之一:需要可燃物 |
|
|
|
|
(2)稀盐酸呈酸性 |
|
|
|
|
(3)化学反应中不通过燃烧也可获得热量 |
|
|
|
 化石燃料
化石燃料
3.[2014贵阳中考32(1)(2)题5分]“生态安全环境治理”是生态文明贵阳国际论坛2014年年会的一个主题。化学在防治大气污染和水污染方面发挥了重要作用,使更多的化学生产工艺和产品向着环境友好的方向发展。
 图①
图①
 图②
图②
 图③
图③
(1)根据图①,如果把煤燃烧看做是C与O2的反应,燃烧的煤炉里可能发生的化学反应共有________个。为使煤充分燃烧,合理的做法是________(写一种做法),这对于节约能源非常重要。
(2)为从源头消除污染,人们在生产、生活中选择对环境影响小的燃料。充分燃烧1kg天然气和煤所产生的二氧化碳和二氧化硫质量如图②、③所示,通过比较选择________燃烧对环境影响较小。随着科技发展,氢气将会成为主要能源之一,氢气在空气中燃烧的反应方程式为____________,请比较分析选用氢气作为能源的优点是________________________________________________________________________。
4.[2013贵阳中考36(3)题3分]贵阳市家用燃料的下列变迁,让我们认识了化学的重要价值。
-→-→
图1
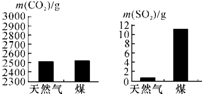 图2
图2
充分燃烧1kg天然气和煤所产生的CO2和SO2的质量如图2所示。为此,改用天然气作燃料的优点是____________。天然气(主要成分为CH4)燃烧的化学方程式为________________________________________________________________________。
 能源的利用和开发
能源的利用和开发
5.[2013贵阳中考35(5)题1分]一年的化学学习,我们感受到了化学的重要和化学的美,形成了一些化学基本观念。
化学反应伴随能量变化。人类需要的大部分能量由化学反应产生。如酒精燃烧即是________(选填“放热”或“吸热”)反应。
 ,中考考点清单)
,中考考点清单)
 燃烧与灭火(高频考点)
燃烧与灭火(高频考点)
1.燃烧与灭火
|
燃烧 |
灭火 |
|
|
|
正文 |
通常情况下,可燃物跟空气中的①______发生的一种发热发光剧烈的②______反应 |
原理 |
破坏可燃物的条件 |
|
燃 烧 的 条 件 |
|
|
|
|
有③________ |
|
|
|
|
跟⑤________接触 |
|
|
|
|
达到燃烧所需的⑦________(即着火点) |
灭 火 的 方 法 |
|
|
|
隔离④______ |
|
|
|
|
隔绝⑥______ |
|
|
|
|
降低温度到⑧______以下 |
|
|
|
|
能燃烧 |
三者缺一不可 |
能灭火 |
三者必具其一 |
[易错点]①不是所有的燃烧都有氧气参加,如金属钠在氯气中可以燃烧,镁带能在CO2中燃烧。
②着火点:是物体燃烧所需的最低温度,它是物体的固有性质,一般不随外界条件发生改变,对于某种物体来说,只能降低温度,不能降低着火点。
2.生活中常用灭火器的适用范围
|
灭火器 |
灭火原理 |
适用范围 |
|
干粉灭 火器 |
隔绝空气 |
扑灭一般性火,还可以扑灭油、气等燃烧引起的火 |
|
CO2灭 火器 |
降温, 隔绝空气 |
扑灭图书、档案贵重设备,封密仪器街头物的火 |
|
水基灭火 器(泡沫 灭火器) |
隔绝空气 |
扑灭汽油、柴油、木材、棉布等引起的火 |
|
高压水枪 |
降低温度 |
一般可燃物引起的火 |
3.常见的灭火实例、灭火方法、灭火原理
|
实例 |
灭火方法 |
灭火原理 |
|
森林灭火 |
砍倒树木, 造成隔离带 |
隔离可燃物 |
|
熄灭酒精灯 |
灯帽盖灭 |
隔绝空气 |
|
棉被着火 |
洒水 |
降低温度到着火点灯 |
|
仪器室着火 |
CO2灭火器 |
降温,隔绝氧气 |
|
油罐车着火 |
高压水枪喷水 |
降低温度到着火点 以下 |
4.发现火险或遇到火灾时的应对措施
(1)如果火势不大,应根据起火的原因选择合适的方法和灭火器,将火扑灭;
(2)如果火势很大,且蔓延的速度很快,应立即拨打119火警电话并采取必要的自救措施。例如:用湿毛巾捂着口鼻,蹲下贴近地面或沿着墙角迅速离开火险区域。
 实验突破:燃烧条件的探究
实验突破:燃烧条件的探究
1.燃烧条件的探究
中考说明要求“完成的基础的学生实验”
|
装置 |
 |
|
原理 |
4P+5O22P2O5 |
|
现象 |
①甲装置中薄铜片上的白磷燃烧;②甲装置铜片上的红磷不燃烧;③甲装置热水中的白磷不燃烧;④乙装置的白磷燃烧 |
|
现象 分析 |
①温度达到白磷的着火点,且与空气接触;②温度没有达到红磷的着火点;③没有与空气接触;④测试达到着火点,且与氧气接触 |
|
铜片和水 的作用 |
铜片:载体传热;水:隔绝空气,提供热量 |
|
结论 |
燃烧需要的条件:可燃物温度达到着火点,与氧气接触,三者缺一不可 |
|
结论分析 |
①甲中红磷不燃烧,白磷燃烧现象对比得出,燃烧需要温度达到着火点;②水中的白磷不燃烧,铜片上的白磷燃烧,现象对比得出燃烧需要跟氧气接触;③向水中的白磷通入氧气(即使是在水中)也能燃烧,说明满足可燃物温度达到着火点,跟氧气接触的条件,白磷就能燃烧 |
2.实验设计中运用的实验方法:
(1)对比实验法:铜片上的白磷与红磷是一组对比实验,白磷的着火点低可燃烧,红磷的着火点高而不能燃烧。说明燃烧需要的温度达到可燃物的着火点,铜片上的白磷与水中的白磷是另一组对比实验,说明燃烧需要与氧气接触。
(2)条件控制法:把白磷放在热水中,通过液封而隔绝空气,其设计意图是:提供可燃物与反应所需的温度使可燃物隔绝氧气,检验是否能够燃烧(提供燃烧所需的任意两个条件而控制另一个条件)。
3.实验装置的评价改进。

由于铜片中的白磷露置在空气中,燃烧产生白烟对空气造成了污染,所以对该实验装置加以改进。图A,把红磷和白磷放在U型管的两端,中间用细沙隔离,管口分别绑上两个瘪气球。图B,把红磷和白磷分别放在两支试管中,试管口上分别绑上瘪气球,让白磷在密闭的容器中燃烧。图C,试管中的氧气与白磷接触,在水中燃烧(出现水火相容的现象),改进后的装置,容易操作,现象明显。
 易燃物、易爆物的安全知识
易燃物、易爆物的安全知识
1.缓慢氧化、自燃和爆炸
(1)缓慢氧化:氧化反应进行得________,甚至不易被察觉,如动植物的呼吸作用,食物的腐烂,酒和醋的酿造,农家肥的腐熟等都属于________。
(2)自燃:________在自然环境中,达到了燃烧的条件,(由缓慢氧化引起)就能引起自发燃烧,如白磷很容易自燃。
(3)爆炸、易燃物满足:①在有限空间;②快速燃烧;③聚积大量的热三个条件就会发生爆炸。
[特别提醒]油库、面粉加工厂、纺织厂和煤矿井下就容易使其易燃物满足这三个条件,在这些地方都会严禁烟火。
设问:如果在这些地方严禁烟火,能发生爆炸吗?如果不能,缺少哪一个条件?加油站为什么四面是敞开的?缺少哪一个条件?
2.常见燃烧的爆炸有关图示

3.与燃烧、爆炸有关的安全知识
(1)煤气泄漏需要立即关闭阀门,并打开门窗通风。
(2)室内起火,应用湿毛巾捂住口鼻、蹲下贴近地面或沿墙壁迅速离开起火区域。
 化学反应中的能量变化
化学反应中的能量变化
1.化学反应中的能量变化
(1)能量变化通常表现为________的变化。
放热反应:燃烧产生热量
不燃烧产生热量
吸热反应:C+CO22CO
(2)能量的意义:
人类所需的大部分能量都是通过________产生的。如燃料燃烧产生的热量用来________、取暖、发电、________、发射________、开山炸石等。
 化石燃料(高频考点)
化石燃料(高频考点)
1.化石燃料
当前人类利用的三大化石燃料:__________、________、________,都是________能源。
(1)煤:被称为“工业的________”,是混合物,主要含有________元素,还会有少量的氢、硫、氧等元素以及无机矿物质,煤中含有硫、氧,大量烧煤会生成SO2、NO2,还有CO,会对空气造成严重污染。
(2)石油:被称为“工业的________”,是混合物,主要含有________、________等,组成物质种类有多种,沸点不同,将它们进行分离,得到溶剂油、汽油、煤油和柴油等多种产品。
[特别提醒]煤的干馏是化学变化,石油的蒸馏是物理变化。
(3)天然气:主要成分是________(CH4),是化石燃料中的________燃料,可燃冰的主要成分是甲烷的水合物,燃烧的化学方程式为________________________________________________________________________。
(4)燃料充分燃烧的条件和意义:
①条件:a.燃料燃烧需要________的空气,b.燃料与空气要有________的接触面积。
②意义:提高燃料的利用率,减少环境污染。
2.使用化石燃料对环境的影响
(1)汽车燃料燃烧产生的主要污染物:________、未燃烧的碳氢化合物、氮的氧化物、含铅化合物和烟尘等。
(2)煤燃烧产生的污染物:________、________、________及烟尘等。二氧化硫、二氧化氮在空气中发生反应后的生成物溶于雨水,形成酸雨。
 能源的利用和开发
能源的利用和开发
1.能源的分类
|
能源分类 |
意义 |
实例 |
|
不可再 生能源 |
随其本身的转化或人类的利用而减少的能源 |
煤、石油、天然气等 |
|
可再生 能源 |
不随其本身转化或人类的利用而减少的能源 |
太阳能、风能、地热能、水能、氢能、乙醇等 |
2.清洁能源和新能源
常见清洁能源:通过化学变化产生能源,乙醇和氢气;不需发生化学变化就能产生的能源:电能、风能、太阳能。
|
名 称 |
制取途径 |
产生能量的反应 |
优点 |
|
氢 气 |
①Zn+H2SO4===ZnSO4+H2↑ ②2H2O2H2↑+O2↑ |
2H2+O22H2O |
原料来源广泛,燃烧产生的热量高,生成物是水,不污染环境,是清洁的燃料 |
|
乙醇 (俗称 酒精) |
粮食酿造 |
C2H5OH+3O22CO2+3H2O |
节约石油资源,污染少 |
3.目前人们正在利用和开发许多新能源:太阳能、风能、核能、地热能、潮汐能等。
[特别提醒]氢气不能被广泛使用:因为制取氢气的成本高,贮存困难。制取氢气最理想的途径是用太阳能使水分解。
 保护环境
保护环境
1.使用化石燃料对环境的影响
(1)化石燃料燃烧造成空气污染,主要有以下几方面原因:
①燃料中的一些杂质如________等燃烧时,产生空气污染物如________等;
②燃料燃烧不充分,产生________等;
③未燃烧的________及炭粒、尘粒等排放到空气中形成浮尘。
(2)酸雨的形成
煤燃烧时排放出________、________等污染物,这些气体或气体在空气中反应后的生成物溶于雨水,会形成酸雨。
2.使燃料充分燃烧通常考虑两点:一是____________________________________;二是燃料与空气要有________________________________。
3.汽车尾气的污染与防治
(1)汽车用的燃料多是汽油或柴油。它们燃烧时产生的一些物质直接排放到空气中,会对空气造成污染。尾气中主要污染物有____________和未燃烧的________、________的氧化物和含________化合物以及________等。
(2)为减少燃料使用和汽车尾气对空气的污染,目前所采用的主要措施有:
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________;
④________________________________________________________________________。 ,中考重难点突破)
,中考重难点突破)
 燃烧的条件和灭火的原理
燃烧的条件和灭火的原理
[例1](2014兰州中考)在蜡烛及其燃烧实验的探究中,用嘴吹灭蜡烛的原理是( )
A.降低蜡烛的着火点
B.清除可燃物
C.隔绝空气
D.使其温度降至着火点以下
[解析] 物质的着火点是物质的固有属性,一般是不变的,故A错误;用嘴吹灭蜡烛时,可燃物并没有消除,故B错误;吹灭蜡烛时没有隔绝空气,故C错误;用嘴吹蜡烛,使燃着的烛心温度降低到其火点以下,蜡烛熄灭,D正确。故选D。
1. 野炊结束后,同学们及时用沙土盖灭火堆,其主要灭火原理是( )
野炊结束后,同学们及时用沙土盖灭火堆,其主要灭火原理是( )
A.将可燃物与氧气隔离
B.撤离可燃物
C.降低可燃物的着火点
D.降低可燃物的温度
[方法指导]1.燃烧是剧烈的发光放热的化学反应,不一定有氧气参加,例如镁条在二氧化碳气体中燃烧。
2.着火点与温度:着火点和温度的概念不同,着火点是可燃物燃烧所需的最低温度,一般不可变;而温度是一个变量,物体燃烧需要温度达到可燃物的着火点。
 探究燃烧的条件
探究燃烧的条件
[例2](2014苏州中考)为探究物质的燃烧条件,某同学进行了如图所示的实验,下列有关说法正确的是( )

A.现象①③说明物质燃烧需要达到一定的温度
B.现象①②说明白磷的着火点比红磷的着火点低
C.现象②③说明物质燃烧需要氧气
D.现象②说明红磷不是可燃物
[解析] 现象①③不同是因为铜片上的白磷满足了物质燃烧的三个条件因而可以燃烧,而水中的白磷不燃烧是因为不与氧气接触,未涉及红磷与白磷着火点的对比,故A错误;现象②红磷不燃烧是因为温度没有达到着火点,现象③水中的白磷不燃烧是因为不与氧气接触,选取的对比实验不合理,因此不能说明物质燃烧需要氧气,故C错误;现象②红磷不燃烧,是因为温度没有达到红磷的着火点,不能说明红磷不是可燃物,D错误。故选B。
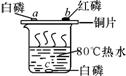
2. 下图是探究燃烧条件的实验,图中出现火焰的地方是________点(选填“a”、“b”或“c”)。烧杯中热水的作用是升温和________________________________________________________________________。
下图是探究燃烧条件的实验,图中出现火焰的地方是________点(选填“a”、“b”或“c”)。烧杯中热水的作用是升温和________________________________________________________________________。
 易燃物和易爆物的安全知识
易燃物和易爆物的安全知识
[例3](2014永州中考)下列气体混合物,遇明火可能会发生爆炸的是( )
A.H2、CO2 B.CO、O2
C.H2、CO D.CO、N2
[解析] H2具有可燃性,CO2不具有助燃性,缺少助燃性物质,A错误;CO具有可燃性,O2具有助燃性,两者的混合气体遇明火可能发生爆炸,B正确;H2、CO都具有可燃性,缺少助燃性物质,C错误;CO具有可燃性,N2不具有助燃性,缺少助燃性物质,D错误。故选B。
3. 煤矿的矿井内,空气中常混有可燃性的气体和粉末,它们遇到明火就有可能发生________事故。为防止事故的发生,煤矿的矿井内通常采取的安全措施是______________________________。
煤矿的矿井内,空气中常混有可燃性的气体和粉末,它们遇到明火就有可能发生________事故。为防止事故的发生,煤矿的矿井内通常采取的安全措施是______________________________。
[方法指导]1.爆炸:爆炸不一定是由化学变化引起的,常见的爆炸分为两种:一种是由可燃物在有限的空间里急剧的燃烧,在短时间里聚集大量的热,使气体的体积迅速膨胀而引发爆炸,属于化学变化;一种是气体物质在有限的空间内,因受热等原因使体积急剧膨胀而引发的爆炸,属于物理变化,如汽车轮胎爆炸。
2.爆炸极限:可燃性气体等在空气中达到一定含量时,遇火源就会发生爆炸。这个能发生爆炸的含量范围叫做爆炸极限,爆炸极限分为爆炸下限和爆炸上限。如果可燃性气体浓度低于爆炸下限,遇明火既不会燃烧,也不会发生爆炸;如果高于爆炸上限,遇到明火,虽然不会爆炸,但接触空气点燃能燃烧。
 化石燃料
化石燃料
[例4](2014常德中考)下列不属于化石燃料的是( )
A.石油 B.煤 C.天然气 D.酒精
[解析] 煤、石油、天然气是三大化石燃料,属不可再生能源;酒精属于可再生能源,不属于化石燃料。故选D。
4. 下列关于煤、石油和天然气的说法错误的是( )
下列关于煤、石油和天然气的说法错误的是( )
A.在地球上的蕴藏量都是有限的
B.都是可再生能源
C.都属于混合物
D.完全燃烧时都有二氧化碳生成
 绿色能源
绿色能源
[例5](2014重庆中考)氢气作为21世纪极具开发前景的新能源之一,理由是( )
①燃烧热值高 ②原料资源丰富
③贮存和运输时安全性高 ④燃烧产物无污染
A.①②③ B.①②④ C.②③④ D.①③④
[解析] 氢气作为燃料的优点有:氢气燃烧产物是水,不污染环境;氢气燃烧的热值高;氢气可以通过电解水得到,原料资源丰富,①②④正确;由于现阶段氢气的制作成本高,贮存、运输较困难,作为燃料尚不能广泛使用,③错误。故选B。
5. 从环境保护的角度看,下列能源中最清洁的是( )
从环境保护的角度看,下列能源中最清洁的是( )
A.石油 B.煤 C.天然气 D.氢气
[方法指导]能源分为可再生能源和不可再生能源。可再生能源是不随本身的转化或人类利用而减少的能源,如太阳能、水能、风能等;不可再生能源是随本身的转化或人类的利用而减少,在短时间内不能恢复的能源,如化石燃料等。
 保护环境
保护环境
[例6](2014抚州中考)去年10月,我市多地出现了几次较为严重的雾霾天气,从而再次引起人们对空气质量的关注,下列一些行为和举措,有利于改善空气质量的是( )
A.力推火力发电 B.燃放烟花爆竹
C.露天焚烧垃圾 D.推广使用乙醇汽油
[解析] 火力发电一般为燃煤发电,煤燃烧过程中会产生大量有害气体和粉尘,不利于改善空气质量,A错误;燃放烟花爆竹会产生大量的污染空气的二氧化硫等气体和粉尘,不利于改善空气质量,B错误;露天焚烧垃圾产生大量的污染空气的气体和粉尘,不利于改善空气质量,C错误;推广使用乙醇汽油,乙醇汽油的使用可有效地降低汽车尾气中有害气体的排放,改善能源结构,从而改善空气质量,D正确。故选D。
6. 为了减少汽车尾气的污染,下列措施中不可取的是( )
为了减少汽车尾气的污染,下列措施中不可取的是( )
A.改进发动机燃烧方式,以便汽油能完全燃烧
B.使用催化、净化装置,使有害气体转化成无害气体
C.将汽车尾气全部收集起来不排放
D.使用无铅汽油,禁止含铅类物质排放