
1.PM 2.5是指大气中直径小于或等于2.5 μm的颗粒,大气中PM 2.5含量增高易导致雾霾天气。下列关于雾霾的说法错误的是( )
A.工业废气、汽车尾气是产生雾霾的主要原因 B.倡导市民骑自行车上、下班,减少雾霾
C.就地焚烧大量农作物秸秆会加重雾霾 D.为了减少雾霾的危害,禁止使用化石燃料
2.生活中应用缓慢氧化的实例很多,下列反应中不属于缓慢氧化的是( )
A.酒和醋的酿造 B.农家肥料的腐熟
C.酒精灯的燃烧 D.人在长跑时呼吸
3.科学家用单个分子制成了“纳米车”,它能在人工操纵下运输药物分子到病源处释放以杀死癌细胞。下列有关“纳米车”的说法正确的是( )
A.“纳米车”的研制成功说明分子要在人为外力作用下才能运动 B.“纳米车”分子不是由原子构成的 C.“纳米车”运输药物分子的过程是肉眼可以直接看见的 D.“纳米车”研制成功说明在一定条件下人可以控制分子运动
4.最近科学家发现,水在-157℃超低温、正常压力或真空条件下仍呈液态,但比蜂蜜还粘稠。下列关于这种“高密度液态水”的说法正确的是( )
A.化学性质与普通水不同 B.分子不再运动 C.氢、氧两种原子的个数比为2︰1 D.分子间的间隔比普通水大
5.下列关于O和O2−的认识正确的是( )
A.氧离子比氧原子的化学性质稳定 B.它们的核内质子数不相同
C.它们不属于同种元素 D.它们的核外电子数相同
6.某同学为了探究微观粒子总是在不断地运动着,设计了如下图所示实验,其中不能达到目的的是( )
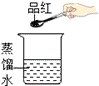
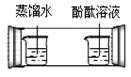

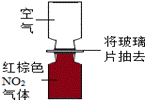
A B C D
7.推理是学习化学的一种重要的方法。下列推理得出的相关结论合理的是( )
A.阳离子一定带正电荷,所以带有正电荷的粒子一定是阳离子
B.化合物是由不同种元素组成的纯净物,所以只含一种元素的物质一定不是化合物
C.氧化物中一定含有氧元素,所以含有氧元素的化合物一定是氧化物
D.同种元素的粒子具有相同的质子数,所以具有相同质子数的粒子一定属同一种元素
8.将汽车尾气中的有毒气体转化为空气中的成分,其微观结构示意图如下,下列说法不严谨的是( )
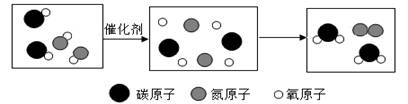
A.反应前有两种物质的分子
B.化学变化的本质是:分子分成原子,原子重新组合成新物质的分子
C.在化学变化中,分子分成原子,原子重新组合成新物质
D.图中共有三种氧化物
9.对一个问题要多方面深入分析,用这样的思想方法对下面的问题作出判断:经测定某物质只含有一种原子,则下列推断正确的是( )
A.该物质中一定只含同种分子 B.该物质一定是纯净物
C.该物质中可能含不同种分子 D.该物质一定是混合物
10.某同学利用如图装置做了“空瓶生烟”的化学小魔术。操作步骤如下:
(1)将软塑料瓶中充满氨气,用胶塞塞紧;
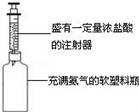 (2)用注射器取一定量的浓盐酸;
(2)用注射器取一定量的浓盐酸;
(3)把注射器针头穿过胶塞,缓缓向瓶中注入浓盐酸,观察到空瓶中产生浓浓的白烟,发生反应的化学方程式为:NH3+HCl═NH4Cl。
下列有关说法中,正确的是( )
①NH4Cl为白色固体 ②该反应属于分解反应 ③会观察到软塑料瓶变瘪的现象。
A.①③ B.①② C.②③ D.①②③
11.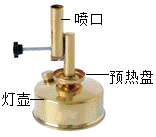 座式酒精喷灯的火焰温度可达1000℃以上。使用时,向预热盘中注入酒精(C2H5OH)并点燃,待灯壶内酒精受热气化从喷口喷出时,预热盘内燃着的火焰就会将喷出的酒精蒸气点燃.下列说法不正确的是( )
座式酒精喷灯的火焰温度可达1000℃以上。使用时,向预热盘中注入酒精(C2H5OH)并点燃,待灯壶内酒精受热气化从喷口喷出时,预热盘内燃着的火焰就会将喷出的酒精蒸气点燃.下列说法不正确的是( )
A.预热过程中,分子的运动速率发生了改变
B.在燃烧的过程中,分子的种类发生了改变
C.酒精从喷口喷出时,分子体积发生了明显的改变
D.该实验过程既发生了物理变化又发生了化学变化
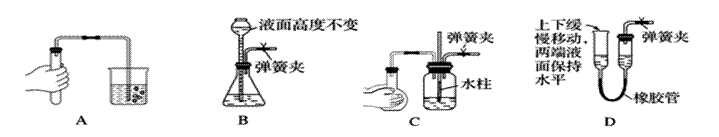
12.下列各图所示装置的气密性检查中,一定漏气的是( )
13.如图所示,两个甲分子反应生成三个乙分子和一个丙分子,从图示获得信息,不正确的是( )

A.物质分类时甲物质属于化合物 B.该反应在基本反应类型中属于分解反应
C.该反应生成的丙物质属于单质 D.乙分子由1个A原子和1个B原子构成
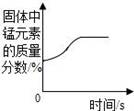
14.下列图象能正确反映相关变化关系的是( )
|
A |
B |
C |
D |
 |
 |
 |
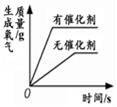 |
|
测定空气中 氧气的含量 |
加热一定量的 高锰酸钾固体 |
将水通直流 电一段时间 |
用等质量、等浓度 的双氧水制取氧气 |
第Ⅱ卷(非选择题,共58分)
15.(12分)在“宏观−微观−符号”之间建立联系,是学习化学的一种重要思维方式。
观察下列原子结构示意图和元素周期表(部分),回答有关问题。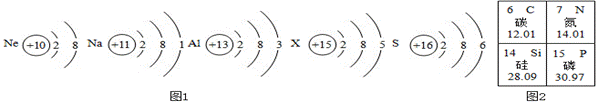
(1) 图1中,具有相对稳定结构的原子是 (填元素符号)。
(2) 图1中,属于金属元素的是 、 (填元素名称)。
(3) 含有X元素的化合物常用作化肥,X元素的原子序数是 ,相对原子质量为 。
(4) 在某金属单质与硫单质反应过程中,硫原子得到2个电子形成硫离子。下列说法正确的是______(填字母序号)。
A.硫离子属于阴离子 B.硫离子可表示为S2+
C.“S”既可以表示1个硫原子,也可以表示硫元素 D.硫离子的核外电子数与质子数相等 (5) Al3+中右上角数字3 的含义 。
(6) 食盐的主要成分是氯化钠,氯化钠是由 和 构成的。(填化学符号)
(7) 右下图为元素周期表中的一部分,X、Y、Z代表三种不同元素,以下判断正确的是 。
|
|
He |
||
|
X |
|
|
|
|
Y |
Z |
|
|
A.原子序数:Z>X
B.核外电子数:X=Y
C.Y和Z处于同一族
D.X和Y的化学性质相似
(8)气体甲在氧气中燃烧生成氮气和水,甲分子中一定含有的原子是 和 (填符号)。
16.(16分)水是生命之源,没有水就没有生命。
(1) 从物质的分类角度分析,水不属于___(填字母)
 A.单质 B.氧化物 C.化合物
D.纯净物
A.单质 B.氧化物 C.化合物
D.纯净物
(2) 右图为电解水的实验,a试管中收集到的气体为 ,
此反应的符号表达式(能写化学方程式最好) ,
此实验可以说明水是由 组成的;
从能量转化角度分析,电解水是将 能转化为 能。
(3)自来水厂净水过程的主要操作流程如下图:

[资料:常用的絮凝剂有明矾[ KAl(SO4)2.12H2O ],消毒剂有液氯。]
回答下列问题:
①操作X 的名称是 。
②明矾的作用是 ;其原理是明矾与水反应生成氢氧化铝胶状物。
③液氯(化学式Cl2)杀菌消毒属于 变化(填“物理”或“化学”),液氯也会与水中杂质反应生成一些对人体有害的物质。因此,水煮沸后,仍需要打开壶盖继续加热一会儿。
 ④自来水厂的净水过程 (填“能”或“不能”)将硬水软化成软水,
④自来水厂的净水过程 (填“能”或“不能”)将硬水软化成软水,
生活中将硬水软化的方法是 。
(4)海水淡化可缓解淡水资源匮乏的问题。右图为太阳能海水淡化装置图。
水变成水蒸气的过程中,不发生变化的是 (填字母序号)。
A.分子质量 B.分子运动 C.分子间隔 D.分子种类
这种方法与实验室通过 (填操作名称)净化水的方法原理相同。
(5)右图净水器入水口在下方的优点是 。
A.使水的化学性质发生改变 B.有助于除去悬浮性颗粒
C.不易堵塞活性炭孔 D.可以将硬水软化
 (6)保护水环境,珍爱水资源,是每个公民应尽的责任和义务。为了防止水的污染,下列做法有利于保护水资源的是(填序号)______。
①抑制水中所有动、植物的生长; ②不任意排放工业废水;
(6)保护水环境,珍爱水资源,是每个公民应尽的责任和义务。为了防止水的污染,下列做法有利于保护水资源的是(填序号)______。
①抑制水中所有动、植物的生长; ②不任意排放工业废水;
③大量使用化肥农药; ④生活污水经过净化处理后再排放。
17.(12分)知识整合是巩固化学知识的一种重要手段,请看下面某同学的知识整合:
A、B、C、E、F、G、H、甲、乙都是初中化学中的常见物质,它们之间有如下转换关系。已知A为暗紫色固体,B为黑色固体,甲和E常温下都为液体,乙和F、H都为白色固体,其中反应⑤是烟幕弹里的主要化学反应。
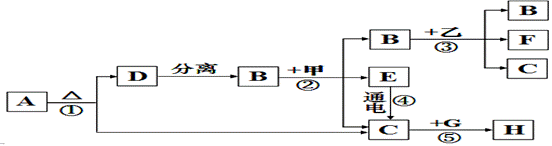
(1) H的化学式为 ,D 属于 (“混合物”或“纯净物”)。
(2)反应①的符号表达式(能写化学方程式最好)为 。
(3) 反应③的符号表达式(能写化学方程式最好)为 。
(4)反应⑤的反应条件是 ,反应类型为 。
在我们所学的化学知识中,反应⑤还常用于测空气中氧气的含量,在此测定中可能出现氧气的含量偏大的情况,写出其中一条可能的原因 。
(5)从微观的角度:分析甲与E的化学性质不相同的原因是 ,区别甲与E的方法是 。
(6)反应①、②的共同点有(答一点) 。
18.(13分)在实验室里选用下图中A-G的装置可以制取氧气。
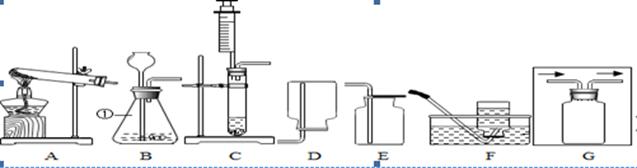
(1)实验室选择上图中某发生装置进行高锰酸钾制取O2,请指出该装置的缺陷: 。 (2)某同学选用装置B和F来制取氧气。 ①请写出该方法制氧气的的符号表达式(能写化学方程式最好)为 。 ②装置B中的长颈漏斗下端管口要浸在液面下,其目的是 ______。
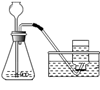 ③在实验过程中,该同学动作太慢,氧气还没有收集满,锥形瓶中的反应就已经停止(如右图).若想集满这瓶氧气,在不拆卸装置的前提下,请你帮他想出两种解决的方法:
;
___ _。
④与装置B相比,C装置的优点有:
。
A.便于控制反应快慢 B.定量添加药品更方便 C.生成氧气质量更大
③在实验过程中,该同学动作太慢,氧气还没有收集满,锥形瓶中的反应就已经停止(如右图).若想集满这瓶氧气,在不拆卸装置的前提下,请你帮他想出两种解决的方法:
;
___ _。
④与装置B相比,C装置的优点有:
。
A.便于控制反应快慢 B.定量添加药品更方便 C.生成氧气质量更大
(3) 回收二氧化锰,需要进行过滤操作。过滤时, 的末端要轻轻的斜靠在三层滤纸的一边。过滤结束后,小心取下滤纸,将纸上的固体 (操作名称),转移装瓶,贴上标签。
回收的二氧化锰,还可以在上述反应中反复使用。其原因是 。(4) 实验室常用氯化铵固体与熟石灰固体共热来制取氨气。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,NH3极易溶于水.请根据信息回答下列问题: ①实验室制取氨气,可选用的发生装置是______,收集装置可以是______(填序号);
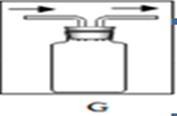
②若用如图G装置进行“排空气法”收集制取的NH3,请把图中的“导气管”补画完整。
19.(5分)同学们应用数字化实验探究外界条件对双氧水分解速率的影响。实验装置如图:
[进行实验]
|
序号 |
主要实验步骤 |
装置内压强−时间图象 |
|
实 验 1 |
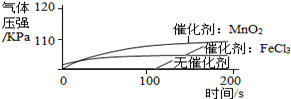
①1号抽滤瓶中不加任何试剂, 2号抽滤瓶中加入0.2 g MnO2粉末, 3号抽滤瓶中加入0.2 g FeCl3粉末。 ②用三支分液漏斗分别加入15 mL 4%的H2O2溶液。 |
 |
|
实 验 2 |
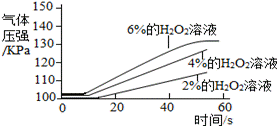
①三个抽滤瓶中分别加入0.2 g FeCl3粉末。 ②分别用1号分液漏斗加入15 mL2%的H2O2溶液;用2号分液漏斗加入15 mL4%的H2O2溶液;用3号分液漏斗加入15 mL6%的H2O2溶液。 |
 |
|
实 验 3 |
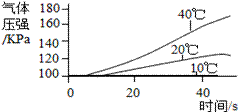
①三个抽滤瓶中分别加入0.2 g FeCl3粉末,分别放入装有10℃、20℃、40℃水的水槽中。 ②用三支分液漏斗分别加入15 mL4%的H2O2溶液。 |
 |
[解释与结论]
(1)某同学得到“不同催化剂的催化效果不同”的结论,他的依据是 ___。
(2) 通过上述实验得到:影响该反应速率的外界因素有 __。
[反思与评价](3)经过多次实验,有的同学对比实验1的3号瓶、实验2的2号瓶中同为40s时的气体压强,发现存在较大的差异,可能的原因是 ___。
题号 1 2 3 4 5 6 7
答案 D C D C A B B
题号 8 9 10 11 12 13 14
答案 C C A C C D B
15.(12分)
(1)__ Ne ____
(2)___钠____ 、____铝_____
(3)___15_____,____30.97_____
(4)___A C____
(5)_每个铝离子带三个单位正电荷__
(6)___ Na+__________和_____Cl-________
(7)___A D__________
(8)___N___和 ___H___
16.(16分)
(1)___A____
(2)___H2___ , 略 ,
水是由 氢元素和氧元素 组成的;
___电___ ___化学____
(3) ①___过滤_____
②___吸附杂质,使杂质沉淀___
③___化学___
④___不能___ ___煮沸___
(4) __A D___ ___蒸馏___
(5) __B C___
(6) __②_④__
17.(12分)
(1)__ P2O5___ ___混合物 __
(2)___略______________________________
(3)___略______________________________
(4) ___点燃___ _化合反应__
___止水夹没有夹紧 ;燃烧匙伸入瓶内太慢__
(5) _分子构成不同(或分子不同,化学性质不同),
_取样品分别加入二氧化锰,有气泡冒出的是甲,无气体的是E
(6)_都有氧气生成,都是分解反应,
都需要一定条件________。
18.(13分)
(1)__ 试管口未塞棉花_
(2) ①_ 略_______
②_液封,防止产生的气体从长颈漏斗逸出 _
③_从长颈漏斗添加双氧水___;
_从长颈漏斗注水_。
④__ A B___
(3)___ 玻璃棒_____ ___洗涤烘干____
MnO2 是该反应催化剂,反应前后质量和化学性质不变_
(4)①__A___,__D__
②请把图中的“导气管”补画完整 短进长出
19.(5分)
(1)__实验1中2,3号瓶曲线不同__
(2)__催化剂种类,反应物浓度,温度__
__实验温度不同____
(3)_______________________________________