
1.下列是同周期元素基态原子的最外层电子排布式,所表示的原子最容易得到电子的是 ( )
A.ns2 B.ns2np1
C.ns2np4 D.ns2np5
2.某基态原子核外共有6个电子,分布在K与L电子层上,在下列L层分布中正确的是 ( )
A. B.
B.
C.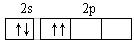 D.
D.
3.构造原理揭示的多电子原子的电子排布能级顺序,实质是各能级能量高低。若以E(nl)表示某能级的能量,以下各式中正确的是 ( )
A.E(5s)>E(4f)>E(4s)>E(3d) B.E(3d)>E(4s)>E(3p)>E(3s)
C.E(4s)<E(3s)<E(2s)<E(1s) D.E(5s)>E(4s)>E(4f)>E(3d)
4.下列分子或离子中键角由大到小排列顺序是: ( )
①BF3 ②NH3 ③H2O ④NH4+ ⑤BeCl2
A.⑤④①②③ B.⑤①④②③
C.④①②⑤③ D.③②④①⑤
5.下列各组微粒中,都互为等电子体的是 ( )
A.CO、NO、NaH、N2 B.SO2、NO、N、CNO-
C.CO、NO、BeCl2 D.SiF4、SiO、SO、PO
6.下列每组物质中化学键类型和分子的极性都相同的是 ( )
A.CO2和CS2 B.NaCl和HCl
C.H2O和CH4 D.O2和HBr
7.下面的排序不正确的是 ( )
A、.晶体熔点由低到高:CF4<CCl4<CBr4<CI4
B、硬度由大到小:金刚石>碳化硅>晶体硅
C、.熔点由高到低:Na>Mg>Al
D.、晶格能由大到小: NaF> NaCl> NaBr>NaI
8.下列各组中的两种固态物质熔化或升华时,克服的微粒间相互作用力属于同种类型的是
A.碘和氯化钾 B.金刚石和重晶石 ( )
C.二氧化硅和干冰 D.软脂酸甘油酯和冰醋酸
9.下列判断正确的是 ( )
A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大
B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7
C.晶体中一定存在化学键
D.正四面体分子中键角可能是109°28′或60°
10.对Na、Mg、Al的有关性质的叙述正确的是 ( )
A.碱性:NaOH<Mg(OH)2<Al(OH)3
B.第一电离能:Na<Mg<Al
C.电负性:Na>Mg>Al
D.还原性:Na>Mg>Al
11.下列有关叙述正确的是 ( )
A.只含有离子键的化合物才是离子化合物
B.硫酸铵晶体是含有离子键、极性键和配位键的分子晶体
C.由于I—I键的键能比F—F、Cl—Cl、Br—Br键的键能都小,所以在卤素单质中碘的熔点最低
D.在分子晶体中一定不存在离子键,而在离子晶体中可能存在共价键
12.有下列物质:①白磷;②金刚石;③石墨;④二氧化硅;⑤甲烷;⑥四氯化碳;⑦单质硅;
⑧铵根离子,其分子结构或晶体结构单元中存在正四面体的是 ( )
A.除③外 B.①②⑤⑥
C.除③⑧外 D.③④⑦⑧
13.短周期元素X、Y、Z、W、Q在元素周期表中位置如下图所示。下列说法正确的是( )
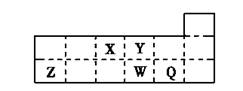
A.元素X与元素Z的最高正化合价之和的数值等于8
B.原子半径的大小顺序为:rX>rY>rZ>rW>rQ。
C.Y2-和Z3+的核外电子数和电子层数都不相同
D.元素W的最高价氧化物对应的水化物的酸性比Q的强
14.下列说法或有关化学用语的表达正确的是 ( )
A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
B.基态Fe原子的外围电子排布图为:
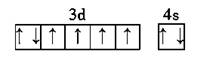
C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大
D.根据原子核外电子排布的特点,Cu在周期表中属于s区元素
15.下列关于晶体的说法中,不正确的是 ( )
①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性
②含有金属阳离子的晶体一定是离子晶体 ③共价键可决定分子晶体的熔、沸点
④MgO的晶格能远比NaCl大,这是因为前者离子所带的电荷数多,离子半径小
⑤晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列
⑥晶体尽可能采取紧密堆积方式,以使其变得比较稳定
⑦干冰晶体中,一个CO2分子周围有12个CO2分子紧邻;CsCl和NaCl晶体中阴、阳离子的配位数都为6
A.①②③ B.②③④ C.④⑤⑥ D.②③⑦
16.下列有关说法不正确的是 ( )
A.C3H8中碳原子都采用的是sp3杂化
B.O2、CO2、N2都是非极性分子
C.酸性:H2CO3<H3PO4<H2SO4<HClO
D.CO的一种等电子体为NO+,它的电子式为 +
17.关于化学式Cl2.H2O的配合物的下列说法中正确的是 ( )
A.配位体是Cl-和H2O,配位数是9
B.中心离子是Ti4+,配离子是2+
C.内界和外界中的Cl-的数目比是1:2
D.加入足量AgNO3溶液,所有Cl-均被完全沉淀
18.在有机物中,若碳原子上连接的四个原子或原子团不相同,则这个碳原子称为手性碳原子。含有手性碳原子的分子一般是手性分子具有镜像异构及光学活性,下列分子中具有光学活性的是 ( )
A.CBr2F2 B.CH3CH2OH
C.CH3CH2CH3 D.CH3CH(OH)COOH
19.正硼酸(H3BO3)是一种层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如下图),下列有关说法正确的是 ( )

A.正硼酸晶体属于原子晶体 B.H3BO3分子的稳定性与氢键有关
C.分子中硼原子最外层满足8电子稳定结构 D.1 mol H3BO3晶体中有3 mol氢键
20.六氟化硫分子为正八面体构型(分子结构如图所示),难溶于水,在高温下仍有良好的绝缘性,在电器工业方面具有广泛用途。下列推测正确的是 ( )
 A.SF6中各原子均达到8电子稳定结构
A.SF6中各原子均达到8电子稳定结构
B.SF6易燃烧生成SO2
C.SF6分子是含有极性键的非极性分子
D.SF6是原子晶体
第II卷(非选择题,共40分)
|
二、填空题(共40分) |
21.(10分)已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E的+1价阳离子的核外有3层电子且各层均处于全满状态。
(1)E元素基态原子的核外电子排布式为___________________。
(2)B、C、D三种元素的第一电离能由小到大的顺序为________(填元素符号),其原因是___________________________。
(3)B2A4是石油炼制的重要产物之一 。B2A4分子中B原子轨道的杂化类型为________;1 mol B2A2分子中含________mol σ键。
(4)已知D、E能形成晶胞结构如图所示的两种化合物,则化学式:甲为____________________,乙为______________________;高温时,甲易转化为乙的原因为___________________________。

22、(10分)某配位化合物为深蓝色晶体,由原子序数由小到大的A、B、C、D、E五种元素构成,其原子个数比为14∶4∶5∶1∶1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布式为(n-1) dn+6ns1,回答下列问题。
(1)元素B、C、D的第一电离能由大到小的排列顺序为________。(用元素符号表示)
(2)D元素原子的最外层电子排布图为____________________________
(3)该配位化合物的化学式为________,配体的中心原子的杂化方式为________。
(4)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1∶1和1∶2,两种化合物可以任意比互溶,解释其主要原因为_____________
___________________________________________________________。
(5)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为______,分子中含有________个σ键,________个π键。
23.(10分)下表中实线是元素周期表的部分边界,其中上边界并未用实线画出。

根据信息回答下列问题:
(1)基态Ga原子的最外层电子排布式为____________________
(2)铁元素位于元素周期表的__________区;Fe和CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为__________。
(3)已知:原子数目和价电子总数均相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO互为等电子体的分子和离子分别为__________和__________(填化学式)。
(4)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有__________。
(5)根据VSEPR模型预测ED的空间构型为__________。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子为__________(写3种)。
24.(10分)氧是地壳中含量最多的元素。
(1)氧元素基态原子核外未成对电子数为________个。
(2)H2O分子内的O—H键、分子间的范德华力和氢键从强到弱依次为__________________________________________________________。
 ,原因是_____________________________。
,原因是_____________________________。
(3)H+可与H2O形成H3O+,H3O+中O原子采用________杂化。H3O+中H—O—H键角比H2O中H—O—H键角大,原因为______________________。
(4)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为a g.cm-3,NA表示阿伏加德罗常数,则CaO晶胞体积为________ cm3。