
网址:http://www.1010jiajiao.com/paper/timu/1855478.html[举报]
24.(13分)“低碳循环”已引起各国家的高度重视,而如何降低大气中CO2的含量和有效地开发利用CO2正成为化学家研究的主要课题。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:___ C+ ___ KMnO4+ ____ H2SO4→____CO2↑+ ____MnSO4 + ____K2SO4+ ____ ____
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应
CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
|
实验组 |
温度℃ |
起始量/mol |
平衡量/mol |
达到平衡所需 时间/min |
||
|
CO |
H2O |
H2 |
CO |
|||
|
1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
|
2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
|
3 |
900 |
a |
b |
c |
d |
t |
①实验2条件下平衡常数K= 。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值______(填具体值或取值范围)。
③实验4,若900℃时,在此容器中加入CO、H2O、CO2 、H2均为1mol,则此时V正 V逆(填“<” ,“>” ,“=”)。
(3)已知在常温常压下:
①2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH=-1275.6 kJ/mol
②2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ/mol
③H2O(g) = H2O(l) ΔH=-44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:____________
(4)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。常温下,向10 mL 0.01 mol.L-1 H2C2O4溶液中滴加10mL 0.01mol.L-1 NaOH溶液时,比较溶液中各种离子浓度的大小关系 ;
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为1×10-4mo1/L ,则生成沉淀所需CaCl2溶液的最小浓度为 mo1/L。
化学试题参考答案
|
题号 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
答案 |
A |
D |
B |
B |
B |
C |
B |
C |
B |
D |
B |
B |
|
题号 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
21 |
22 |
23 |
/ |
|
答案 |
D |
B |
C |
C |
D |
B |
D |
B |
C |
C |
D |
/ |
24.(14分)
(1)5C+ 4 KMnO4+ 6 H2SO4→5CO2↑+ 4MnSO4 + 2K2SO4+ 6H2O
(2) ①1/6(或0.17) ②<1 ③<
(3) CH3OH(l)+O2(g)=CO (g)+2H2O(l)△H=-442.8KJ/mol
(4)c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)
(5)1.12×10-4 mol/L-4
25.(共13分)
(1)(共5分,在酸性高锰酸钾之前增加检验CO2是否除尽的装置不扣分,其它合理过程也给分)
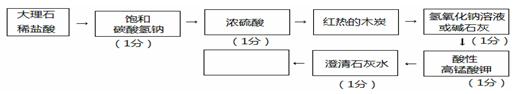
(2)①ABD(2分)(错选不得分,漏选得1分)
②Fe(CO)5+4NaOH=Na2Fe(CO)4+Na2CO3+2H2O(2分)
③Fe2O3(2分);2∶1(2分)
26.(13分)
(1) (2分)
(2分)
(2)干燥Cl2 (2分) 防止熔融的硫堵塞导管 (2分)
(3)②③①⑤④(或③②①⑤④) (2分)
(4)碱石灰(1分) 吸收Cl2尾气,防止空气中的水汽使S2Cl2水解(各1分,共2分)
(5)2S2Cl2 + 2H2O = SO2 + 3S + 4HCl (2分)
27.(14分)(1)CH2=CH2 (1分)
(2)C2H4O (1分) 2CH3CH2Cl + NH3→NH(CH2CH3)2 +2HCl (2分)
(3)取代反应(硝化反应) (2分)
(4)
 (2分)
(2分)
(5)①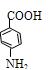 (2分)
(2分)
②
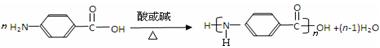 (2分)
(2分)
③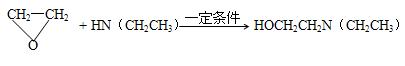 (2分)
(2分)