
网址:http://www.1010jiajiao.com/paper/timu/3058935.html[举报]
21.(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.《物质结构与性质》
⑴太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层。试写出基态镍原子的核外电子排布式 ▲ 。
 ⑵富勒烯衍生物由于具有良好的光电性能。富勒烯(C60)的结构如图1,分子中碳原子轨道的杂化类型为 ▲
;1 mol
C60分子中σ键的数目为 ▲
。科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图2所示。该化合物中的K原子和C60分子的个数比为 ▲
。
⑵富勒烯衍生物由于具有良好的光电性能。富勒烯(C60)的结构如图1,分子中碳原子轨道的杂化类型为 ▲
;1 mol
C60分子中σ键的数目为 ▲
。科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图2所示。该化合物中的K原子和C60分子的个数比为 ▲
。
⑶已知CS2与CO2分子结构相似,CS2的电子式是__ ▲ _。
⑷某配合物甲的焰色反应呈紫色,其内界由中心离子Fe2+与配位体CN-构成,配位数为6。甲的水溶液与稀硫酸在加热时发生非氧化还原反应,生成三种硫酸盐和一种与CN-是等电子体的气态化合物,反应的化学方程式为 ▲ 。
B.《实验化学》
亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:
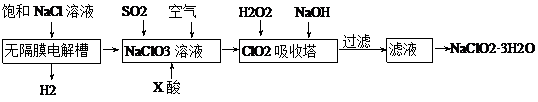
 已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体只能保持在稀释状态下以防止爆炸性分解,且需现合成现用。
③ClO2气体在中性和碱性溶液中不能稳定存在。
④在无隔膜电解槽中持续电解一段时间后,生成氢气和NaClO3,阳极的电极反应为:Cl--6e-+6OH-=ClO3-+3H2O
(1)反应生成ClO2气体需要X酸酸化的原因为: ▲ 。
(2)X酸为 ▲ 。
(3)吸收塔内的温度不能过高的原因为: ▲
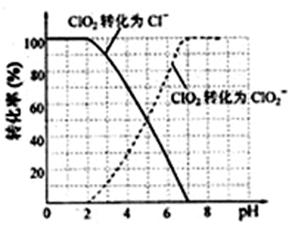
(4)吸收塔内ClO2随着还原剂的不同和溶液酸碱性的变化可被还原为ClO2-或Cl-。ClO2被S2-还原为ClO2-、Cl-的转化率与溶液pH的关系如右图所示。请写出pH≤2时ClO2与S2-反应的离子方程式:
▲ 。
(5)第二步向NaClO3溶液中通SO2的同时通入空气的原因为:
▲ 。
(6)从滤液中得到NaClO2●3H2O粗晶体的操作步骤为
a.蒸发浓缩; b. ▲ ; c.过滤。 高三年级第一学期期中考试化学试题参考答案
单项选择题:本题包括10小题,每小题2分,共计20分。每小题只有一个选项符合题意。
1~5:A C A B A 6~10:D C B B D
不定项选择题:本题包括5小题,每小题4分,共计20分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
11.CD 12.AB 13.A 14.BD 15.C
非选择题
16.(14分,每空2分)
⑴过滤 漏斗
⑵AlO、OH-(写出一个且正确的得1分,只要有错误,就得0分); 稀硫酸
⑶Al(OH)3+3H+===Al3++3H2O 在装置Ⅰ 、Ⅱ 之间增加一个盛有饱和NaHCO3溶液的洗气瓶(合理答案即给分) ⑷节约原料,防止环境污染。
17.(第(5)小题6分,其余每空2分,共14分)
(1) 2CaCO3+2SO2+O2=2CaSO4+2CO2 (2分) (2)D (2分)
(3) K2SO4在40%的乙二醇溶液中溶解度小,能充分析出 (2分)
(4) 2OH-+SO2 = SO32-+H2O(2分)
(5)解:氯气的物质的量为:0.224L/22.4L/mol=0.01mol
氯气氧化Fe2+为Fe3+,根据电子转移守恒可知Fe2+的物质的量为:0.01mol×2=0.02mol,
故氧化物中+2价铁的物质的量为:0.02mol …………………………………………(2分),
Fe2O3的物质的量为:8g/160g/mol=0.05mol,
原化合物中+3价铁的物质的量为:0.05mol×2-0.02mol=0.08mol……………………(2分),
故FeO与Fe2O3的物质的量之比为:0.02mol:0.08mol/2=1:2,
该产品化学式为:FeO•2Fe2O3或Fe5O7………………………………………………(2分)
18.(12分)(1)H2O+CO2+NH3==NH4HCO3 (2分)
(2)检查装置气密性(2分)
①固体氢氧化钠或碱石灰(2分)
②不需要干燥;提供低温环境,提高转化率(2分,答对任意一点就给分)
③氢氧化钠固体溶于水产生大量热,使浓氨水分解产生氨气(2分)
④ 调节恒压滴液漏斗旋塞,减慢氨水滴加速度(2分)
19. (14分)
a (2分)
①2:1 (2分) ② c (2分)
取最后一次洗涤滤液,滴入1-2滴盐酸酸化的BaCl2溶液,若不出现白色沉淀,表示已洗涤完全(2分)
(4)
[实验步骤]①A (2分) ②C (2分)
[问题探究]④促进Fe3+水解转化为沉淀并使过量的H2O2分解除去(2分)
20.(每空2分,共14分)
(1)① -1527.6kJ /mol ② CD
(2)该反应是一个熵增的反应 (△S>0)(2分)
(3)① > ②33.3% (4)① b ② CH3OH+8OH--6e-=CO32-+6H2O
21A 《物质结构与性质》(12分)
⑴ 1s22s22p63s23p63d84s2或[Ar]3d84s2 (2分)
⑵sp2 (2分) 90NA (2分) 3:1 (2分)
⑶ (2分)
(2分)
⑷ K4Fe(CN)6+6H2SO4+6H2O 2K2SO4+FeSO4+3(NH4)2SO4+6CO↑(2分)
2K2SO4+FeSO4+3(NH4)2SO4+6CO↑(2分)
(K4Fe(CN)6写对得1分,方程式全对得2分)
21B.《实验化学》 (12分)

说明:试卷中其他合理答案均可酌情给分。