
网址:http://www.1010jiajiao.com/paper/timu/3077345.html[举报]
24.(12分)Na2O2与水的反应实际是Na2O2 +2H2O═2NaOH+H2O2,反应放热使部分H2O2受热分解:2H2O2═2H2O+O2↑。为了测定某过氧化钠固体的纯度,做如下实验(假设杂质不参加反应)
①称取过氧化钠固体2.00g
②把这些过氧化钠固体放入气密性良好的气体发生装置中
③向过氧化钠中滴加水,用某一量筒排水集气,量筒内液面在112mL处恰好与水槽内液面相平
④将烧瓶中的液体转移到250mL的容量瓶中,洗涤并将洗涤液也转入容量瓶,然后加入蒸馏水,定容,使液面恰好与刻度相切
 ⑤取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4 溶液去滴定,至终点时用去了24.20mLKMnO4 溶液(此时锰全部以Mn2+ 存在)
⑤取25.00mL容量瓶中的液体,放入锥形瓶中,用过量的稀硫酸酸化,然后用0.01mol/L的KMnO4 溶液去滴定,至终点时用去了24.20mLKMnO4 溶液(此时锰全部以Mn2+ 存在)
(1)有500mL、250mL、150mL的量筒备用,应选用量程为______的量筒。
(2)在步骤③测量气体体积时,必须待烧瓶和量筒内的气体都冷却到室温时进
行,若此时量筒内的液面高于水槽中液面(如图),立即读数会使Na2O2的
纯度______(填“偏高”“偏低”或“不变”);应进行的操作是 。
(3)在步骤⑤中反应的离子方程式是______判定滴定达到终点的依据是 。
(4)该过氧化钠的纯度为______。(保留一位小数;实验中得到的气体体积均看作为标准状况下)
化学答案
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
A |
D |
C |
D |
D |
B |
C |
B |
B |
D |
|
11 |
12 |
13 |
14 |
15 |
16 |
17 |
18 |
19 |
20 |
|
A |
C |
D |
A |
B |
A |
C |
B |
B |
C |
21.(1)6∶3∶2 (2分) 23∶12∶9 (2分)
22.(1)NaNO2 (2分) (2)①④ (2分) (3)B (2分)
(4) 10 Al+ 6 NaNO3+ 4 NaOH = 10 NaAlO2+ 3 N2↑+ 2 H2O (2分)
11.2L (2分)
23.(1)NH4+ (2分) SO42- (2分)
(2)Cl- (2分)
取少量废水试样,滴加足量的Ba(NO3)2溶液,静置;取上层清液,滴加硝酸酸化的AgNO3溶液,若有白色沉淀产生,则存在Cl-;若无白色沉淀产生,则不存在Cl- (3分)
(3)6I-+2NO+8H+===3I2+2NO↑+4H2O (2分)
24.(1)150mL(2分)
(2)偏高(2分) 应慢慢把量筒往下移,使量筒中液面恰好与水槽中液面相平(2分)
(3)2MnO4-+5H2O2+6H+ = 2Mn2++5O2↑+8H2O(2分)滴入最后一滴溶液刚好由无色变为浅紫红色,且在半分钟内不褪色(2分)
(4)62.6% (2分)
25.(1)2:1 (4分) (4)2.4mol/L(4分)
26.(1)C4H8(1分)
(2)消去反应(1分)、氧化反应(1分)
(3)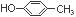 (2分)
(2分)
 (4)(CH3)2CHCHO
+ 2Cu(OH)2 + NaOH →(CH3)2CHCOONa + Cu2O↓+ 3H2O(3分)
(4)(CH3)2CHCHO
+ 2Cu(OH)2 + NaOH →(CH3)2CHCOONa + Cu2O↓+ 3H2O(3分)
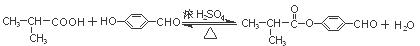 (3分)
(3分)
(5)6种(2分);(四种结构邻、间、对各3种,共12种)
 (2分)(邻、间、对任写一种即可)
(2分)(邻、间、对任写一种即可)