
网址:http://www.1010jiajiao.com/paper/timu/4166031.html[举报]
2.常温下,用0.100 mol.L-1的NaOH溶液分别滴定20.00 mL 0.100 mol.L-1的盐酸和0.100 mol.L-1的醋酸,得到两条滴定曲线,如图所示:
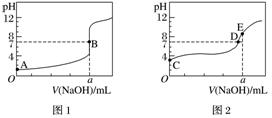
下列说法正确的是( )
A.滴定盐酸的曲线是图2
B.两次滴定均可选择甲基橙或酚酞作指示剂
C.达到B、E点时,反应消耗的n(CH3COOH)=n(HCl)
D.以HA表示酸,当0 mL<V(NaOH)<20.00 mL时,图2对应混合液中各离子浓度由大到小的顺序一定是c(A-)>c(Na+)>c(H+)>c(OH-)
答案 C
解析 0.100 mol.L-1盐酸的pH=1,0.100 mol.L-1醋酸的pH>1,故A项错误;甲基橙的变色范围是3.1-4.4、酚酞的变色范围是8.2-10.0,由图2中pH突变的范围(>6)可知,当氢氧化钠溶液滴定醋酸时,只能选择酚酞作指示剂,B项错误;B、E两点对应消耗氢氧化钠溶液的体积均为a mL,所以反应消耗的n(CH3COOH)=n(HCl),C项正确;0 mL<V(NaOH)<20.00 mL时,图2对应混合溶液可能显中性,此时c(A-)=c(Na+)>c(H+)=c(OH-),D项错误。