
网址:http://www.1010jiajiao.com/paper/timu/4190673.html[举报]
14.一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。
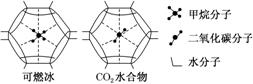
“可燃冰”中分子间存在的2种作用力是________。为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知上图中笼状结构的空腔直径为0.586nm,根据下述图表,从物质结构及性质的角度分析,该设想的依据是______________________。
|
参数 |
|
|
|
分子 |
分子直径/nm |
分子与H2O的结合能 |
|
E/kJ.mol-1 |
|
|
|
CH4 |
0.436 |
16.40 |
|
CO2 |
0.512 |
29.91 |
参考答案
1.[解析]H2O2是极性分子,分子内既有极性键,又有非极性键,而CS2为非极性分子,根据“相似相溶”规律,H2O2难溶于CS2。
[答案]极性 非极性 极性H2O2为极性分子,而CS2为非极性溶剂,根据“相似相溶”规律,H2O2难溶于CS2
2.[解析]氨分子之间形成氢键,分子间作用力增大,故沸点高于膦(PH3)
[答案]高于 NH3分子间可形成氢键
3.6NA CH3COOH分子间存在氢键
4.<  中形成分子内氢键,使其更难电离出H+
中形成分子内氢键,使其更难电离出H+

6.[解析]该有机物分子易与水分子形成分子间氢键,而2丁烯则不能,故该有机物在水中的溶解度大于2丁烯
[答案]大
7.平面三角 加成产物CH3OH分子之间能形成氢键
8.硅烷为分子晶体,随相对分子质量增大,分子间作用力增强,熔沸点升高
9.[解析]由于该晶体具有和石墨相似的层状结构,所以B原子采取sp2杂化,同层分子间的作用力是范德华力,由于“在硼酸[B(OH)3]分子中,B原子与3个羟基相连”虽然三个B-O都在一个平面上,但σ单键能够旋转,使O-H键位于两个平面之间,因而能够形成氢键,从而使晶体的能量最低,达到稳定状态。
[答案]sp2,氢键
10.极性共价键、范德华力
11.N、O、F X物质形成分子内氢键,Y物质形成分子间氢键,分子间氢键使分子间作用力增大
12.sp2 7NACO(NH2)2分子与水分子之间能形成氢键
 [答案]172 低
[答案]172 低
14.[解析]可燃冰中存在分子间作用力即范德华力,另外水分子间还存在氢键。分子与H2O的结合能越大表明越容易与H2O结合。
[答案]氢键、范德华力 CO2的分子直径小于笼状结构空腔直径,且与H2O的结合能大于CH4
15.离子键、氢键、范德华力