
网址:http://www.1010jiajiao.com/paper/timu/4190890.html[举报]
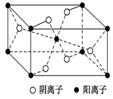
6.Z基态原子的M层与K层电子数相等,它与某元素形成的化合物的晶胞如下图所示,晶胞中阴离子和阳离子的个数之比是________。
参考答案
1.[解析]甲中N(x)∶N(y)=1∶=2∶1;乙中N(a)∶N(b)=1∶=1∶1;丙中N(c)=12×+1=4,N(d)=8×+6×=4。
[答案]2∶1 1∶1 4 4
2.[解析]由图可知,晶胞中A位于顶点,晶胞中含有A为8×=1个,B位于晶胞的体心,含有1个,O位于面心,晶胞中含有O的个数为6×=3则化学式为ABO3。
[答案]ABO3
3.[解析]晶胞中含有X原子数目=8×+1=2,含有Cu:4,晶胞的化学式Cu2X;根据晶胞结构,与X等距离且最近的X原子个数为8个。
[答案]Cu2X 8
 [答案]VO2
[答案]VO2
5.[解析]Cu原子位于面心,个数为6×=3,Ni原子位于顶点,个数为8×=1,铜原子与镍原子的数量比为3∶1。
[答案]3∶1
6.2:1
7.[解析]根据晶胞结构利用切割法分析,每个晶胞中含有铜原子个数为8×+6×=4,氯原子个数为4,该化合物的化学式为CuCl;则1 mol晶胞中含有4 mol CuCl,1 mol晶胞的质量为4×99.5 g,又晶胞参数a=0.542 nm,此晶体的密度为g.cm-3。
[答案]CuCl
8.[解析]O2-半径大于Na+半径,由F的晶胞结构可知,大球代表O2-,小球代表Na+,每个晶胞中含有O2-个数为8×+6×=4,含有Na+个数为8,故O2-、Na+离子个数之比为4∶8=1∶2,从而推知F的化学式为Na2O。由晶胞结构可知,每个O原子周围有8个Na原子,故O原子的配位数为8。晶胞参数a=0.566 nm=0.566×10-7 cm,则晶胞的体积为(0.566×10-7cm)3,从而可知晶体F的密度为≈2.27 g.cm-3。
[答案] Na2O 8 ≈2.27g.cm-3
9.[解析]GaAs的熔点为1 238 ℃,其熔点较高,据此推知GaAs为原子晶体,Ga与As原子之间以共价键键合。分析GaAs的晶胞结构,4个Ga原子处于晶胞体内,8个As原子处于晶胞的顶点、6个As原子处于晶胞的面心,结合“均摊法”计算可知,每个晶胞中含有4个Ga原子,含有As原子个数为8×+6×=4(个),Ga和As的原子半径分别为rGapm=rGa×10-10cm,rAspm=rAs×10-10 cm,则原子的总体积为V原子=4×π×[(rGa×10-10cm)3+(rAs×10-10cm)3]=×10-30(r+r)cm3。又知Ga和As的摩尔质量分别为MGag.mol-1和MAsg.mol-1,晶胞的密度为ρg.cm-3,则晶胞的体积为V晶胞=cm3,故GaAs晶胞中原子的体积占晶胞体积的百分率为×100%=×100%=×100%。
[答案]原子晶体 共价×100%
 [答案]分子 Mg2NiO3
[答案]分子 Mg2NiO3
11.[解析]CaF2晶体中Ca2+的配位数为8,F-的配位数为4,Ca2+和F-个数比为1∶2,一个晶胞中实际拥有的Ca2+为8×+6×=4,F-为8个,晶胞顶点及六个面上的离子为Ca2+,晶胞内部的离子为F-,1个晶胞实际拥有4个“CaF2”。则CaF2晶体的密度:4×78 g.mol-1÷[(a×10-8 cm)3×6.02×1023mol-1]= g.cm-3。
[答案]8 g.cm-3
12.由金刚石的晶胞结构可知,晶胞内部有4个C原子,面心上有6个C原子,顶点有8个C原子,晶胞中C原子数目为4+6×+8×=8;若C原子半径为r,金刚石的边长为a,根据硬球接触模型,则正方体对角线长度的就是C-C键的键长,即a=2r,所以r=a,碳原子在晶胞中的空间占有率w===。
[答案]8 =
13.3∶1结构相似的分子晶体的相对分子质量越大,分子间作用力(或范德华力)越强,熔化所需的能量越多,故熔点:Si60>N60>C60;而破坏分子需断开化学键,元素电负性越强其形成的化学键越稳定,断键时所需能量越多,故破坏分子需要的能量大小顺序为N60>C60>Si60
14.b ×1030
15.< FeO和NiO相比,阴离子相同,阳离子所带电荷相同,但亚铁离子半径大于镍离子,所以FeO晶格能小,熔点低