
网址:http://www.1010jiajiao.com/paper/timu/4362569.html[举报]
7.(1)CS2分子中,共价键的类型有________,C原子的杂化轨道类型是________,写出两个与CS2具有相同空间构型和键合形式的分子或离子______________________。
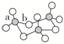
(2)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是________对,分子的立体构型为________;SO3气态为单分子,该分子中S原子的杂化轨道类型为________;SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为________;该结构中S-O键长有两类,一类键长约140 pm,另一类键长约为160 pm,较短的键为________(填图中字母),该分子中含有________个σ键。
(3)S的氢化物(H2S)分子的空间构型为________。
(4)①与OH-互为等电子体的一种分子为________(填化学式)。
②醛基中碳原子的轨道杂化类型是________;1 mol乙醛分子中含有的σ键的数目为________。
(5)BCl3和NCl3中心原子的杂化类型分别为________和________。
(6)已知元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍,则在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是________,YZ的空间构型为________。
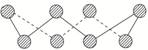
(7)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是________。
(8)甲醛(H2C===O)在Ni催化作用下加氢可得甲醇(CH3OH),甲醇分子内C原子的杂化方式为________,甲醇分子内的O-C-H键角________(填“大于”、“等于”或“小于”)甲醛分子内的O-C-H键角。
[解析] (1) CS2分子中,存在σ键和π键。CS2分子中,C原子的价层电子对数为2,杂化轨道类型为sp。根据等电子理论,与CS2具有相同空间构型和键合形式的分子有CO2、COS和N2O,离子有NO、SCN-。(2)SO2分子中S原子价电子排布式为3s23p4,价层电子对数是3对,分子的立体构型为V形;SO3气态为单分子,该分子中S原子的杂化轨道类型为sp2杂化;SO3的三聚体环状结构如图所示,该结构中S原子的杂化轨道类型为sp3杂化;该结构中S-O键长有两类,一类键长约140 pm,另一类键长约为160 pm,较短的键为a,该分子中含有12个σ键。(3)H2S的结构类似于H2O,为V形。(4)①OH-有2个原子,10个电子,与其互为等电子体的分子是HF。②乙醛中甲基的C原子是sp3杂化,醛基的C原子是sp2杂化,一个乙醛分子中4个C-H σ键,1个C-C σ键,1个C-O σ键,共6个σ键。(5)BCl3中B原子3个价电子全部成键,杂化类型为sp2,NCl3中N原子有一个孤电子对,N的杂化类型为sp3。(6)Y基态原子的3p轨道上有4个电子,Y为S元素,元素Z的原子最外层电子数是其内层的3倍,Z是O元素。H2S中S原子的杂化方式为sp3,SO的空间构型为正四面体。(7)S8中每个S原子连接2个S原子,S原子还有2个孤电子对,所以S的杂化方式为sp3。(8)甲醇中碳原子形成四个σ键,为sp3杂化,甲醇分子内O-C-H键角接近109°28′,甲醛分子的空间构型为平面形,键角接近120°。
[答案] (1)σ键和π键 sp CO2、SCN-(或COS等)
(2)3 V形 sp2 sp3 a 12 (3)V形
(4)①HF ②sp2 6NA (5)sp2 sp3
(6)sp3 正四面体 (7)sp3 (8)sp3 小于