
网址:http://www.1010jiajiao.com/paper/timu/4401560.html[举报]
16.蓝铜矿主要含有[Cux(OH)y(CO3)z],还含有少量Fe、Si的化合物。常用于治疗黄水引起的麻风病、皮肤瘙痒症,受热时分解成三种氧化物。为了确定其组成,某研究小组设计了下图实验。
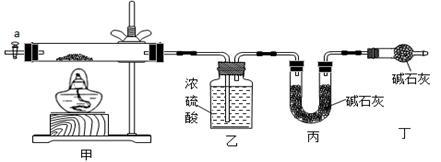
(1)实验步骤:①称取3.46g样品于硬质玻璃管内,称量乙、丙装置的质量;②按如图所示装置组装好仪器,并检查装置的气密性;③加热甲中玻璃管,当乙瓶内不再有气泡产生时,停止加热;④打开活塞a,缓缓通入空气数分钟之后,称量乙、丙装置的质量;⑤计算。
步骤④中缓缓通入空气数分钟的目的是 。
(2)某同学发现上述装置中存在一个明显的缺陷,为解决这一问题,可将装有 (填名称)固体的干燥管连接在活塞a之前。
(3)若按正确装置进行实验,测得如下的数据,则该蓝铜矿的化学式为 。
|
|
乙装置的质量/g |
丙装置的质量/g |
|
加热前 |
76.00 |
60.00 |
|
加热后 |
76.18 |
60.88 |
(4)1mol氨气通过灼热的蓝铜矿时可产生1.5mol金属铜,写出该反应的化学方程式: 。
(5)胆矾(CuSO4.5H2O)可杀菌消毒、配制波尔多液,用蓝铜矿制备该晶体的方案如下:
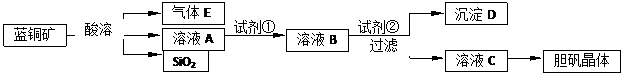
①溶液A中的金属离子有Cu2+、Fe2+、Fe3+,则实验中的试剂①可选用 (填字母)
a.KMnO4 b.Cl2 c.H2O2 d.稀HNO3
②准确量取20.00mL溶液A于锥形瓶中,用0.01200mol.L—1酸性高锰酸钾标准溶液滴定是应选用
(填“酸式”或“碱式”)滴定管,滴定至终点时消耗KMnO4标准溶液15.00mL,则溶液A中Fe2+的浓度为 mol.L—1。
③已知:
|
金属离子(0.1mol.L—1) |
Fe3+ |
Fe2+ |
Cu2+ |
|
|
PH |
氢氧化物开始沉淀 |
1.48 |
6.34 |
4.67 |
|
氢氧化物完全沉淀 |
2.18 |
8.34 |
6.67 |
加入试剂②CuO的作用是调节溶液的PH,若采用标准比色卡对照,则PH的范围应为 。
[习题7--金属铜的冶炼]