
网址:http://www.1010jiajiao.com/paper/timu/505562.html[举报]
12.某温度下在2 L密闭容器中加入一定量A,发生以下化学反应:2A(g)B(g)+C(g) ΔH=-48.25 kJ.mol-1
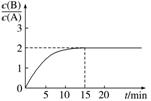
反应过程中B、A的浓度比与时间t有下图所示关系,若测得第15 min时c(B)=1.6 mol.L-1,下列结论正确的是( )
A.该温度下此反应的平衡常数为3.2
B.A的初始物质的量为4 mol
C.反应到达平衡时,放出的热量是193 kJ
D.反应达平衡时,A的转化率为80%
答案 D
解析 根据c(B)=1.6 mol.L-1,n(B)=3.2 mol,看图可推知n(A)=1.6 mol,根据三步法计算可知
2A(g)B(g)+C(g)
开始/mol x 0 0
变化/mol 6.4 3.2 3.2
平衡/mol 1.6 3.2 3.2
可以计算出x=8 mol,B错误;K==4,A错误;A的转化率为(8-1.6)/8=80%,D正确;到达平衡时生成B为3.2 mol,放出的热量是3.2 mol×48.25 kJ.mol-1=154.4 kJ,C错误。