
2006年山东省淄博市初三第二学期期中考试
第一卷
相对原子质量:H:1 C:12 N:14 O:16 Ca:40 Cl:35.5 S:32 P:31
一、选择题:(请将各小题的正确选项填入下表,50分)每小题有1~2个正确答案
1、早期化学家为了认识空气的本质,将一些物质放在密闭的容器中进行实验,结果发现每次都有约1/5的空气不知去向,当时化学家把这1/5的空气称为“有用的空气”,这种“有用的空气”是指
A、氮气 B、氧气 C、二氧化碳 D、稀有气体
2、下列有关空气的说法中,正确的是
A、空气是一种实实在在的物质
B、空气是一种纯净物
C、空气是由几种元素组成的纯净物
D、洁净的空气也是混合物
3、下列做法中,能减缓化学反应速率的是
A、面团发酵时放在温热处
B、人在进食时细细咀嚼食物
C、在食品密封包装时充入氮气
D、煤燃烧时向煤炉中鼓入空气
4、下列物质中属于氧化物的是
A、Na2SO4 B、NaOH C、O3 D、Fe3O4
5、医物人员用3%的过氧化氢溶液为伤者处理伤口时,伤口上会看到大量的气泡。下列有关说法中,错误的是
A、生成的气体可能是过氧化氢分解产生的氧气
B、只有二氧化锰能够使过氧化氢在常温下迅速分解产生氧气
C、过氧化氢和水的分子构成不同,所以它们的化学性质不同
D、伤口处的生物酶可能对过氧化氢的分解起到催化作用
6、燃放烟花爆竹能增添节日的气氛。有关对烟花、爆竹成分的推测不合理的是
A、鞭炮爆炸后,产生有刺激性气味的气体,说明鞭炮中可能含有硫粉
B、燃放烟花时,发出耀眼的白光,说明烟花中可能含有镁粉
C、鞭炮的火药呈黑色,说明鞭炮中可能有木炭粉
D、燃放烟花时,发出蓝紫色火焰,说明烟花中可能有铁粉
7、对实验现象的观察和分析,有助于获得化学知识并学会科学探究的方法。下列对实验现象的分析科学的是
A、某物质完全燃烧产生一种能够使石灰水变浑浊的气体和水,证明该物质的组成中一定含有碳、氢、氧三种元素
B、把燃着的木条插入某无色气体中,火焰熄灭,该气体可能是二氧化碳
C、将相同质量的蔗糖放入不同温度的水中,温度高的水中的蔗糖溶解的快,说明蔗糖溶解的速率大小只与温度有关
D、将一固体放入试管内的某液体中,发现有气体产生,因此可判断,试管内的液体一定是过氧化氢溶液
8、铁丝在空气中灼热发红,但不能燃烧,而在纯氧中却能燃烧,这一事实与下列哪一因素关系最密切
A、氧气的浓度
B、铁丝的表面积
C、集气瓶内气体的多少
D、对铁丝加热的时间
9、某些农村用明矾[KAl(SO4)x?12H2O]来净化水,根据元素的化合价来判断x为
A、1 B、2 C、3 D、4
10、下列物质分别放入一密封的充满氧气的集气瓶里,充分燃烧后,冷却至室温,由于瓶内压强明显减小,使瓶塞最难启开的是
A、木炭 B、硫 C、红磷 D、蜡烛
11、从安全、环保、节能、简便等方面考虑,实验室制氧气的最佳方法是
A、通电使水分解
2H2O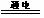 2H2↑+O2↑
2H2↑+O2↑
B、过氧化氢催化分解剂
2H2O2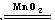 2H2O+O2↑
2H2O+O2↑
C、高锰酸钾加热分解
2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
D、氯酸钾加热分解 2KClO3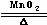 2KCl+3O2↑
2KCl+3O2↑
12、检验容器中是否收集满氧气的方法是
A、将烧红的木炭伸入容器内
B、加入澄清的石灰水
C、将带火星的木条伸入容器中
D、将带火星的木条放在容器口
13、检查装置的气密性,下列几步操作中,其顺序正确的是
①用手握住试管外壁;②把带有导管的橡皮塞塞进试管口;③把导管的一端浸在水里
A、①②③ B、③①② C、②③① D、②①③
14、质量相等的两份过氧化氢,一份中混有少量的MnO2,另一份加热,放出H2的质量m与反应时间t的关系图象正确的是(a线是纯过氧化氢曲线,b线是混有MnO2的过氧化氢曲线)

15、空气在标准状况下的密度是1.293g/L,以下四种气体中,既能用排水法收集,又能用向下排空气法收集的气体是

16、下表是某城市空气质量日报的一部分,①~⑤所示情况中,不会对表中三个空气质量指标产生影响的是

①生活垃圾的焚烧
②使用含磷洗衣粉
③火力发电厂和居民生活中用煤作燃料
④长江三峡水力发电 ⑤机动车尾气的排放
A、①②④⑤ B、②④ C、①④ D、②③④
17、下列关于化合价的说法中,正确的是
A、在H2O中,氢原子显+1价,氧原子显-2价
B、非金属元素在化合物中总显负价
C、一种元素在同一化合物中,可能有几种化合价
D、某元素的原子最外层上有5个电子,因此该元素的最低价态为-5价
18、化合物Ca(ClOx)2的相对分子质量是207,则x的值为
A、1 B、2 C、3 D、4
19、已知(NH4)2SO4和(NH4)2HPO4的混合物中氮的质量分数为21.2%,则混合物中氧元素的质量分数为
A、42.2% B、48.5% C、82% D、无法确定
20、能用质量守恒定律解释的现象是
A、酒精在敞口容器中,质量减少了
B、镁条燃烧后,质量增加了
C、湿衣服在日光下晾干了
D、水分解的质量等于生成氢气和氧气的质量总和
21、煤的气化是提高煤的利用率,减少环境污染的有效措施。煤的气化过程中发生了化学反应。C+H2O(气)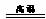 CO+H2,反应前后发生了变化的是
CO+H2,反应前后发生了变化的是
A、元素的种类 B、分子的种类 C、原子的数目 D、物质的总质量
22、芬太奴是强有力的麻醉剂,在军事上作为“非致命性武器”曾被用作解救人质,其化学式为C20H24N2O,下列关于芬太奴的说法中正确的是
A、芬太奴是由碳、氢、氧、氮四种元素组成的物质
B、芬太奴是国际禁用的杀伤性武器
C、芬太奴的每一个分子中含有47个原子
D、芬太奴中碳、氢、氧、氮四种元素的质量比为120:12:7:8
23、下列化学方程式中正确的是
A、CuSO4+NaOH=Na2SO4+Ca(OH)2
B、2Mg+O2 2MgO
2MgO
C、Fe+H2SO4=FeSO4+H2
D、CH4+2O2 CO2↑+2H2O
CO2↑+2H2O
24、某同学利用右图装置测定空气中氧气的含量,红磷燃烧后恢复至室温,打开弹簧夹发现进入广口瓶的液体液面高度超过广口瓶体积的1/5,造成这一现象的原因可能是
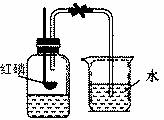
A、实验前没有将弹簧夹夹紧
B、实验装置可能漏气
C、实验中所取的红磷过量
D、实验中所取的红磷不足
25、在一个密闭容器内有M、N、X、Y四种物质,在一定条件下反应一段时间后,测得反应前后各物质的质量如下:
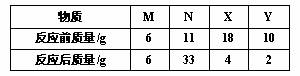
下列能正确表示容器中化学变化的表达式是
A、X+Y=M+N B、N=X+Y+M
C、X+Y+M=N D、X+Y=N
第二卷
二、填空题:(40分)
1、(4分)
(1)生命活动中离不开氧气,请你说出自然界中氧气的来源________。
(2)下列事实说明空气中有哪些成分:_____________。
①可燃物能在空气中燃烧______________。
②空气是制造氮肥的原料之一_______________。
③酥脆的饼干在空气中放置一段时间后会变软_____________。
2、(11分)完成铁丝在氧气中燃烧的实验报告:
实验题目:
(1)实验所用的仪器:_____________________。
(2)操作步骤:
①先用砂纸将细铁丝磨成光亮的_______色,
②把一端固定在粗铁丝(或燃烧匙柄)上,另一端绕成螺旋状并裹一根火柴,
③点燃火柴梗,将铁丝伸入充满氧气的集气瓶中。
(3)实验中的现象:______________。
(4)注意事项:___________原因是__________________。
(5)反应的化学方程式:___________________。
3、(4分)
由碳氢两种元素组成的化合物,若所含碳元素与氢元素的质量比为____________
8:1,则碳原子和氢原子的原子个数比为_________如果测得该化合物的相对分子质量为54,则该化合物的化学式为______________。
4、(6分)
在一个陌生的星球上充满了一种浅黄绿色的气态单质,科学家研究了该单质,确定其化学式为F2,相对分子质量为38,进一步研究证明,该元素的单质不导电,当该元素原子与金属元素原子化合时,只能形成F-,该元素原子与非金属原子化合时,只显-1价,试回答下列问题:
(1)根据上面提供的信息判断,F元素属于_________元素(填金属或非金属),
你的判断依据是_________________________________________________。
(2)钙原子与F原子化合时Ca显+2价,则这种化合物的化学式为____________。

(1)由前两行内容对照得出的规律是:元素或原子团的化合价数值往往与相应离子所带的 ________数相等。
(2)由最后一行内容对照可得出的规律是:通过元素或原子团的________可以确定相应化合物的化学。
(3)利用表格中所给内容,请你写出一种氧化物的化学式____________。
(4)根据硫酸锌的化学式ZnSO4,可推出该物质所含阳离子的符号为____________。
6、(4分)
某种能够提供医用氧气的便携式制氧器,其制氧剂为复方过碳酸钠(含A、B剂),A剂的主要成分为过碳酸钠(2Na2CO3?3H2O2)。过碳酸钠是一种易溶于水的白色固体,受热易分解,溶于水时生成碳酸钠和过氧化氢。B剂是一种难溶于水的固体。在反应仓内加入适量的水,先放入A剂,再放入B剂,即可产生氧气。
2Na2CO3?3H2O=2Na2CO3+3H2O2,2H2O2=2H2+O2↑,反应完全后,过滤、分离残余物,测得滤渣的质量与原加入反应仓内B剂的质量相等,若将滤渣与A剂、水再次混合,又有氧气生成。请回答下列问题:
(1)在制氧过程中,B剂的作用是_____________。
(2)与实验室用高锰酸钾制氧气比较,该方法更方便家庭制氧的理由之一是_______________________________________________。
(3)从贮存制氧剂,处理残渣两方面,为该制氧器的使用者各提一条合理化的建议:_______________________________________________。
7、(5分)
某实验测出人呼吸中各种气体的体积分数如下表所示:
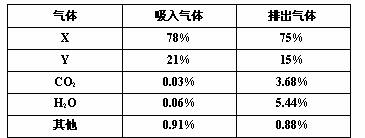
(1)请你判断:X是________,Y是_______________(填化学式)
(2)因参与人体新陈代谢而消耗的气体是__________(填化学式)
(3)X气体在呼吸过程中,没有参与化学反应,但在呼出气体中体积分数和却减少了,
原因________________________________________。
三、实验探究题:(16分)
1、(5分)
下面是测定空气中氧气体积含量的两个实验:
实验1:在集气瓶内预先装少量水,余下的容积5等分,做好标记。在带橡皮塞和导管的燃烧匙内装足量的红磷,立即伸入集气瓶内塞紧橡皮塞(如图1所示),待红磷熄灭并冷却到室温后打开弹簧夹。
实验2:将试管的容积5等分,做好标记,在试管中加入一小块白磷(足量),用橡皮塞塞紧试管口,将试管放入热水中使白磷燃烧,待白磷熄灭并冷却到室温后,将试管倒立于盛有室温下水的水槽中(如图2所示),并在水中将橡皮塞取下。
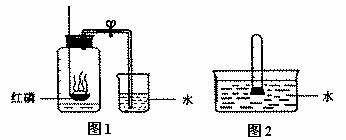
(1)写出磷燃烧的化学方程式:__________________
(2)实验2中,在水中而不在空气中取下橡皮塞的原因是_____________________________
(3)从测定结果分析,上述实验中效果较好的实验是________,
写出另一个实验的两点不足________________________
2、(7分)
催化剂在生产、生活和科研中有重要作用,实验用过氧化氢分解制氧气,常用MnO2作催化剂。
[提出问题]其他物质能作过氧化氢的催化剂吗?
[猜想]甲同学认为CuO或Fe2O3可以代替MnO2,因为按物质的分类MnO2、CuO、Fe2O3都属于
[设计实验]甲同学按下面步骤进行实验:
①在试管中加入5mL5%的过氧化氢溶液,把带火星的木条伸入试管
②用精密的天平准确称量0.5g Fe2O3红色粉末,并将其加入另一试管中
③在步骤②的试管中加入5mL5%的H2O2溶液,把带火星的木条伸入试管
④待步骤③的试管中没有气泡后,进行“某一操作”将固体洗净、干燥、称量,得红色固体的质量仍为0.5g
[现象]甲同学观察到步骤①中的现象为_________________,步骤③中带火星的木条复燃。
[反思]步骤④中进行的“某一操作”是_________________,
乙同学认为在步骤④后还需增加一个实验,请你写出该实验的操作方法和现象__________________________________________________。
[结论]通过以上步骤得出的结论是_________________________________________________请你举出一生活中应用催化剂的事例__________________________________
3、(4分)
某兴趣小组为了探究质量守恒定律,进行了如右图所示的小实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上40cm长的粗铜线,并使玻璃棒保持水平,然后,用酒精灯给左边一端铜丝加热1~2分钟。停止加热后冷却,仔细观察发生的现象。
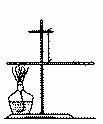
(1)冷却后,他们观察到的现象是:①______________,②_________________________。
(2)写出铜丝加热时所发生的化学方程式:______________________。
四、计算题:(14分)
1、(6分)
某地一不法商贩销售的“尿素”中,经检验含氮的质量分数为28%。
求:(1)已知尿素的化学式为CO(NH2)2,则尿素中氮元素的质量分数是多少?
(2)该商贩所售每袋“尿素”(50kg),实际含尿素多少千克?
2、(8分)
2005年5月22日,中国登山测量队成功登上珠峰顶,圆满完成珠峰高度最新测量工作。登山队员常用的能源是氢化钙(CaH2)固体,用它和水反应生成氢气供燃烧之需,化学方程式为:CaH2+2H2O=Ca(OH)2+2H2↑,请回答下列问题:
(1)CaH2中钙元素为+2价,氢元素的化合价为 。
(2)现有875g CaH2固体,与足量水反应可生成多少克氢气?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com