
2005年山东省威海市中等学校招生考试
第一卷
一、 选择题(本题包括6小题,每题3分,共18分。每题只有一个选项正确)
1.某些金属工艺品的外观有银白色的金属光泽,同学们认为它可能和铁一样,有磁性。在讨论时,有同学提出“我们可以先拿磁铁来吸一下”。就“拿磁铁来吸一下”这一过程而言,属于科学探究中的
A.假设 B.实验 C.观察 D.做出结论
2.按照一定的依据把物质进行分类,是我们认识物质的组成、结构、性质和用途的便捷途径。姜宇同学在家中建立了小小化学实验室,他收集了许多物质,其中有:①纯碱;②生石灰;③醋酸;④熟石灰;⑤酒精;⑥铜;⑦石墨;⑧氧化铁;⑨蔗糖;⑩尿素。
对上述物质的分类不正确的是
A.属于有机物的有③⑤⑨⑩ B.属于单质的有⑥⑦
C.属于碱的有①④ D.属于氧化物的有②⑧
3.下列关于实验室制取氢气的四种说法中,正确的是
A.必须选择含氢元素的物质作原料 B.必须用排水法收集氢气
C.必须使用锌与稀硫酸反应 D.必须使用酒精灯加热
4.下列有关溶液的叙述正确的是
A.一杯食盐水,下部分比上部分咸
B.温度一定时,析出硝酸钾晶体的溶液未必是硝酸钾的饱和溶液
C.物质溶于水时,常使溶液的温度发生改变
D.75%的医用酒精消毒液,溶剂是酒精
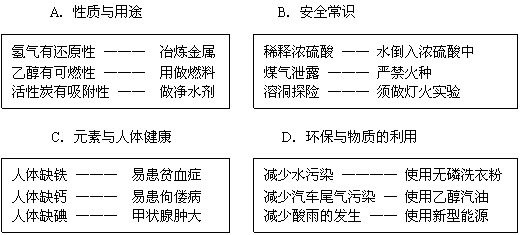 5.下面是王小莉同学用连线的方式对某一主题知识进行归纳的情况,其中有错误的一组是
5.下面是王小莉同学用连线的方式对某一主题知识进行归纳的情况,其中有错误的一组是
6.某同学想用实验证明FeCl3溶液显黄色不是Cl―离子造成的,下列实验无意义的是
A.观察KCl溶液没有颜色
B.向FeCl3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失
C.FeCl3溶液中滴加适量无色硝酸银溶液,振荡后静置,溶液黄色未消失
D.加水稀释后FeCl3溶液黄色变浅
第二卷
二、填空与简答题(本题包括5小题,共32分)
7.(4分)苏丹红是一类染色剂。在我们日常接触的物品中,家用的红色地板漆或红色鞋油通常含有苏丹红的成分。根据2004年4月MSDS提供的数据,苏丹红存在有限的致癌作用,不可服用。2005年2月23日中国政府发布紧急公告,禁止苏丹红作为食品添加剂。下表是苏丹红1号的有关信息:
编号
化学式
C16H12N2O
①
外观
暗红色或深黄色片状晶体
②
溶解度
在水中:<0.01g/100ml; 汽油中:任意比例互溶
③
熔点
404~406 ℃
④
升华
475 ℃
⑤
致癌原因
在人体内分解出一种有毒的有机物(苯胺)
试回答下列问题:
(1)苏丹红1号中含有 元素,其相对分子质量为 。
(2)在上表给出的信息中,属于苏丹红一号物理性质的有(填编号) 。
(3)苏丹红1号对动物和人体有致癌作用,主要是因为该物质在体内发生了 变化。
8.(8分)化学科学中许多原理与我们的生活、生产以及其他科学中的道理是一致的。请用短线将A栏与B栏相互关联的两项连接起来。
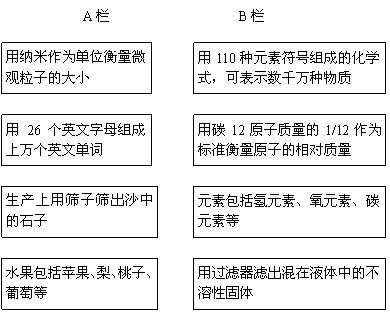
9.(4分)化学是关于人类如何应用物质的科学。根据你对化学反应的理解,回答下列问题:
(1)人类利用化学反应,可以获取生活和生产所需的 和 。另外,人类还利用化学反应消除有害物质。
(2)在铁制品表面镀上一层保护膜,是为了防止和减缓铁的锈蚀;在实验室里用氯酸钾制氧气时,加热和加入二氧化锰是为了加快反应速率。虽然物质之间的化学反应极其复杂,但是人类可以根据物质的 ,通过改变 来控制化学反应。
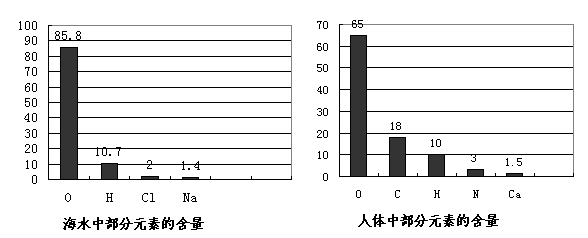 信息2:下图分别是海水和人体中部分元素的质量分数。
信息2:下图分别是海水和人体中部分元素的质量分数。
根据
上面提供的信息,运用你学过的有关知识回答下列问题:
(1)在海水中,金属元素含量最高的是钠元素。 我国青海湖是个内湖,其湖水是不能流到大海中,湖水与海水相似也是咸的,而地球上多数的湖水是淡的。从物质在水中溶解的规律和水的天然循环的角度看,海水中钠元素的含量比较高的原因是
。
(2)水中氧元素的质量分数比海水中氧元素的质量分数(填“大”或“小”) 。
人体中碳元素的相对含量较多的原因是
。
(3)原始大气是指绿色植物出现以前的大气。假设把现代的人或其他的动植物放在原始大气中,你认为他们能否生存下去? 。原因是
。
(4)绿色植物出现以后,原始大气中的CO2逐渐减少。同时O2逐渐增加,原因是 。
(5)随着原始大气中O2缓慢地增加,CH4、NH3、CO等气体逐渐被氧气氧化而缓慢地减少,使大气的成分逐渐演化成现代大气。原始大气中NH3可转化为现代大气中的 。试写出氧气分别与CO、CH4反应的化学方程式。
;
。
11.(6分)在宏观物质、微观粒子和化学符号之间建立联系,是化学科学特有的思维方式。已知氢、碳、氧、钠、氯五种元素的核电荷数分别为1、6、8、11、17。试按下列要求,写出微观粒子的化学符号,以及由这种粒子构成的或含有这种粒子的一种物质的名称(微观粒子和物质所涉及的元素限定在上述5种元素内)。
需满足的条件
粒子的化学符号
对应的物质的名称
(1)质子数为11的同种元素的原子和离子
(2)质子数均为10的两种不同的分子
(3)质子数为1的阳离子和质子数为9的阴离子
三、实验与探究(本题包括1小题,共10分)
12.(10分)铁暴露在空气中会生锈。不知你注意了没有,将苹果切开不久,果肉上就会产生一层咖啡色的物质,也好象是生了“锈”一样。某化学活动小组对此进行了探究。
【提出问题】切开的苹果“生锈”与什么因素有关?
【猜想与假设】
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”。
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”;
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”;
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”;
猜想⑤:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关。
【收集证据】
(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的一种物质发生反应,生成咖啡色的物质。
(二)实验探究:针对上面的猜想①至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次观察到下列实验现象。请你将他们设计的可行的实验探究方案,填写在下表中。
猜想
可行的实验方案
观察到的实验现象
猜想①
将一小块果肉浸入盛有蒸馏水的烧杯中,观察现象。
果肉表面不变色。
猜想②
果肉表面变色。
猜想③
果肉表面不变色。
猜想④
果肉表面不变色。
猜想⑤
温度高的先变色。
【得出结论】
。
【反思与评价】 (1)在②―⑤四种猜想中,你认为猜想 (填代号)最不合理,理由是
。
(2)在验证猜想①时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是 。
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施是
。
四、实验与计算(本题包括1小题,共10分)
13.(10分)小明家购买了一瓶白醋,标签上注明醋酸的质量分数≥5%。小明想,这瓶白醋中醋酸的含量是否与标签的标注相符?
请你与小明一起,用有关酸碱的知识,定量测定白醋中醋酸的含量。
【实验原理】
(1)用已知浓度的氢氧化钠溶液和醋酸反应,反应的化学方程式为:
CH3COOH + NaOH = CH3COONa + H2O。
(2)在混合溶液中,当醋酸和氢氧化钠完全中和时,再增加1滴氢氧化钠溶液,溶液就呈碱性,而1滴氢氧化钠溶液约为0.05 mL,对测定结果的影响很小,可忽略不计。
【实验步骤】
①用 取12.0 mL白醋(密度近似为1.0g/ mL),倒入烧杯中,再加入20 mL蒸馏水稀释。
②量取45.0 mL溶质质量分数为1.0%的氢氧化钠溶液(密度近似为1.0 g/ mL),用胶头滴管取该氢氧化钠溶液,逐滴地滴加到稀释后的白醋中,同时不断地搅拌烧杯中的溶液。滴至恰好完全反应,剩余氢氧化钠溶液5.0 mL。
【交流反思】
(1)在实验步骤①中,加适量水稀释白醋,对实验结果有无影响?为什么?
(2)在实验步骤②中,小明如何确定醋酸和氢氧化钠已完全中和?
【数据处理】根据实验数据,通过计算判断白醋中醋酸的含量是否与标签的标注相符?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com