
2006-2007学年度烟台市栖霞初四摸底考试
化 学 试 题(2007.04)
注意事项:考生将自己的姓名、考号、考试科目涂写在答题卡上,选择题的答案选出后,甩铅笔把答题卡对应题目的答案标号涂黑,如有改动必须用橡皮擦千净,再选涂另一个答案,考试结束后交答题卡和试卷。
可能用到的相对原子质量:K 39 C 12 O 16 C1 35.5 Fe 56 Ca 40 Si 28 A1 27 N l 4
一、选择题(本题包括l0个小题,每小题1分,共10分,每小题只有1个选项符合题意)
1.下列物质的用途只与物质的物理性质有关的是
A.干冰用于人工降雨 B.用熟石灰中和土壤的酸性
C.液氧用作火箭的助燃剂 D.氢氧化钠用于制肥皂
2.材料与人类生活紧密相关。下列物品与所用材料的对应关系不正确的是
A.羊绒衫一天然纤维 B.不锈钢餐具一铁合金
C.食品袋一塑料 D.汽车轮胎一塑料
3.下列做法正确的是
A.用工业用盐亚硝酸钠腌鱼肉。 B.添加“瘦肉精”喂猪以增加瘦肉
C.用X射线照射胃部前服用碳酸钡 D.使用可降解塑料食品袋
4.以下是三种气体的密度(0℃、101kPa)和溶解度(20℃、101kPa)。

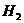
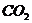

密度/g/L
0.0899
1.977
2.716
溶解度/g
0.0001603
0.1688
11.28
实验室收集 气体,可采用的方法是
气体,可采用的方法是
A.向上排空气法 B.向下排空气法
C.排水集气法 D.既可用向上排空气法,又可用排水集气法
5.油炸食物不宜多吃,因为食物长时间煎炸后产生微量的丙烯醛(化学式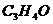 )等有毒物质会损害人体健康。下列有关丙烯醛的说法不正确的是
)等有毒物质会损害人体健康。下列有关丙烯醛的说法不正确的是
A.该物质由碳、氢、氧三种元素组成
B.该物质中碳、氢、氧三种元素的质量比为9:1:2
C.该物质的分子中碳、氢、氧原子的个数比为3:4:1
D.该物质在空气中完全燃烧的产物是二氧化碳和水
6.为探究二氧化碳与氢氧化钠溶液是否发生反应,某同学设计了下图所示的实验方案,其中不可行的是
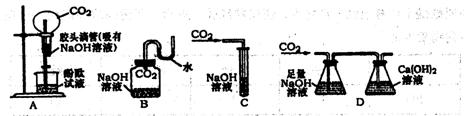
7.学校研究性学习小组选择探究“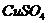 溶液显蓝色与什么离子有关?”作为研究课题,以下是他们提交的实验方案,其中不需要做的实验是
溶液显蓝色与什么离子有关?”作为研究课题,以下是他们提交的实验方案,其中不需要做的实验是
A.观察 、
、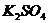 溶液的颜色
溶液的颜色
B.观察 、
、 溶液的颜色
溶液的颜色
C.加水稀释后观察溶液的颜色
D.向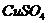 溶液中滴加适量的
溶液中滴加适量的 溶液,静止后观察溶液的颜色
溶液,静止后观察溶液的颜色
8.取70g某温度下的氯化钾饱和溶液,将其恒温蒸发10g水,析出4g氯化钾固体,则剩余溶液所含溶质质量为
A.16g B.20g C.40g D.56g
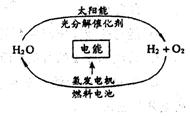
9.目前,科学家提出了一种经济而且理想的获得氢能的循环体系(如下图)。关于此循环体系,下列说法中错误韵是
A.燃料电池能够使化学反应产生的能量转化为电能
B.该氢能源的循环体系能够实现太阳能转化为电能
C.在此循环中发生了反应: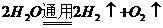
D.眉前化学家急需解决的问题是寻找合适的光照条件下分解水的催化剂
10.缺钙能导致儿童发育不良或佝偻病。小明同学从食物中摄入钙元素不足,每天还需要服用2片某钙片。该钙片标签的部分内容如下右图所示(钙片中只有碳酸钙含有钙元素),小明每天从钙片中摄入钙元素的质量为

A.0.30G B:0.60g C.0.75g D.1.50g
二、选择题(本题包括l0个小题,每小题2分,共20分,每小题有l或2个选项符合题意)
11.等电子体具有原子数目相同,电子数目相同的特征。下列各组中属于等电子体的是
A.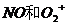 B.
B.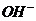 和
和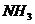 C.
C.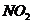 和
和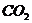 D.
D.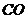 和
和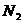
12.家庭中的一些常见物质的pH,蚊子、蜂、蚂蚁等昆虫叮咬人时,会向人体射入一种叫蚁酸(具有酸性)的物质,使皮肤红肿、瘙痒。要清除这种症状,可在叮咬处涂抹下列物质中的
物质;
食醋
牙膏
肥皂水
火碱水
PH
3
9
10
13
A.牙膏 B.肥皂水 C.火碱液 D.食醋
13.下图所示的实验操作中正确的是

14.小王在家里用鸡蛋壳与盐酸反应,证明鸡蛋壳里是否含有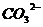 ,其中正确的是
,其中正确的是
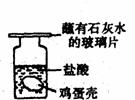
A.若有气泡产生且玻璃上出现浑浊,说明鸡蛋壳里含有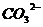
B.能与盐酸反应产生大量气体的物质中一定含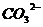
C.若玻璃片上的石灰水没有变浑浊说明鸡蛋壳里没有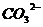
D.若玻璃片上的石灰水没有变浑浊,有可能是盐酸中溶质质量分数过大
15.已知钾、钠等活泼金属在常温下能与水发生剧烈反应。例如金属钠可与水反应: ,据此判断下列说法不正确的是
,据此判断下列说法不正确的是
A.钠与水反应属于置换反应
B.反应前钠与水的质量一定等于生成氢氧化钠和氢气的质量
C.石蕊试液滴入钠和水反应后的溶液中会变成蓝色
D.能用手直接拿取金属钠
16.某有机物的相对分子质量为46,4.6克该物质在氧气中充分燃烧生成8.8克二氧化碳和5.4克水,据此判断,该有机物
A.只有碳、氢两种元素组成 B.一定含有碳、氢、氧三种元素
C.化学式为CH2O2 D.分子中C、H、O原子个数比为2:6:1
17.利用化学实验可以鉴别生活中的一些物质。下表中各组物质的鉴别方法能将本组待鉴别的物质都区分出来的是
待鉴别物质
鉴别方法
A
硬水。软水
加肥皂水,搅拌,观察产生泡沫的多少
B
_
N2、O2、CO2、空气
用燃着的木条检验,观察木条燃烧情况
C
棉纤维、羊毛纤维、涤纶
闻燃烧产生的气味,观察燃烧情况和灰烬
D
Zn、Fe
加入 溶液
溶液
18.1991年著名物理学家卢瑟福等人为探索原子的内部结构进行了下面的实验。他们用一束带正电的、质量比电子大得多的高速运动的 粒子轰击金箔,发现:①大多数
粒子轰击金箔,发现:①大多数 粒子能穿透金箔而不改变原来的运动方向;②一小部分
粒子能穿透金箔而不改变原来的运动方向;②一小部分 粒子改变了原来的运动方向;③有极少数
粒子改变了原来的运动方向;③有极少数 粒子被弹了回来。由此推出关于原子内部结构的一些假设不合理的是
粒子被弹了回来。由此推出关于原子内部结构的一些假设不合理的是
A.原子核体积很小 B.原子是一个实心球体
C.原子核与 粒子带同种电荷
D.原子内有相对较大的空间
粒子带同种电荷
D.原子内有相对较大的空间
19.向一定量的饱和氢氧化钠溶液中,加入少量的氧化钠(氧化钠与水反应生成氢氧化钠),恢复到原来的温度时,下列说法正确的是
A.溶液中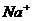 的总数不变
B.单位体积内的
的总数不变
B.单位体积内的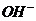 数目不变
数目不变
C.溶液溶质质量分数不变 D.溶液质量不变
20.已知
 硅不与盐酸反应。将含铁、铝、硅的合金样品分为等质量的两份,分别与足量的稀盐酸和烧碱溶液充分反应,测得放出的氢气质量相同。则该合金样品中铁、铝、硅的质量比不可能是
硅不与盐酸反应。将含铁、铝、硅的合金样品分为等质量的两份,分别与足量的稀盐酸和烧碱溶液充分反应,测得放出的氢气质量相同。则该合金样品中铁、铝、硅的质量比不可能是
A.112:81:28 B.56:81:56 C.324:135:36 D.56:27:14
三、填空题(29分)
21.食物是维持人类生命和健康的支柱。下表是某食品包装袋上的说明:
品名
×××蔬菜苏打饼
配料
小麦粉、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、
脱水青菜、橙汁、碳酸氢钠
从该说明的配料中分别选出一种物质,填在相应的横线上:
(1)富含蛋白质的是____________;富含油脂的是_____________;富含维生素的是____.
(2)属于无机盐的是_______________.
22.写出符号中数字“2”的意义或根据要求写出相应的符号:
(1)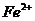 __________________________________________________;
__________________________________________________;
(2)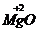 __________________________________________________;
__________________________________________________;
(3)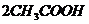 __________________________________________________;
__________________________________________________;
(4)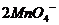 __________________________________________________;
__________________________________________________;
(5)同一种元素的原子和离子____________、________________。
(6)质子数相同的两种不同的分子____________、________________。
(7)电子数相同的两种不同的离子____________、________________。
23.除去粗盐中的少量泥沙,第一步操作是溶解。溶解时应在_____(填一种仪器名称)里进行;第二步操作是对制成的液体进行_____;第三步操作是将滤液加热蒸发,待蒸发皿中出现_____固体时应熄灭酒精灯。在三步操作中都用到玻璃棒,玻璃样作用分别是:①_____________________;②_________________;③__________________________;
24.碱式碳酸铜(相对分子质量为222)加热完全分解后生成的黑色固体物质是什么?甲乙丙三位同学对此进行了探究。他们称取了4.44g碱式碳酸铜在试管中高温加热使之完全分解,冷却至室温后,称量黑色固体产物质量为3.2g。
他们结合碱式碳酸铜的化学式对黑色固体产物做出以下猜想:①可能是氧化铜②可能是炭粉③可能是氧化铜和炭粉的混合物。以上猜想的理由是:___________、______________。
(1)甲同学设计的实验方案是:向盛有少量该黑色固体的试管中加入足量的稀硫酸,充分振荡,静置后观察现象。
如果猜想①正确,现象应该是______________________________________;
如果猜想③正确,现象应该是______________________________________;
(2)乙同学从资料中得知:碳、氢气、一氧化碳在加热或高温条件下都能夺取金属氧化物中的氧,使其变为金属单质。他经过思考后,认为猜想③可以排除,他的理由是 _________________________________________________________________________。
(3)丙同学通过对得到的实验数据进行计算,排除了猜想②,他的理由是(通过计算式说明)_______________________________________。
25.下图是两种常用化肥包装袋上的部分说明,根据图回答下列问题:
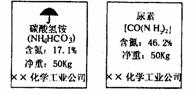
(1)保存碳酸氢铵应注意________________________;
(2)这包尿素的纯度可达________________________。
(3)根据农技员计算,小军家小麦地需要200kg碳酸氢铵,而小红则建议他买含氮量高的化肥,到化肥经销处后,小军面对价格犹豫不决。(假设表中化肥均为纯品)请你帮他计算一下,他应买___________。
价格表
品种
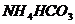
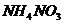

价格(元/kg)
0.54
1.05
1.25
四、简答题(11分)
26.小刚在实验室发现,盛放 溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。小刚叫来小军和小红,共同探究这种白色粉末的成分。他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:
溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。小刚叫来小军和小红,共同探究这种白色粉末的成分。他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:
(1)可能是氢氧化钠(2)可能是碳酸钠(3)可能是氢氧化钠和碳酸钠的混合物。为了证明猜想,他们分别做了下面的实验:
小刚取少量白色粉末,滴加稀盐酸,有气体生成。由此小刚认为自色粉末是碳酸钠。请你判断小刚所得结论是否正确,并简述理由:___________________________。
小军取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变红色。由此小军认为白色粉末是氢氧化钠。请判断小军所得的结论是否正确,并简述理由。_______________。
小红取少量白色粉末溶于水,向所得溶液中滴加 液,有白色沉淀产生。由此判断白色粉末中含有____________。为了验证猜想3,小红继续向溶液中滴加
液,有白色沉淀产生。由此判断白色粉末中含有____________。为了验证猜想3,小红继续向溶液中滴加 溶液至不再产生沉淀为止,然后过滤。你认为她接下来应进行的实验是____________________。
溶液至不再产生沉淀为止,然后过滤。你认为她接下来应进行的实验是____________________。
在小红所做的实验中,若把 溶液换成
溶液换成 溶液是否可行?请简述理由。______。
溶液是否可行?请简述理由。______。
27.如图所示,在甲、乙两只试管中,装有足量的质量和溶质质量分数均相同的稀盐酸,在两只试管上方各罩一个完全相同的气球,两个气球中分别装有相同质量的金属A和金属B,现同时提起两只气球,使其中的金属迅速与稀盐酸接触反应。实验发现:开始时,甲气球迅速鼓起,而乙气球鼓起较慢。反应结束时,甲气球鼓起的体积比乙气球大。根据以上事实,可得出以下结论:
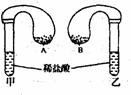
(1)_______________________________;(2)________________________________
(3)若在上述条件下,A、B两种金属与盐酸反应均生成+2价盐。据此还可以得到的结论是:_____________________________________________________________。
五、实验题;(21分)
28.化学实验室要把一些回收的氯化钠配制成质量分数为l6%的氯化钠溶液。据此回答下列问题:
(1)若称量发现回收的氯化钠共9.6g,则需要水的质量是___________g。
(2)下图是某同学配制过程中的部分操作,请用字母排出正确的顺序
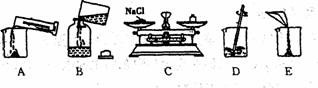
(3)将配制好的溶液装瓶保存,以备以后使用,最好装________________瓶中。
(4)下列错误操作可能导致溶质质量分数偏高的是___________________。(填序号)
①称量氯化钠时砝码和氯化钠放错托盘
②量水时俯视凹液面的最低处读数
③搅拌溶解时有少量水溅出
④装瓶过程中溶液洒出。
(5)请你为配制好的溶液设计标签,将标签内容填写在下边

29.纳米材料具有特殊的性能。“引火铁”(极细的铁粉)是一种准纳米材料,它在空气中可以自燃。下图所示是新制的四氧化三铁与纯净的氢气制备“引火铁”的装置。
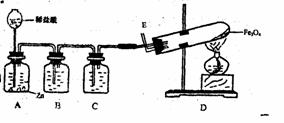
(1)四氧化三铁与氢气反应生成“引火铁”的化学方程式_______________________。
(2)B、C中所盛的物质是:B__________________;C______________________。
(3)加热前, 如何使用实验来检验装置中空气是否排尽?____________________。
(4)未参加反应的氢气直接排入实验室中,可能引起爆炸。应该用什么方法处理? _____________________________________________________。
30.小玉同学在探究浓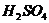 、
、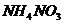 固体、
固体、 固体在水中溶解的热量变化情况时,设计了如下图所示的实验装置,请回答下列问题:
固体在水中溶解的热量变化情况时,设计了如下图所示的实验装置,请回答下列问题:
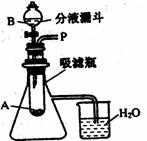
(1)若试管中的物质A是 固体,分液漏斗中的物质B是_________,打开分液漏斗,开关,向试管中滴加物质B,观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______________________________________________________。
固体,分液漏斗中的物质B是_________,打开分液漏斗,开关,向试管中滴加物质B,观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______________________________________________________。
(2)若试管中的物质A是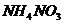 固体,打开分液漏斗开关,向试管中滴加水,你能观察到的现象是:
固体,打开分液漏斗开关,向试管中滴加水,你能观察到的现象是:
①________________________________________;
②________________________________________。
(3)若小玉探究是的浓硫酸在水中溶解时热量的变化情况,则试管中的物质A是_______。
(4)小芳同学认为该装置还可以用来探究镁条与盐酸反应的能量变化情况,若物质A是镁条,加入稀盐酸后,你能观察到的实验现象是:
①_________________________;②_________________________。若要在P点处点燃产生的气体,必须进行的操作是__________。
六、计算题(9分)
31.葡萄糖( )在体内经缓慢氧化生成二氧化碳和水,释放出热量。每90g葡萄糖完全氧化,可以产生大约l402kJ热量。若500g5%的葡萄糖注射液中葡萄糖完全氧化,至少消耗氧气多少克?大约释放多少千焦热量?(计算结果取整数)
)在体内经缓慢氧化生成二氧化碳和水,释放出热量。每90g葡萄糖完全氧化,可以产生大约l402kJ热量。若500g5%的葡萄糖注射液中葡萄糖完全氧化,至少消耗氧气多少克?大约释放多少千焦热量?(计算结果取整数)
32.草木灰是农村常用的一种化肥(主要成分是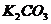 )。某兴趣小组为了测定草木灰中
)。某兴趣小组为了测定草木灰中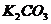 的含量,取现有的草木灰7.5g逐滴加入稀盐酸至恰好完全反应,消耗稀盐酸45g,过滤除去杂质,得到溶液45.5g。(已知
的含量,取现有的草木灰7.5g逐滴加入稀盐酸至恰好完全反应,消耗稀盐酸45g,过滤除去杂质,得到溶液45.5g。(已知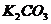 与
与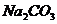 的化学性质相似,假设草木灰中除
的化学性质相似,假设草木灰中除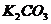 外,其他物质均不溶于水,也不与盐酸反应)试计算:
外,其他物质均不溶于水,也不与盐酸反应)试计算:
(1)该草木灰中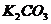 的质量分数。(2)反应后所得溶液中溶质的质量分数。
的质量分数。(2)反应后所得溶液中溶质的质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com